東大塾長の山田です。
このページでは燃料電池について解説しています。
燃料電池は環境に優しい電池です。各電極での反応を詳しく説明しています。是非参考にしてください。
1. 燃料電池とは?
外部から燃料を供給して、それらの酸化還元反応で得られる燃料熱えお効率的に電気エネルギーに変える装置のことを燃料電池といいます。
燃料電池には様々な種類がありますが、ここでは水素ー酸素燃料電池について解説します。
水素ー酸素燃料電池は、負極活物質、正極活物質にそれぞれ水素と酸素を使用します。つまり、水素を還元剤、酸素を酸化剤として原料供給し電気エネルギーを得るのです。この燃料電池の生成物は水であるので、クリーンな発電として注目されています。
この燃料電池は、電解液の種類によっておこる化学変化が異なります。ここでは、リン酸型燃料電池とアルカリ型燃料電池の2種類の仕組みについて詳しく見ていきましょう。
1.1 リン酸型燃料電池
まず、リン酸型燃料電池の仕組みについて解説します。
【リン酸型燃料電池の仕組み】
① 負極で水素\(H_2\)が酸化されて電子\(e^-\)を放出して水素イオン\(H^+\)となる。
負極側では、水素\(H_2\)が還元剤となります。供給された\(H_2\)は酸化され電子\(e^-\)を放出し水素イオン\(H^+\)になります。このとき反応しなかった\(H_2\)はそのまま外に排出されます。
負極で起こる反応の反応式は電解液がリン酸の時は次のようになります。
\(H_2 →2H^+ + 2e^-\)
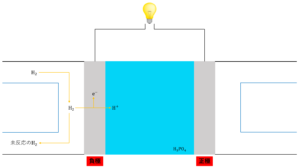
② 放出された電子\(e^-\)は導線を通り正極に流れ込み、\(H^+\)は電解液中を正極に向かって移動する。
①の反応で発生した電子は導線を通り正極に流れ込みます。また、同様に①で発生した水素イオンは電解液中を正極の方へ移動していきます。
このとき、電子が通過することで(電流が発生して)豆電球が点灯します。
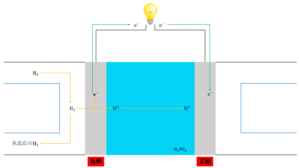
③ 酸素\(O_2\)が電子を受け取り還元され、\(H_2O\)を生成する。
正極側では、酸素\(O_2\)が酸化剤になります。①で発生し②で正極へ移動した\(e^-\)、\(H^+\)と正極に供給された\(O_2\)が反応します。\(O_2\)は電子を受け取り還元され\(H_2O\)になります。このとき反応しなかった\(O_2\)はそのまま外に排出されます。
正極で起こる反応の反応式は電解液がリン酸の時は次のようになります。
\(O_2 + 4H^+ + 4e^- →2H_2O\)
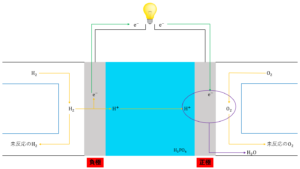
以上①~③がリン酸型燃料電池の仕組みです。
燃料電池の構成を表す電子式は次のとおりです。
\((-)H_2 | H_3PO_4 aq | O_2(+)\)
また、負極、正極で起こる反応の反応式を電子を消去するように足し合わせると次のようになります。
\(2H_2 + O_2 →2H_2O\)
となります。これが全体の反応の反応式を表したものです。
1.2 アルカリ型燃料電池
次に、アルカリ型燃料電池の仕組みについて解説します。ここでは、塩基性の溶液を\(KOH\)とします。
【アルカリ型燃料電池の仕組み】
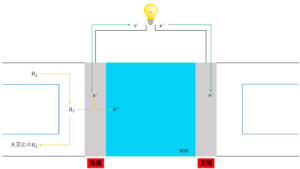
① 負極で水素\(H_2\)が酸化されて電子\(e^-\)を放出して水素イオン\(H^+\)となる。
負極側では、水素\(H_2\)が還元剤となります。供給された\(H_2\)は酸化され電子\(e^-\)を放出し水素イオン\(H^+\)になります。このとき反応しなかった\(H_2\)はそのまま外に排出されます。
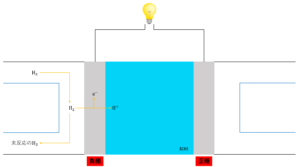
② 放出された電子\(e^-\)は導線を通り正極に流れ込み、\(H^+\)は電解液中を正極に向かって移動する。
①の反応で発生した電子は導線を通り正極に流れ込みます。また、同様に①で発生した水素イオンは電解液中を正極の方へ移動していきます。
このとき、電子が通過することで(電流が発生して)豆電球が点灯します。
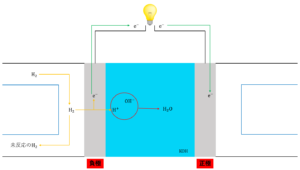
③ \(KOH\)から電離した\(OH^-\)が\(H^+\)と反応し、\(H_2O\)が生成する。
①で発生した\(H^+\)が電解液中に存在している\(OH^-\)が反応し\(H_2O\)が生成します。
これより、負極で起こる反応の反応式は電解液が塩基性のとき次のようになります。
\(H_2 + 2OH^- →2H_2O + 2e^-\)
④ 負極から流れてきた\(e^-\)と③で生成した\(H_2O\)が\(O_2\)と反応する。
負極から流れてきた\(e^-\)と③で発生した\(H_2O\)が正極に供給された\(O_2\)と反応して\(OH^-\)が生成します。
正極で起こる反応の反応式は電解液が塩基性の溶液の時は次のようになります。
\(O_2 + 2H_2O+ + 4e^- →4OH^-\)
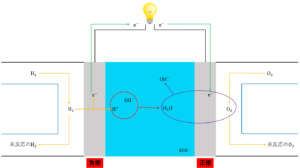
以上①~③がアルカリ型燃料電池の仕組みです。
燃料電池の構成を表す電子式は次のとおりです。
\((-)H_2 | KOH aq | O_2(+)\)
また、負極、正極で起こる反応の反応式を電子を消去するように足し合わせると次のようになります。
\(2H_2 + O_2 →2H_2O\)
となります。これが全体の反応の反応式を表したものです。
アルカリ型燃料電池では、正極で使う\(H_2O\)を負極が、負極で使う\(OH^-\)を正極で作り出しているので、燃料電池は連続的にエネルギーを生み出すことができます。
2. 燃料電池の特徴
アルカリ型燃料電池を用いる場合には、できるだけ純粋な水素や酸素を供給する必要があります。供給する水素や酸素に二酸化炭素\(CO_2\)が含まれていると、\(CO_2\)が電解液と反応し電解液中に炭酸イオン\({CO_3}^{2-}\)が生成し、電池の性能を低下させてしまいます。
リン酸型燃料電池の場合には、白金触媒を含む多孔質の黒鉛板または金属膜などを電極として使います。
常温では、白金などの触媒がないと水素、酸素はほとんど反応しません。しかし、白金触媒があることによって常温でも水素と酸素はゆっくり反応します。
白金触媒は、水素ー酸素燃料電池にとって重要な存在であるのですが、白金のような高価な触媒が必要であることが燃料電池の実用化の障害になっています。
3. まとめ
最後に、燃料電池についてまとめておこうと思います。
① 負極で水素\(H_2\)が酸化されて電子\(e^-\)を放出して水素イオン\(H^+|)となる。
② 放出された電子\(e^-\)は導線を通り正極に流れ込み、\(H^+\)は電解液中を正極に向かって移動する。
③ 酸素\(O_2\)が電子を受け取り還元され、\(H_2O\)を生成する。
負極:\(H_2 →2H^+ + 2e^-\)
正極:\(O_2 + 4H^+ +4e^- →2H_2O\)
① 負極で水素\(H_2\)が酸化されて電子\(e^-\)を放出して水素イオン\(H^+|)となる。
② 放出された電子\(e^-\)は導線を通り正極に流れ込み、\(H^+\)は電解液中を正極に向かって移動する。
③ 塩基性の溶液中に電離している\(OH^-\)が\(H^+\)と反応し、\(H_2O\)が生成する。
④ 負極から流れてきた\(e^-\)と③で生成した\(H_2O\)が\(O_2\)と反応する。
負極:\(H_2 + 2OH^- →2H_2O + 2e^-\)
正極:\(O_2 + 2H_2O +4e^- →4OH^-\)
燃料電池は環境に優しく注目されている電池です。難しくないのでこの記事を何度も読み返してしっかりマスターしてください!














水素ー酸素燃料電池の全体反応は、\(2H_2 + O_2 →2H_2O\)で、これは水素の燃焼反応と同じになります。このため、この電池では水素の燃焼熱が直接電気エネルギーに変換されます。したがって、水素ー酸素燃料電池は環境に優しく、エネルギー効率の良い電池です。