東大塾長の山田です。
このページでは鉛蓄電池について解説しています。
放電、充電の仕組みや計算問題の例など詳しく説明しています。是非参考にしてください。
1. 鉛蓄電池とは?
1800年代後半に実用化された代表的な二次電池で、鉛\(Pb\)板と酸化鉛(Ⅳ)\(PbO_2\)板を希硫酸\(H_2SO_4\)に浸した電池のことを鉛蓄電池といいます。
外部の直流電池から放電時とは逆向きの電流を流すことで、起電力を回復させることができる電池のことを二次電池といいます。このような逆向きの電流を流すことを充電といい、二次電池は蓄電池とも呼ばれます。
まず、鉛蓄電池の仕組みについて説明していきましょう。
【鉛蓄電池の仕組み】
① 鉛\(Pb\)板が酸化され硫酸鉛\(PbSO_4\)になり、電子\(e^-\)を放出する。
まず、鉛\(Pb\)板と酸化鉛(Ⅳ)\(PbO_2\)板のどちらの板が酸化され電子を放出するのか考えていきましょう。
これには、\(Pb^{2+}\)と\(Pb^{4+}\)の安定性について考える必要があります。鉛\(Pb\)板、酸化鉛(Ⅳ)\(PbO_2\)板が溶解するとそれぞれ\(Pb^{2+}\)と\(Pb^{4+}\)になります。
この2つのイオンの安定性は\(Pb^{2+}>Pb^{4+}\)となっています。つまり、\(Pb^{2+}\)の方が安定でより、鉛\(Pb\)板の方がより溶解しやすいということになります。
\(Pb^{4+}\)が\(Pb^{2+}\)になるため反応は還元反応であり、電子を受け取る必要があるということからもこのことは正しいと考えることができます。
このとき、鉛\(Pb\)板が酸化されて硫酸鉛\(PbSO_4\)になり電子を放出します。すなわち、\(Pb\)板は電子を放出する電極(負極)になります。
負極での反応を細かく説明すると、手順は次のようになります。
まず、\(Pb\)板が酸化され、\(Pb^{2+}\)になります。
このときの反応の反応式は、
\(Pb →Pb^{2+} + 2e^-‥‥(1)\)
となります。
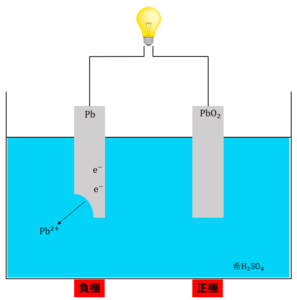
次に、放出された電子\(e^-\)が酸化鉛\(PbO_2\)板の方へ移動します。
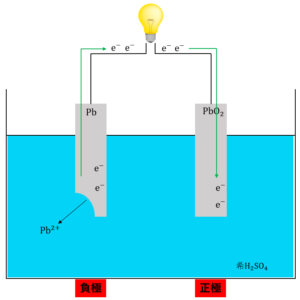
最後に、発生した\(Pb^{2+}\)が溶液中の\({SO_4}^{2-}\)とくっつき\(PbSO_4\)を生成します。
このときの反応の反応式は、(1)式の両辺に\({SO_4}^{2-}\)を加えたものであるから、
\(Pb + {SO_4}^{2-} →PbSO_4 + 2e^-‥‥(2)\)
となります。
(2)式が負極で起こっている反応になります。
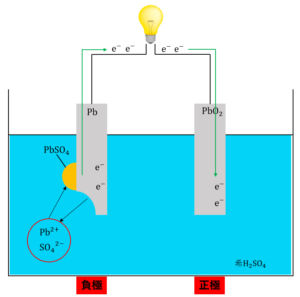
② 酸化鉛\(PbO_2\)板が流れてきた電子\(e^-\)を受け取り、還元されて硫酸鉛\(PbSO_4\)になる。
酸化鉛\(PbO_2\)板では、酸化鉛\(PbO_2\)が流れてきた電子\(e^-\)を受け取り、還元されて硫酸鉛\(PbSO_4\)になります。すなわち、\(PbO_2\)板は電子を受け取る電極(正極)になります。
正極での反応を細かく説明すると、手順は次のようになります。
まず、負極から流れてきた電子\(e^-\)を\(PbO_2\)を構成している\(Pb^{4+}\)が受け取って、溶液中に\(Pb^{2+}\)として溶け出します。
このときの反応の反応式は、
\(PbO_2 + 4H^+ + 2e^- →Pb^{2+} + 2H_2O‥‥(3)\)
となります。
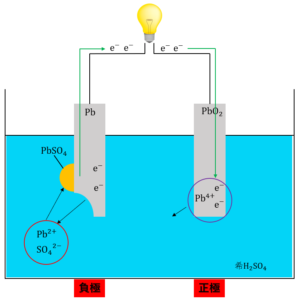
次に、発生した\(Pb^{2+}\)が溶液中の\({SO_4}^{2-}\)とくっつき\(PbSO_4\)を生成します。
このときの反応の反応式は、(3)式の両辺に\({SO_4}^{2-}\)を加えたものであるから、
\(PbO_2 + 4H^+ + {SO_4}^{2-} + 2e^- →PbSO_4 + 2H_2O‥‥(4)\)
となります。
(4)式が正極で起こっている反応になります。
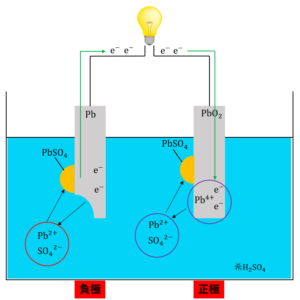
以上①、②が鉛蓄電池の仕組みです。
鉛蓄電池の構成を表す電子式は次のとおりです。
\((-)Pb|H_2SO_4 aq|PbO_2(+)\)
また、この電池全体では次の酸化還元反応が起こります。
\(Pb + 2H_2SO_4 + PbO_2 →2PbSO_4 + 2H_2O\)
これは、(2)式と(4)式を足し合わせたものです。
2. 充電
改めて放電、充電について解説します。
電子を負極から正極に流して電流を発生させることを放電、それとは逆向きに電流を流すことを充電といいます。また、鉛蓄電池のように充電を行い繰り返し使用できる電池を二次電池といい、ダニエル電池のように一回しか使用できない電池のことを一次電池といいます。
ここでは、鉛蓄電池の充電の仕組みについて解説します。充電を開始する前の鉛蓄電池は放電を終え、鉛\(Pb\)板と酸化鉛\(PbO_2\)板に硫酸鉛\(PbSO_4\)が付着した状態です。
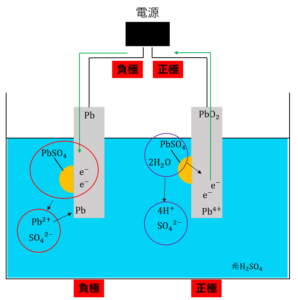
【充電の仕組み】
まず、外部の直流電源の正極に鉛蓄電池の正極を、外部の直流電源の負極に鉛蓄電池の負極を接続します。「ボルタ電池とは(仕組み・分極の原理など)」の記事で説明したように、導線に向かって電子が流れ出す電極を負極と呼びました。よって、電源の負極から鉛蓄電池の負極に向かって電子\(e^-\)が流れ込みます。
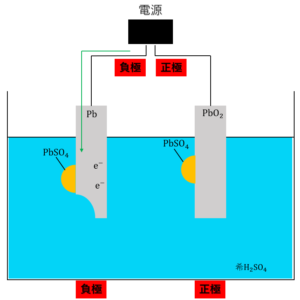
このとき、負極では放電のときと逆の反応が起こります。
\(PbSO_4 + 2e^- →Pb + {SO_4}^{2-}\)
これが充電時の鉛蓄電池の負極での反応です。
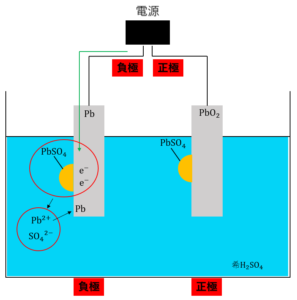
また、鉛蓄電池の正極では電流が逆向きになることから電子を放出します。このとき、正極でも放電のときの反応と逆の反応が起こります。
\( PbSO_4 + 2H_2O →PbO_2 + 4H^+ + {SO_4}^{2-} + 2e^-\)
これが充電時の鉛蓄電池の正極での反応です。
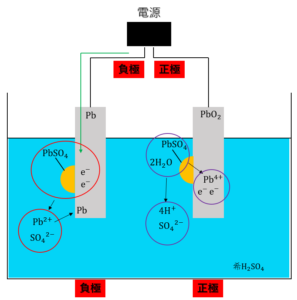
鉛蓄電池の正極から放出された電子は電源の正極に電子が流れ込みます。したがって、導線から電子が流れ込む電極が正極であるという正極の定義にも当てはまりますよね。
これより、充電時の鉛蓄電池全体での反応は
\( 2PbSO_4 + 2H_2O →Pb + 2H_2SO_4 + PbO_2\)
となります。
この式を見てわかるように、充電することで放電する前の状態に戻すことができるので何度でも繰り返し電池として使用することができます。
このとき鉛蓄電池の正極、負極と表現していますが、ここにおける正極、負極には定義された意味(導線に向かって電子が流れ出す電極が負極、導線から電子が流れ込む電極が正極であるということ)はなく単純に場所を示すためだけに用いていることに注意してください。
3. 鉛板、酸化鉛板、電解液の放電時・充電時の変化
3.1 鉛板、酸化鉛板の変化
放電により、負極、正極ともに白色で水に難溶の\(PbSO_4\)が生成し、両極板の表面に付着します。負極では、\(SO_4\)分の質量が増加し、正極では、\(SO_2\)分の質量が増加します。したがって、放電時は両電極の質量は増加します。逆に、充電時には両極面の質量は減少します。
物質量や質量の変化を反応式と絡めて解く問題が多く出題されるので両電極でどの原子分質量が増加するのか間違えないようにしてください・
3.2 電解液の変化
電解液中では、放電により硫酸が消費され水が生成されます。よって、放電することで希硫酸の濃度は減少します。一方で、充電すると希硫酸の濃度は増加します。
4. 計算問題
ここでは、鉛蓄電池に関する計算問題について紹介します。
鉛蓄電池を100秒間放電したところ、1.93Aの電流が流れた。この時の正極、負極ではそれぞれどのくらい質量が変化するか求めよ。ただし、ファラデー定数を\(9.65\times10^4〔C/mol〕\)とし、答えは有効数字3桁とする。
【解答】
まず、この反応で流れた電子\(e^-\)の物質量を求めます。\(A=C/s\)であるので、求める電子\(e^-\)の物質量を\(x〔mol〕\)とおくと次の式が成り立ちます。
\(\begin{align}
\displaystyle x〔mol〕\times 9.65\times10^4〔C/mol〕&=100〔s〕\times1.93〔C/s〕\\
\\
x〔mol〕&=\frac{100〔s〕\times1.93〔C/s〕}{ 9.65\times10^4〔C/mol〕}\\
\\
&≒2.00\times10^{-3}
\end{align}\)
これをもとに正極、負極の質量変化を求めていきましょう。
最初に、正極の質量変化についてです。
正極の放電時の反応式は
\(PbO_2 + 4H^+ + {SO_4}^{2-} + 2e^- →PbSO_4 + 2H_2O\)
となります。
反応式より、正極では\(2〔mol〕\)の電子が流れたとき、\(SO_2\)分の\(64〔g〕\)が増加します。この反応で流れた電子の物質量は\(2.00\times10^{-3}\)であるので、正極で増加した質量を\(y〔g〕\)とすると、
\(\begin{align}
2 : 2.00\times10^{-3}&=64 : y\\
\\
y&=\frac{64\times2.00\times10^{-3}}{2}\\
\\
y&=6.40\times10^{-2}
\end{align}\)
次に、負極について考えましょう。
負極の放電時の反応式は
\(Pb + {SO_4}^{2-} →PbSO_4 + 2e^-\)
となります。
反応式より、負極では\(2〔mol〕\)の電子が流れたとき、\(SO_4\)分の\(96〔g〕\)が増加します。この反応で流れた電子の物質量は\(2.00\times10^{-3}\)であるので、正極で増加した質量を\(z〔g〕\)とすると、
\(\begin{align}
2 : 2.00\times10^{-3}&=96 : z\\
\\
z&=\frac{96\times2.00\times10^{-3}}{2}\\
\\
y&=9.60\times10^{-2}
\end{align}\)
答‥正極:6.40×10-2〔g〕増加する。 負極:9.60×10-2〔g〕増加する。
5. まとめ
最後に、鉛蓄電池についてまとめておこうと思います。
① 鉛\(Pb\)板が酸化され硫酸鉛\(PbSO_4\)になり、電子\(e^-\)を放出する。
② 酸化鉛\(PbO_2\)板が流れてきた電子\(e^-\)を受け取り、還元されて硫酸鉛\(PbSO_4\)になる。
負極:\(Pb + {SO_4}^{2-} →PbSO_4 + 2e^-\)
正極:\(PbO_2 + 4H^+ + {SO_4}^{2-} + 2e^- →PbSO_4 + 2H_2O\)
充電:放電の時とは逆向きに電流を流すこと
充電時の両電極での反応は放電時の逆向きになる。
二次電池:鉛蓄電池のように充電を行い繰り返し使用できる電池
一次電池:ダニエル電池のように一回しか使用できない電池
鉛蓄電池は充電ができるという他の電池にはない特徴があります。放電、充電ともに反応式が自分で書けるようになるまでこの記事を読み込んでください。
また、計算問題もよく出題されるので例題を参考にたくさん練習してしっかりマスターしてください!















私が持っている教材は反応を細かく説明してくれておらず、反応を理論的に理解するのが難しかったです。
手順通りに説明された反応のおかげでとても理解できました。ありがとうございます
充電中二バッテリ−がかなり高温になりますナゼ