東大塾長の山田です。
このページでは「理想気体と実在気体・状態方程式」について解説しています。
計算問題の例やグラフを使って理解しやすいように説明しているので、是非参考にしてください。
1. 気体の状態方程式
1.1 気体定数
気体の圧力を\(P\)、体積を\(V\)、絶対温度を\(T\)とします。また、\({\rm 1mol}\)の気体の体積を\(V_m\)、\({\rm 1mol}\)の気体についての\(k\)を\(R\)とおきます。すると、ボイル・シャルルの法則\(\frac{PV}{T}=k\)は、\({\rm 1mol}\)の気体について、
\[\frac{PV_m}{T}=R‥‥①\]
と表せます。①式に「\({\rm 1mol}\)の気体の体積は、標準状態(\(273 K(0℃)\)、\(1.013\times10^5 Pa(1 atm)\))で\({\rm 22.4L}\)であること」を代入すると、\(R\)の値が求まります。
\[R=\frac{PV_m}{T}=\frac{1.013\times10^5\times22.4}{273}=8.31\times10^3 〔\frac{\rm Pa・L}{\rm K・mol}〕\]
この\({\rm 1mol}\)の気体についての定数\(R\)を、気体定数といいます。
\[R=8.31\times10^3 Pa・L/(K・mol)\]
圧力の単位にatmを用いると、\(R=0.0821 atm・L/(K・mol)\)となります。
1.2 気体の状態方程式
\(V_m\)は\({\rm 1mol}\)の気体の体積ですが、\(n〔mol〕\)の気体の体積を\(V\)とすると、\(V_m=\frac{V}{n}\)となるので、①式から、\(PV=nRT\)が得られます。この式を、気体の状態方程式といいます。\(P\)、\(V\)、\(n\)、\(T\)のうち3つが決まれば、残る1つも決まります。
\[PV=nRT\]
1.3 気体の状態方程式と分子量
ある気体のモル質量を\(M〔g/mol〕\)とおくと、\(w〔g〕\)のこの気体の物質量\(n〔mol〕\)は、\(n=\frac{w}{M}\)ですから、気体の状態方式\(PV=nRT\)から、
\[PV=\frac{w}{M}RT\]
が得られます。この式に、実験で測定した、圧力\(P〔Pa〕\)、体積\(V〔L〕\)、温度\(T〔K〕\)、気体の質量\(w〔g〕\)と気体定数\(R〔Pa・L/(K・mol)〕\)を代入すれば、
\[M=\frac{wRT}{PV}‥‥①\]
より、気体のモル質量\(M〔g/mol〕\)が求められます。すなわち、気体の分子量\(M\)が求められるということになります。
さらに、ある気体の密度を\(d〔g/L〕\)とおくと、\(w〔g〕\)のこの気体の体積が\(V〔L〕\)であることから、\(d=\frac{w}{V}\)となるので、①式より、
\[M=\frac{dRT}{P}\]
が得られます。この式に、実験で測定した、圧力\(P〔Pa〕\)、密度\(d〔g/L〕\)、温度\(T〔k〕\)と気体定数\(R〔Pa・L/(K・mol)〕\)を代入しても、気体の分子量\(M\)を求めることができます。
常温・常圧で液体である物質でも、揮発性の物質であれば、上述の式を利用してその分子量を求めることができます。
\[M=\frac{wRT}{PV} または M=\frac{dRT}{P}\]
2. 状態方程式を使った計算問題
ここでは、いくつか状態方程式を使った計算問題の例を紹介したいと思います。
ただし、気体定数を\(R={\rm 8.3\times10^3〔Pa・L/(K・mol)〕}\)、水素の原子量を1、窒素の原子量を14、酸素の原子量を16とし、1で用いたアルファベットをここでもそのまま用いることとします。また、答えはすべて有効数字2桁で表します。
\(27℃、4.5\times10^4Paにおける1.2molの気体の体積を求めよ。\)
気体の状態方程式は\(PV=nRT\)であるから、式を変形すると、\(V=\frac{nRT}{P}\)となるので値を代入して
\[V=\frac{nRT}{P}=\frac{8.3\times10^3\times300\times1.2}{4.5\times10^4}=66.4\]
これを四捨五入して
答‥\(6.5\times10〔L〕\)
\(57℃、2.0\times10^5Paにおける3.2gの酸素の体積を求めよ。\)
気体の状態方程式は\(PV=nRT\)であり、物質量\(n\)は\(n=\frac{w}{M}\)とできるので、式を変形すると、\(V=\frac{wRT}{PM}\)となるから値を代入して
\[V=\frac{wRT}{PM}=\frac{330\times8.3\times10^3\times3.2}{2.0\times10^5\times32}=1.36‥\]
これを四捨五入して、
答‥\(1.4〔L〕\)
\(27℃、1.5\times10^5Paで体積が2.0Lの窒素の質量を求めよ。\)
気体の状態方程式は\(PV=nRT\)であり、物質量\(n\)は\(n=\frac{w}{M}\)とできるので、式を変形すると、\(w=\frac{PVM}{RT}\)となるから値を代入して
\[w=\frac{PVM}{RT}=\frac{1.5\times10^5\times2.0\times28}{8.3\times10^3\times300}=3.37‥\]
これを四捨五入して、
答‥\(3.4〔g〕\)
\(127℃、4.0\times10^4Paで体積が2.5Lの質量が0.54gの気体の分子量を求めよ。\)また、この気体は何であるか求めよ。
気体の状態方程式は\(PV=nRT\)であり、物質量\(n\)は\(n=\frac{w}{M}\)とできるので、式を変形すると、\(M=\frac{wRT}{PV}\)となるから
\[M=\frac{wRT}{PV}=\frac{0.54\times8.3\times10^3\times400}{4.0\times10^4\times2.5}=17.9‥\]
これを四捨五入すると、気体の分子量は\(18\)となる。また、分子量が\(18\)となるのは水\({\rm H_2O}\)である。
答‥\(18〔g/mol〕、 水{\rm H_2O}\)
\(30℃、3.6\times10^5Paにおける密度が0.29g/Lの気体の分子量を求めよ。\)また、この気体は何であるか求めよ。
気体の状態方程式は\(PV=nRT\)であり、密度\(d\)は\(d=\frac{w}{V}\)とできるので、式を変形すると、\(M=\frac{dRT}{P}\)となるから値を代入して
\[M=\frac{dRT}{P}=\frac{0.29\times8.3\times10^3\times303}{3.6\times10^5}=2.02‥\]
これを四捨五入しすると、気体の分子量は\(2\)である。また、分子量が\(2\)となるのは水素\({\rm H_2}\)である。
答‥\(2〔g/mol〕、 水素{\rm H_2}\)
状態方程式を使った計算問題はこれから先たくさんでてくると思います。しっかり練習して、確実に素早く解けるようにしてください。
3. 理想気体と実在気体
分子自身の体積を0と仮定し、分子間に引力が働かず、気体の状態方程式にして従う気体を理想気体といいます。理想気体は、冷却しても、圧縮しても、凝縮したり凝固したりすることはありません。
一方で、実際に存在する気体のことを実在気体といいます。実在気体は、冷却や圧縮によって液体や固体になります。つまり、気体の状態方程式には厳密には従いません。
これは、分子自身が体積をもっていて、分子間に引力が働くからです。
理想気体と実在気体の比較を表にまとめると次のようになります。
| 実在気体 | 理想気体 | |
| 状態方程式 | 厳密には従わない | 厳密に従う |
| 分子自身の体積 | もつ | 0と仮定する |
| 分子間の引力 | 働く | 働かない |
| 冷却・圧縮下 | 凝縮、または、凝固する | 気体の状態を保つ |
4. 理想気体と実在気体のグラフ
次式で定義される\(Z\)は、実在気体からのずれを示す指標としてよく用いられている値です。
\[\frac{PV}{nRT}=Z (理想気体の場合:Z=1)\]
理想気体の場合には\(Z=1\)となりますが、実在気体の場合には必ずしも\(Z=1\)にはなりません。実在気体について、さまざまな温度\(T\)、圧力\(P\)の下での体積\(V\)を測定し、\(Z\)が1からどれほどずれるかをみることにより、理想気体からのずれの程度を知ることができます。
次のグラフは、\({\rm 1mol(n=1)}\)の気体について、さまざまな温度\(T\)、圧力\(P\)の下での体積\(V\)を調べ、\(Z(=\frac{PV}{RT})\)の値を圧力\(P\)に対してプロットしたものです。
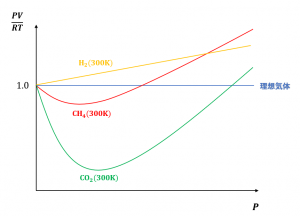
理想気体では、\(Z\)の値は、圧力\(P\)や温度\(T\)の値に関係なく一定(\(Z=1\))ですが、実在気体では、\(Z\)の値は、圧力\(P\)や温度\(T\)の大小によって変化しています。
ちなみに、二酸化炭素\({\rm CO_2}\)のように、圧力が高くなると容易に凝縮して液体になる気体では、単なる圧力の影響以上に体積は小さくなって、理想気体からのずれは一層大きくなります。
次に、このグラフを見ながら、「温度の影響による(実在気体の理想気体からの)ずれ」や「圧力の影響による(実在気体の理想気体からの)ずれ」について考えていきましょう。
【温度の影響にずれ】
温度が低くなると、熱運動のエネルギーが小さくなります。すると、分子間力の影響が相対的に強くなり、\(Z=1\)(理想気体)からずれるようになります。このとき、分子間力の影響は、\(Z\)の値を小さくする方向(\(Z<1\))に働きます。
【圧力の影響によるずれ】
一定温度で\({\rm 1mol}\)の気体の圧力を高くしていくと、体積は小さくなっていきます。そして分子間距離が小さくなってくると、分子間力による影響が大きく出てきます。実在気体では、分子間力があるので理想気体よりも体積の減少量が大きくなります。
その結果、\(\frac{PV}{RT}<1\)となり、グラフは\(Z=1\)(理想気体)の下側にずれます。(ただし、分子量が小さく無極性分子である\({\rm H_2}\)などは分子間力が元々小さく、影響されません。)
さらに、圧力を高く(体積を小さく)していくと、分子の体積の影響が大きく出てきます。つまり、実在気体の体積は理想気体の体積よりも大きくなります。
その結果、
\(\frac{PV}{RT}>1\)となり、グラフは\(Z=1\)(理想気体)の上側にずれます。
このように、低温・高圧では実在気体の挙動は理想気体と比較して大きくずれます。
分子量が大きいほど分子間力が大きいため、\({\rm CH_4(16)}\)に比べて\({\rm CO_2}\)のずれが大きくなります。また、極性をもつ分子も分子間力が大きいため、ずれが大きくなります。
5. 実在気体を理想気体とみなせる条件
3で低温・高圧では実在気体の挙動は理想気体と比較して大きくずれる、と説明しました。これを逆に考えると、実在気体でも高温・低圧であるほど理想気体に近くなると考えることができます。
【高温にする理由】
高温にすると、その分気体の運動エネルギーが大きくなり、相対的に分子間力が無視できるようになります。
【低圧にする理由】
気体分子自体の大きさ(体積)が相対的に小さくなるためです。また、容器の体積が大きくなるのに伴い気体分子間の距離が離れ分子間力が無視できるようにできるからでもあります。
6. まとめ
最後に理想気体と実在気体、状態方程式についてまとめておこうと思います。
- \(PV=nRT\)を、気体の状態方程式という。
- 分子自身の体積を0と仮定し、分子間に引力が働かず、気体の状態方程式にして従う気体を理想気体という。
- 実際に存在する気体のことを実在気体という。
- 実在気体でも高温・低圧であるほど理想気体に近くなる。
理想気体、実在気体に関する考え方や状態方程式は化学の基本となる部分です。理想気体と実在気体についてのグラフは記述問題でよく出題されますし、状態方程式は化学の計算問題でたくさん使います。
何度も読み返してしっかりマスターしてください!















必要な窒素ボンベ15.0Mpa7.0m3の本数の計算式教えてください。
配管気密テストで窒素ガスを使います。
大気圧から規定の圧力まで昇圧し保持します。
テスト圧力2.5Mpa、容積10m3です。
ご指導お願いします。
むっりーーw
よろしくお願いします。