東大塾長の山田です。
このページでは「イオン結合」について解説しています。
間違えることが多い「共有結合」と「イオン結合」が区別できるように解説しているので,是非参考にしてください。
1. イオン結合
原子間の結合において、一方の原子が陽イオン、他方の原子が陰イオンとなり、静電気的引力(クーロン力)によって結びつく結合をイオン結合といいます。
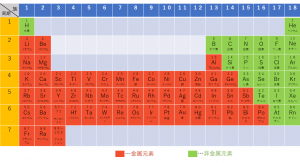
金属元素は陽イオンになりやすく、非金属元素の多くは陰イオンになりやすいことから、イオン結合は金属元素と非金属元素からなります。
(陽イオン、陰イオンそれぞれのなりやすさはイオン化エネルギーと電子親和力に依存しています。イオン化エネルギーと電子親和力については「イオン化エネルギーと電子親和力のまとめ」の記事を参考にしてください。)
ここで次の図を見てください。
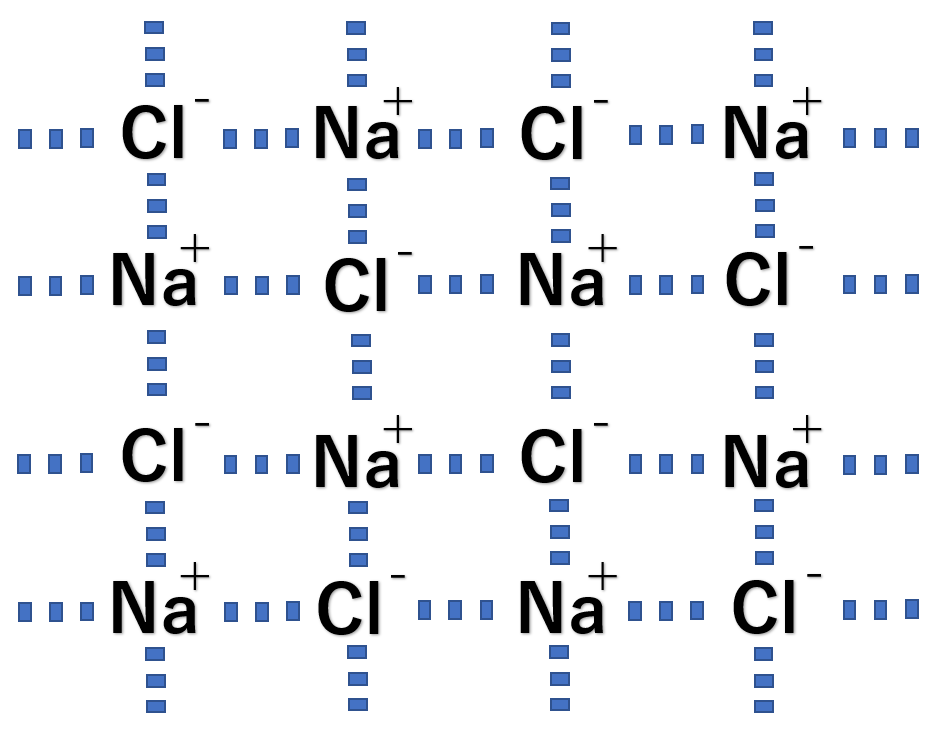
これはイオン結合を表したものです。
この図は共有結合である\({\rm Cl_2}\)や\({\rm CH_4}\)とは異なり、\({\rm NaCl}\)はたくさんのイオンが繋がって作られているのがわかります。
これが共有結合とイオン結合の異なる点です。
共有結合はお互いが持つ電子を出し合って結合を作っているため結合の本数に限度があるのに対し、イオン結合はプラスとマイナスの間に生じるクーロン力によって作られるものであるので「陽イオンと陰イオンがある限り制限なく結合できる」ということになります。
2. イオン結合の例外
1でイオン結合は金属元素と非金属元素の結合であると説明しました。
しかし、これには例外があります。その例塩化アンモニウム\({\rm NH_4Cl}\)です。
塩化アンモニウムを構成する元素である\({\rm N}\)、\({\rm H}\)、\({\rm Cl}\)はすべて非金属元素ですが、塩化アンモニウムは\({\rm {NH_4}^+}\)と\({\rm Cl^-}\)のイオン結合となります。
アンモニウムイオン\({\rm {NH_4}^+}\)は金属ではありませんが、陽イオンとなるので、陰イオンである\({\rm Cl^-}\)とイオン結合をします。
一方で、水素イオンは陽イオンとなりますが、イオン結合をとらず、共有結合となります。
\({\rm HCl}\)の場合は\({\rm Cl^-}\)が\({\rm H^+}\)に電子を1個与え、共有結合します。
イオン結合性物質は基本的に塩(酸と塩基が中和して、塩基の陽イオンと酸の陰イオンとが結合した化合物のこと)で、酸と塩基の中和によって作られます。例えば、
\[{\rm HCl} + {\rm NaOH}→{\rm H_2O} + {\rm NaCl}\]
について、\({\rm NaCl}\)が塩、イオン結合性物質となります。
同様に、\({\rm NH_4Cl}\)は、
\( {\rm HCl} + {\rm NH_3}→{\rm NH_4Cl} \)
の中和反応で作ることができます。
しかし、\({\rm HCl}\)は酸と塩基の中和で作ることはできません。
これより、イオン結合は塩と覚えておくのがいいと思います。
3. 組成式
まず、組成式と分子式について説明したいと思います。
分子が存在する物質に限って用いられ、その分子に含まれている原子をその数とともに示したものを分子式といいます。
また、その物質を構成している原子を最も簡単な整数比であらわしたものを組成式といいます。
グルコース(\({\rm C_6H_{12}O_6}\))を例に見てみましょう。
\({\rm C_6H_{12}O_6}\)は分子式で\({\rm CH_2O}\)は組成式となります。
分子は分子の実態を表すためのもので、組成式は化学式で表せるものにはすべて使えます。
ここで、イオン結合について考えてみましょう。
イオン結合によって作られた物質は、陽イオンと陰イオンの数を最も簡単な整数比にした組成式を使って表します。
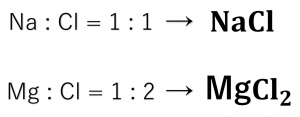
塩化ナトリウムは、Na1個に対して1個のCl、つまりNaとClが「1:1」の割合で結合しているので\({\rm NaCl}\)、塩化マグネシウムはMg1個に対して2個のCl、つまりMgとClが「1:2」の割合で結合しているので\({\rm MgCl_2}\)となります。
共有結合で使われる分子式と区別できるようにしておきましょう。
分子式である\({\rm HCl}\)は「H1つとCl1つ」がくっついていることを、組成式である\({\rm NaCl}\)は「Na+とCl+がたくさんくっついているけれどその比が1:1」となることを表しています。
4. まとめ
最後にイオン結合についてまとめておこうと思います。
- 原子間の結合において、一方の原子が陽イオン、他方の原子が陰イオンとなり、静電気的引力(クーロン力)によって結びつく結合をイオン結合という。
- イオン結合は金属元素と非金属元素からなる。
- イオン結合はプラスとマイナスの間に生じるクーロン力によって作られるものであるので「陽イオンと陰イオンがある限り制限なく結合できる」ということになる。
- 分子が存在する物質に限って用いられ、その分子に含まれている原子をその数とともに示したものを分子式という。
- その物質を構成している原子を最も簡単な整数比であらわしたものを組成式という。
イオン結合と共有結合の違いが分からないといったことがよくありますが、共有結合、イオン結合それぞれについてしっかり理解すれば間違えることはありません。(共有結合については、「共有結合とは(例・結晶・イオン結合との違い・半径)」の記事を参照してください。)
しっかりマスターしてください!
イオン結合の結晶については「イオン結晶・共有結合の結晶・分子結晶」の記事で解説しているのでそちらを参照してください。















コメントを残す