東大塾長の山田です。
このページでは「分圧の法則」について解説しています。
計算問題で間違えることがないように、計算問題の例題を使いながら詳しく解説しています。
是非参考にしてください。
1. 混合気体の体積と物質量
一定圧力 \( P \)、一定温度 \( T \) のもとで、体積 \( V_A \)、物質量 \( n_A \) の気体Aと,体積 \( V_B \)、物質量 \( n_B \) の気体Bを混合すると、混合気体の体積 \( V \) は各成分気体A、Bの体積の和になり(\( V = V_A + V_B \))、混合気体の物質量 \( n \) も各成分気体A、Bの物質量の和になります。(\( n = n_A + n_B \))
2. 分圧、全圧
一定温度 \( T \) のもとで、体積 \( V \) の容器に気体Aと気体Bを入れて混合したとき、「混合気体全体の圧力のことを全圧」、「気体Aや気体Bがそれぞれ単独で混合気体の全体積 \( V \) を占めたときに示す圧力のことを,それぞれの分圧」といいます。
【ドルトンの分圧の法則の導入】
ドルトンの分圧の法則が成立することを、状態方程式から考えてみましょう。次の(1)~(3)の状態があったとします。
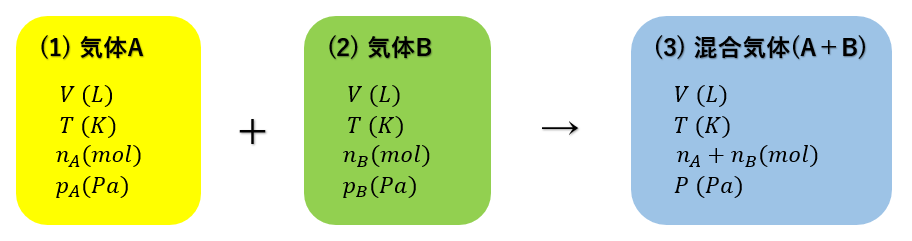
(1) 温度 \( T〔K〕 \) において、容積 \( V〔L〕 \) の容器に、\( n_A〔mol〕 \) の気体Aをいれたとき、\( p_A〔Pa〕 \) の圧力を示した。
(2) 同一温度 \( T〔K〕 \) において、同一容積 \( V〔L〕 \) の容器に、\( n_B〔mol〕 \) の気体Bをいれたとき、\( p_B〔Pa〕 \) の圧力を示した。
(3) 同一温度 \( T〔K〕 \) において、同一容積 \( V〔L〕 \) の容器に、\( n_A〔mol〕 \) の気体Aと \( n_B〔mol〕 \) の気体Bをいれたとき、\( P〔Pa〕 \) の圧力を示した。
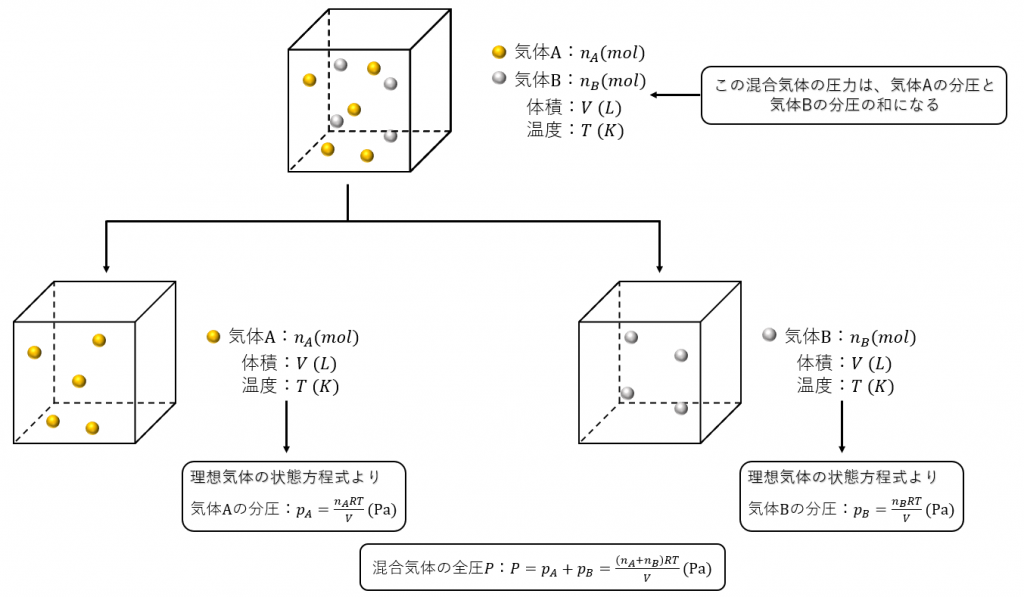
とすると、(1)~(3)について次の状態方程式が成り立ちます。
\( \displaystyle p_AV=n_ART‥‥① \)
\( \displaystyle p_BV=n_BRT ‥‥ ② \)
\( \displaystyle PV = (n_A+n_B) RT ‥‥ ③ \)
①式と②式の辺々を足し合わせると、
\( \displaystyle (p_A+p_B)V=(n_A+n_B)RT ‥‥ ④ \)
となり、④式と③式を比較すると
\( \displaystyle P = p_A+p_B \)
\( \displaystyle (T,V=一定のもとでは、P=p_A+p_B) \)
となることがわかります。
3. モル分率
混合気体の \( mol \) 数に対する特定の気体の \( mol \) 数の割合のことをモル分率といいます。
\( \displaystyle 各成分気体の分圧 = 全圧 \times \frac{各成分の物質量}{全物質量} \)
であるが、\( \displaystyle \frac{各成分の物質量}{全物質量} \) の部分のことをモル分率という。
分圧、全圧、モル分率の関係を、状態方程式から考えてみましょう。2の①式~③式
\( \displaystyle p_AV = n_ART ‥‥ ① \)
\( \displaystyle p_BV = n_BRT ‥‥ ② \)
\( \displaystyle PV = (n_A+n_B)RT ‥‥ ③ \)
を整理すると、
\( \displaystyle \frac{RT}{V} = \frac{p_A}{n_A} = \frac{p_B}{n_B} = \frac{P}{n_A+n_B} ‥‥ ⑤ \)
となるから、⑤式より、
\( \displaystyle p_A=P\times\frac{n_A}{n_A+n_B} \)
つまり \( \displaystyle Aの分圧 = 全圧×Aのモル分率 \)
\( \displaystyle p_B = P \times \frac{n_B}{n_A+n_B} \)
つまり \( Bの分圧=全圧×Bのモル分率 \)
となることがわかります。
ここで、体積 \( V \) と温度 \( T \) が一定の時、
\( \displaystyle PV = nRT \)
\( \displaystyle P = n \times \frac{RT}{V} \)
としたとき、\( \frac{RT}{V} \) は一定であるから、これを定数 \( A \) とおくと、
\( \displaystyle P = A \times n \)
となるので、\( P \) が2倍になれば \( n \) も2倍に、\( P \) が \( \displaystyle \frac{1}{2} \) になれば \( n \) も \( \displaystyle \frac{1}{2} \) になります。
すなわち、「圧力比=物質量比」が成り立ちます。
また、温度 \( T \) と圧力 \( P \) が一定の時、
上と同様に考えれば「体積比=物質量比」が成り立ちます。
4. 混合気体の平均分子量
\( n_A〔mol〕 \) の気体A(分子量 \( M_A \))と\( n_B〔mol〕 \) の気体B(分子量 \( M_B \))からなる混合気体の平均分子量 \( \overline{M} \) は、次式で求めることができます。
\( \displaystyle \overline{M} = M_A \times \frac{n_A}{n_A+n_B} + M_B \times \frac{n_B}{n_A+n_B} \)
【例】
空気を、物質量比で「酸素:窒素=1:4」の混合気体とみなすと、空気の平均分子量は、次式で求められます。
\( \begin{align}
\displaystyle & 空気の平均分子量 \\
\\
& = 32.0 \times \frac{1}{1+4} + 28.0 \times \frac{4}{1+4} \\
\\
& = 28.8
\end{align} \)
\( \displaystyle \overline{M} = M_A \times \frac{n_A}{n_A+n_B} + M_B \times \frac{n_B}{n_A+n_B} \)
平均分子量は、みかけの分子量と呼ばれることもあります。
5. 計算問題
ここでは、分圧に関する計算問題の例を紹介していきます。
以下では、答えは有効数字2桁で求めるとします。また、気体定数 \( R \) を \( R = 8.3 \times 10^3 Pa・L/(K・mol) \) とします。
5.1 問題1
 コックが閉じた状態で、4.5Lの容器Aに \( 3.0 \times 10^5 Pa \) の窒素、1.5Lの容器Bに \( 1.2 \times 10^5 Pa \) の酸素が入っている。温度を一定に保ってコックを開いたとき、窒素と酸素の分圧および全圧を求めよ。
コックが閉じた状態で、4.5Lの容器Aに \( 3.0 \times 10^5 Pa \) の窒素、1.5Lの容器Bに \( 1.2 \times 10^5 Pa \) の酸素が入っている。温度を一定に保ってコックを開いたとき、窒素と酸素の分圧および全圧を求めよ。
窒素と酸素の分圧を \( p_{窒素} \),\( p_{酸素} \) とすると、温度は一定であるからボイルの法則より
\( \displaystyle 3.0\times10^5〔Pa〕\times 4.5〔L〕 \\
= p_{窒素}〔Pa〕\times (4.5+1.5)〔L〕 \)
\( \displaystyle 1.2 \times 10^5〔Pa〕 \times 1.5 〔L〕 \\
= p_{酸素} 〔Pa〕 \times (4.5 + 1.5) 〔L〕 \)
これより、それぞれの分圧は
\( p_{窒素} = 2.3 \times 10^5〔Pa〕 \),\( p_{酸素} = 3.0 \times 10^4 〔Pa〕 \)
また、全圧 \( P \) は \( P = p_{窒素} + p_{酸素} \) であるから
\( \begin{align}
\displaystyle P & = 2.25 \times 10^5 〔Pa〕 + 0.3 \times 10^5 〔Pa〕 \\
\\
& = 2.55 \times 10^5 〔Pa〕
\end{align} \)
となる。
よって、
\(p_{窒素}\)=2.3×105〔Pa〕,\(p_{酸素}\)=3.0×104〔Pa〕,\(P\)=2.6×105〔Pa〕‥‥答
5.2 問題2
次の(1)と(2)を求めよ。
(1) 酸素1.2molと窒素4.8molを体積16.6Lの容器に入れ、温度を47℃に保った。混合気体の全圧と各気体の分圧を求めよ。
(2) 空気を酸素と窒素の体積比が1:4の混合気体であるとして、\( 1.5 \times 10^5 Pa \) の空気中の酸素と窒素の全圧を求めよ。
(1) 全圧を \( P \) とすると、容器内に入っている気体の全物質量は \( 6.0 mol \) であるから、気体の状態方程式より、
\( \displaystyle P \times 16.6 = 6.0 \times 8.3 \times 10^3 \times 320 \)
よって、\( P = 9.6 \times 10^5 〔Pa〕 \)
また、酸素の分圧を \( p_{酸素} \)、窒素の分圧を \( p_{窒素} \) とすると、\( p_{酸素} = P \times \frac{n_{酸素}}{n_{酸素}+n_{窒素}} \)、\( p_{窒素} = P \times \frac{n_{窒素}}{n_{酸素} + n_{窒素}} \) より、
\( \begin{align}
\displaystyle p_{酸素} & = 9.6 \times 10^5 〔Pa〕 \times \frac{1.2〔mol〕}{1.2〔mol〕+4.8〔mol〕} \\
\\
& = 1.92 \times 10^5
\end{align} \)
これより、分圧の法則から
\( \begin{align}
\displaystyle p_{窒素} & = 9.6 \times 10^5 〔Pa〕 – 1.92 \times 10^5 〔Pa〕 \\
\\
& = 7.68 \times 10^5 〔Pa〕
\end{align} \)
よって、
\(P\)=9.6×105〔Pa〕,\(p_{酸素}\)=1.9×105〔Pa〕,\(p_{窒素}\)=7.7×105〔Pa〕‥‥答
(2) 同温・同圧下では体積比=物質量比となるので
\( \begin{align}
\displaystyle p_{酸素} & = 1.5 \times 10^5 〔Pa〕 \times \frac{1}{1+4} \\
\\
& = 3.0 \times 10^4 〔Pa〕
\end{align} \)
分圧の法則より
\( \begin{align}
\displaystyle p_{窒素} & = 1.5 \times 10^5 〔Pa〕 – 0.3 \times 10^5 〔Pa〕 \\
\\
& = 1.2 \times 10^5 〔Pa〕
\end{align} \)
\(p_{酸素}\)=3.0×104〔Pa〕,\(p_{窒素}\)=1.2×105〔Pa〕‥‥答
5.3 問題3
一定温度下で \( 1.0 \times 10^5 Pa \) の酸素6.0Lと、\( 2.5 \times 10^5 Pa \) の窒素3.0Lを5.0Lの容器に入れたときの酸素と窒素それぞれの分圧と混合気体の全圧を求めよ。
酸素と窒素を5.0Lの容器に入れたときの酸素と窒素それぞれの分圧を \( p_{酸素} \)、\( p_{窒素} \) とする。
温度が一定であるのでボイルの法則より
\( \displaystyle 1.0 \times 10^5 〔Pa〕 \times 6.0 〔L〕 \\
= p_{酸素}〔Pa〕 \times 5.0〔L〕 \)
\( \displaystyle 2.5 \times 10^5 〔Pa〕 \times 3.0 〔L〕 \\
= p_{窒素} 〔Pa〕 \times 5.0 〔L〕 \)
これより、\( p_{酸素} = 1.2 \times 10^5 〔Pa〕 \),\( p_{窒素} = 1.5 \times 10^5 〔Pa〕 \)
また、混合気体の全圧 \( P \) は
\( \begin{align}
\displaystyle P & = p_{酸素} + p_{窒素} \\
\\
& = 1.2\times10^5〔Pa〕+1.5\times10^5〔Pa〕 \\
\\
& = 2.7\times10^5〔Pa〕
\end{align} \)
\(P\)=2.7×105〔Pa〕,\(p_{酸素}\)=1.2×105〔Pa〕,\(p_{窒素}\)=1.5×105〔Pa〕‥‥答
6. まとめ
最後に分圧についてまとめます。
- 一定温度 \( T \) のもとで、体積 \( V \) の容器に気体Aと気体Bを入れて混合したとき、混合気体全体の圧力のことを全圧という。気体Aや気体Bがそれぞれ単独で混合気体の全体積 \( V \) を占めたときに示す圧力のことを、それぞれの分圧という。
-
一定体積 \( V \)、一定温度 \( T \) のもとで、圧力 \( p_A \) の気体Aと圧力 \( p_B \) の気体Bを混合すると、混合気体の全圧 \( P \) は各成分気体A、Bの分圧 \( p_A、p_B \) の和になる(\( P = p_A + p_B \))。これをドルトンの分圧の法則という。
- 混合気体の \( mol \) 数に対する特定の気体の \( mol \) 数の割合のことをモル分率という。
-
\( n_A 〔mol〕 \) の気体A(分子量 \( M_A \))と \( n_B〔mol〕 \) の気体B(分子量 \( M_B \))からなる混合気体の平均分子量 \( \displaystyle \overline{M} \) は、\( \displaystyle \color{red}{ \overline{M} = M_A \times \frac{n_A}{n_A+n_B} + M_B \times \frac{n_B}{n_A+n_B} } \) となる。
分圧に関する問題は応用的な問題も多々出てきますが、このページで述べた基本をしっかり理解していればちゃんと対応できます。
この記事を読んでしっかりマスターしましょう!















一定体積 \( V \)、一定温度 \( T \) のもとで、圧力 \( p_A \) の気体Aと圧力 \( p_B \) の気体Bを混合すると、混合気体の全圧 \( P \) は各成分気体A、Bの分圧 \( p_A、p_B \) の和になる。(\( P = p_A + p_B \))
これをドルトンの分圧の法則という。