東大塾長の山田です。
このページでは、「原子構造と電子配置・価電子」について解説しています。
- 「原子半径の大小の規則性」
- 「イオン半径の大小の規則性」
といった疑問がすべて解決できるように、すべて解説しています。
ぜひ、参考にしてください!
1. 原子半径
原子半径とは、そのまま原子であるときの半径のことを言います。
原子半径は、周期表における同族、同一周期で大小に規則性があります。
ここでは、この規則性について説明していこうと思います。
ただし、希ガスについては原子の大きさの測定方法が異なり、この法則は当てはまらないので注意してください。
1.1 同族元素の大小の規則性
同族元素の原子は、周期表で下にいく(原子番号が大きくなる)ほど原子半径が大きくなります。
同族元素では、周期表で下に行くにつれて最外殻がK殻、L殻、M殻‥‥というように変化していきます。
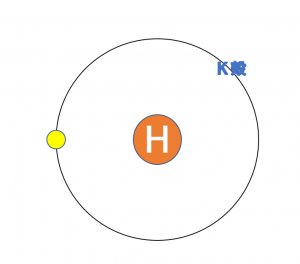
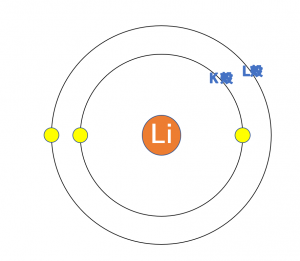
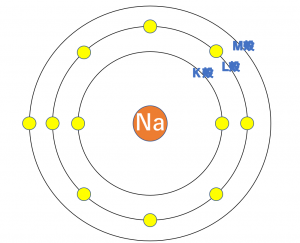
上の図は、1族の\({\rm H}\)、\({\rm Li}\)、\({\rm Na}\)の電子配置です。
原子番号は、\({\rm H}\)<\({\rm Li}\)<\({\rm Na}\)となります。
また、原子半径の大きさは、\({\rm H}\)<\({\rm Li}\)<\({\rm Na}\)となります。
このように、最外殻が増えていく(原子番号が大きくなる)ことで原子半径が大きくなっていくことは上の図から明らかだと思います。
1.2 同一周期の元素の原子半径の大小の規則性
同一周期の元素は、1.1のように考えると最外殻が同じであるので原子半径も同じになるのではないかと思う人もいるのではないでしょうか。
しかし、実際には同一周期の元素の原子は、周期表の右に行く(原子番号が大きくなる)ほど原子半径は小さくなります。
この理由は次のように考えてください。
原子番号が大きくなるにつれて、原子核内の陽子の数も増えていきます。
陽子は正電荷を持っているので原子核の正電荷も原子番号の増加とともに増えていきます。
電子は負電荷を帯びているので、原子核の正電荷との間に引力が生じます。
この引力とはクーロン力と呼ばれます。
ここで働くクーロン力は\(\rm k\)を比例定数、\(\rm r\)を原子半径、\(\rm q_1\)を陽子の総電荷、\(\rm q_2\)を電子の総電荷として\( k\)\(\frac{q_1q_2}{r^2}\)と表すことができます。(詳しくは物理で勉強します。)
この式からわかるように、原子番号が大きくなると原子核の正電荷と電子が増加するので、原子核と電子との間に働くクーロン力が大きくなり原子半径は小さくなります。
2. イオン半径
イオン半径とは、そのままイオンであるときの半径のことを言います。
イオン半径に関しては、同族または同じ電子配置のイオンにおける違いについて説明していきます。
また、ここでも希ガスについては考えません。
希ガスは原子の状態で安定な電子配置を取るため、イオンとなりません。
よって、イオン半径と原子半径は全く違うものでありこの2つは比較できません。
これより、イオン半径でも希ガスは考えなくてOKです。
2.1 同族元素のイオン半径の大小の規則性
同族元素のイオンのイオン半径は、周期表の下にいく(原子番号が大きくなる)ほど大きくなります。
これは、原子半径と同じように考えることができます。
イオンの最外殻も原子と同じように、K殻、L殻、M殻‥‥というように変化します。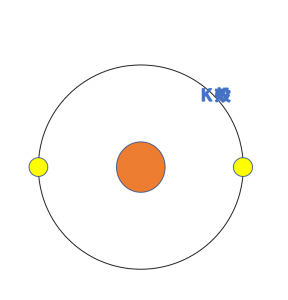 \({\rm Li^+}\)
\({\rm Li^+}\)
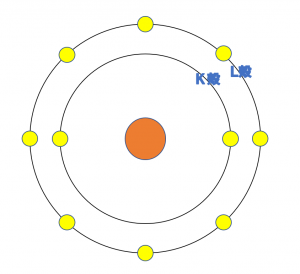 \({\rm Na^+}\)
\({\rm Na^+}\)
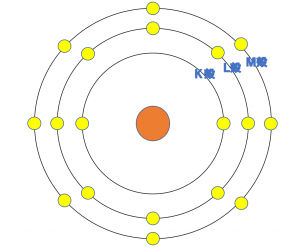
\({\rm K^+}\)
上の図は1族のイオンである\({\rm Li^+}\)、\({\rm Na^+}\)、\({\rm K^+}\)の電子配置です。
原子番号は、\({\rm Li^+}\)<\({\rm Na^+}\)<\({\rm K^+}\)となります。
また、イオン半径の大きさは、\({\rm Li^+}\)<\({\rm Na^+}\)<\({\rm K^+}\)となります。
このように、最外殻が増えていく(原子番号が大きくなる)ことでイオン半径が大きくなっていきます。
2.2 同じ電子配置をとるイオンのイオン半径の大小の規則性
同じ電子配置をとるイオンのイオン半径は、原子番号が大きくなるにつれて小さくなります。
これは、\({\rm O^{2-}}\)、\({\rm F^-}\)、\({\rm Na^+}\)、\({\rm Mg^{2+}}\)、\({\rm Al^{3+}}\)を例に考えていこうと思います。
この5つのイオンはすべて下の電子配置(ネオンの電子配置)を取ります。

原子番号が大きくなると原子核内の正電荷が増加します。
これにより、原子番号が大きくなると電子がより内側に引き付けられるためイオン半径は小さくなり、\({\rm O^{2-}}\)>\({\rm F^-}\)>\({\rm Na^+}\)>\({\rm Mg^{2+}}\)>\({\rm Al^{3+}}\)となります。
3. 原子半径とイオン半径のまとめ
最後に、原子半径とイオン半径についてまとめておこうと思います。
- 同族元素の原子は、周期表で下にいく(原子番号が大きくなる)ほど原子半径が大きくなる。
- 同一周期の元素の原子は、周期表の右に行く(原子番号が大きくなる)ほど原子半径が小さくなる。
- 原子半径について、希ガスは原子の大きさの測定方法が異なり、上の法則は当てはまらない。
- 同族元素のイオンのイオン半径は、周期表の下にいく(原子番号が大きくなる)ほど大きくなる。
- 同じ電子配置をとるイオンのイオン半径は、原子番号が大きくなるにつれて小さくなる。
- 希ガスは原子の状態で安定な電子配置を取るため、イオンとなることはない。イオン半径と原子半径は全く違うものでありこの2つは比較できない。よって、希ガスのイオン半径は考えなくていい。
以上が、原子半径とイオン半径についてのまとめです。
原子半径とイオン半径に関する計算問題が出題されることがありますが、これはそれぞれの結晶についての記事で触れたいと思います。
この内容はすごく間違えやすいところですが、仕組みを理解すれば絶対にできると思います。
しっかりマスターしてください!















2.1と2.2の違いがよくわからなくて、例えば2.2で原子番号が大きくなって中心に引かれることと、2.1の、同族だが原子番号は下に行くほど大きくなっているのにち