東大塾長の山田です。
ここでは、電気陰性度について解説しています。
「電気陰性度と極性」、「電気陰性度の定義」や「覚えておくべき電気陰性度の大小」などこの記事で電気陰性度について完璧に理解できるようになっています。
是非参考にしてください。
1. 電気陰性度
異なる2つの原子が結合するとき、お互いが電子を1個ずつ出し合い共有電子対を形成します。
このとき、原子が共有電子対を自分の方に引っ張る強さのことを電気陰性度といいます。
電気陰性度が高い原子がより強く共有電子対を自分側に引き寄せます。下の図を見てください。
 電気陰性度の大小がA>Bとなるとき、共有電子対は電気陰性度の大きいAの方に引き寄せられます。
電気陰性度の大小がA>Bとなるとき、共有電子対は電気陰性度の大きいAの方に引き寄せられます。
2. 電気陰性度と極性
2.1 電気陰性度と極性の関係
上で説明したように異なる種類の原子が共有結合すると、共有電子対は電気陰性度は大きい原子の方へ偏ります。(共有結合に関しては「共有結合とは(例・結晶・イオン結合との違い・半径)」の記事で解説しているので参考にしてください。)
ここでは、塩化水素(\({\rm HCl}\))を例に考えていきます。
 下でも説明しますが、電気陰性度の大小は\({\rm H}\)<\({\rm Cl}\)となります。このため、共有電子対は電気陰性度のより大きい\({\rm Cl}\)原子の方へと引きつけられます。
下でも説明しますが、電気陰性度の大小は\({\rm H}\)<\({\rm Cl}\)となります。このため、共有電子対は電気陰性度のより大きい\({\rm Cl}\)原子の方へと引きつけられます。
その結果\({\rm Cl}\)原子は負(\({\delta-}\))に、\({\rm H}\)原子は正(\({\delta+}\))に帯電します。このように、原子間の電気陰性度の差によって生じる電荷の偏りを極性といい、極性を持つ分子を極性分子といいます。
一方、水素原子(\({\rm H_2}\))のように同じ種類の原子同士が結合すると、電気陰性度に差がないため共有電子対は2つの(\({\rm H}\))原子のちょうど真ん中に存在します。
そのため極性は生じません。このように極性を持たない分子を無極性分子といいます。
このように極性は電気陰性度が原因で生じるのです。
2.2 無極性分子
上で無極性分子について触れましたが、異なる種類の原子で構成された化合物にも無極性分子になるものが存在します。
ここでは、無極性分子について詳しく解説していこうと思います。
単体
\({\rm H_2}\)や\({\rm Cl_2}\)などの単体の分子は、原子間に電気陰性度の差がないので、結合に極性がなく無極性分子です。
多原子分子の化合物
三原子以上の分子では、極性分子か無極性分子かは分子の形に依存します。
結合に極性があっても、分子全体としてたがいに打ち消しあうような対称構造の分子の形の場合は、無極性分子となります。
ここで分子の形を考えるにあたり規則があるので紹介したいと思います。
まず、分子の形を考えるにあたり電子式を考え、化合物の中心となる元素(\({\rm CH_4}\)であれば\({\rm C}\)、\({\rm NH_3}\)であれば\({\rm N}\))の共有電子対、非共有電子対の合計の電子対の数を調べます。
①電子対が4つであった場合
4つの電子対はマイナスの性質をもった電子なので、クーロン力により反発し、空間的に最も遠ざかる位置に配置されます。4つの電子対すべてを最大限に遠ざけるとそれぞれの電子対が正四面体の頂点方向に配置されます。
分子の形を考えるときは、共有結合対をもった原子の位置を考慮します。
②電子対が3つであった場合
3つの電子対はマイナスの性質をもった電子なので、クーロン力により反発し、空間的に最も遠ざかる位置に配置されます。3つの電子対すべてを最大限に遠ざけるとそれぞれの電子対が正三角形の頂点方向に配置されます。
分子の形を考えるときは、共有結合対をもった原子の位置を考慮します。
③非共有電子対がなく、共有電子対が2つであった場合
このような分子の代表例として\({\rm CO_2}\)が考えられます。これは、\({\rm CO_2}\)のところで詳しく解説します。
この規則に従って実際に分子の形を考え、極性分子となるか無極性分子となるか考えてみましょう。(以下、電子式においてオレンジ色の丸は非共有電子対の電子、緑色の丸は共有電子対の電子を表します。)
①\({\rm H_2O}\)分子の場合
O-Hの結合は、電気陰性度がO原子の方が大きいため、結合の極性があります。ここで、電子式を見てみましょう。

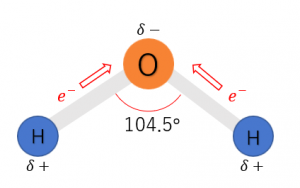
上で述べた規則に基づきO原子に着目すると、共有電子対が2つ非共有電子対が2つあるのがわかります。したがって、4つの電子対は正四面体の頂点方向に配置されます。この結果、\({\rm H_2O}\)は下図のようなH-O-Hの結合角が104.5°の折れ線形をとり、O-Hの極性は打ち消されることがないので、極性分子となります。
②\({\rm NH_3}\)分子の場合
N-Hの結合は、電気陰性度がN原子の方が大きいため、結合の極性があります。ここで、電子式を見てみましょう。
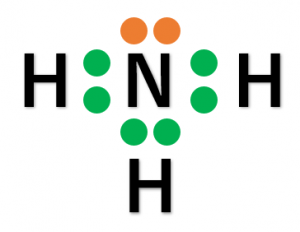
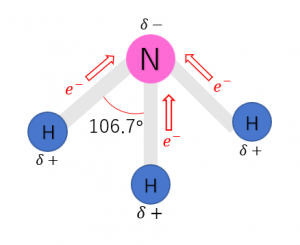
N原子に着目すると、共有電子対が3つ非共有電子対が1つあるのがわかります。したがって、4つの電子対は正四面体の頂点方向に配置されます。この結果、\({\rm NH_3}\)は下図のようなH-N-Hの結合角が106.7°の三角錐形をとり、極性は打ち消されることがないので、極性分子となります。
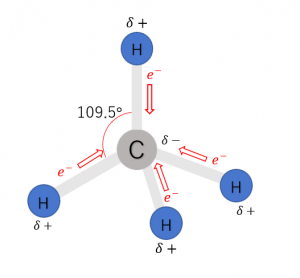
③\({\rm CH_4}\)分子の場合
C-Hの結合は、電気陰性度がC原子の方が大きく、結合に極性があります。ここで、電子式を見てみましょう。
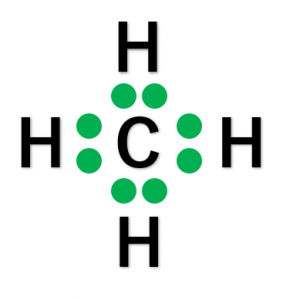
C原子に着目すると、共有電子対が4つあるのがわかります。したがって、4つの電子対は正四面体の頂点方向に配置されます。この結果、C-Hの結合は下図のようなCを中心とする正四面体形をとり、極性が打ち消されるため分子全体では電荷の偏りがなく、無極性分子となります。\({\rm CH_4}\)のHとClが置き換わった\({\rm CCl_4}\)、Cの同族のSiからなる\({\rm SiH_4}\)も正四面体形で無極性分子となります。
④\({\rm CO_2}\)分子の場合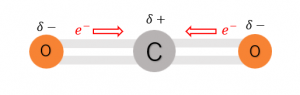
C=Oの結合は、電気陰性度がO原子の方が大きいため、結合の極性があります。ここで、電子式を見てみましょう。

\({\rm CO_2}\)はC原子が二重結合を2つ持ちます。このとき、2つの二重結合はマイナスの性質をもった電子なので、クーロン力により反発し、空間的に最も遠ざかる位置に配置されます。2つの二重結合を最大限に遠ざけるとCを中心に対称となる位置にOが配置されます。この結果、C=Oの結合は下図のようなC原子の両側にO原子が結合する直線形をとり、極性が打ち消しあうため分子全体としては電荷の偏りがなく、無極性分子となります。
3. 電気陰性度とイオン化エネルギー、電子親和力の関係
ここでは、電気陰性度とイオン化エネルギー、電子親和力の関係について解説します。(イオン化エネルギーと電子親和力については「イオン化エネルギーと電子親和力まとめ」で詳しく解説しているのでそちらを参考にしてください。)
3.1 マリケンの定義
電気陰性度・第一イオン化エネルギー・電子親和力の関係を表したものにマリケンの定義と呼ばれる式があります。
\( \displaystyle 電気陰性度=\frac{イオン化エネルギー+電子親和力}{2} \)
この式を見ると電気陰性度は第一イオン化エネルギーと電子親和力の和に比例しており第一イオン化エネルギーと電子親和力が大きくなればなるほど電気陰性度は大きくなることがわかります。
3.2 ポーリングの定義
まず、\({\rm E}\)を原子同士の結合エネルギとして、原子Aと原子Bの結合エネルギーの実測値を、\({\rm E(AB)}\)とすると、純粋な共有結合と仮定した場合の結合エネルギーとの差、\({\Delta(AB)}\)が定義できます。
\( \displaystyle \Delta(AB)=E(AB)-\frac{1}{2}{(E(AA)+E(BB))} \)
この\({\Delta(AB)}\)に関して、
\( \displaystyle \Delta(AB)=K(x^A-x^B)^2 \)
を満たすように決めた\({\rm x^A}\)が原子Aに関してのポーリングの定義による電気陰性度となります。(Kは適当な係数である)
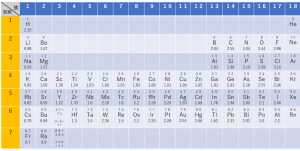
下の図はポーリングの定義によって求められたそれぞれの元素の電気陰性度です。

3.3 エネルギー図
ここでは、エネルギー図を使った電気陰性度の考え方を紹介します。
電気陰性度は、共有電子対を引っ張る強さであり、第一イオン化エネルギーと電子親和力の両方を考慮したものでした。
したがって、エネルギー図で考えると下の図のようになります。
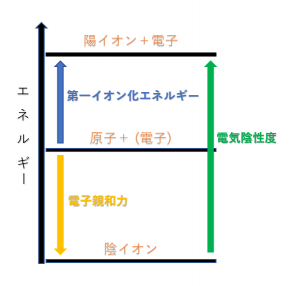 これはあくまでイメージで単純に電気陰性度が第一イオン化エネルギーと電子親和力の和になるというわけではありません(電気陰性度は第一イオン化エネルギーと電子親和力の和に比例するのである)が、このように把握しておくと覚えやすく忘れにくいので参考にしてみてください。
これはあくまでイメージで単純に電気陰性度が第一イオン化エネルギーと電子親和力の和になるというわけではありません(電気陰性度は第一イオン化エネルギーと電子親和力の和に比例するのである)が、このように把握しておくと覚えやすく忘れにくいので参考にしてみてください。
4. 電気陰性度の周期表における大小
ここでは、電気陰性度の周期表における大小を説明します。
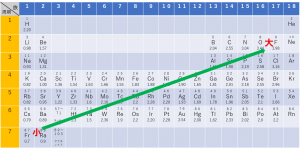
電気陰性度は同周期では右側に、同族では上側にいくにしたがって大きくなります。(多少例外がありますが全体的な傾向としてこれで覚えておけば大丈夫です)
これは、第一イオン化エネルギーと電子親和力が右上にいくにつれて大きくなるからです。(これはマリケンの定義の考え方に基づいています。)(イオン化エネルギーと電子親和力の周期表における大小については「イオン化エネルギーと電子親和力まとめ」の記事を参照してください。)
\({\rm F}\)(フッ素)が最大の値をとります。
しかし、ここで注意してほしいことが2つあります。
注意1
希ガスの電気陰性度は考慮しないということに注意してください。
希ガスは最外殻が満たされているため電子を外から取り込もうとはしません。
そのため、電子を引きつける強さである電気陰性度は考える必要がないのです。
注意2
水素の電気陰性度だけ「周期表の右上にいくにしたがって大きくなる」というルールに従っていないという点にも注意してください。
水素は電子を1つしか持っていないので、それを出してしまうと電子が1つもない原子核のみの状態になってしまいます。
原子核単体だと非常に不安定なので水素はあまり電子を出したがりません。このため、その1つの電子を奪われないように電気陰性度が非常に高くなっています。
4.1 電気陰性度のグラフ
電気陰性度に関するグラフとして次のようなものが出題されることが多いです。
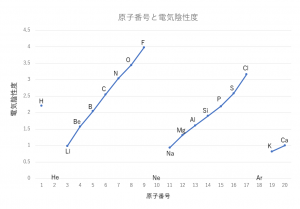 これは上で説明した周期表での電気陰性度の大小を理解していれば当たり前だと思います。
これは上で説明した周期表での電気陰性度の大小を理解していれば当たり前だと思います。
入試で「電気陰性度の傾向を表すグラフとして適切なものはどれか」というように出題されることがあるので覚えておいてください。
4.2 覚えておくべき電気陰性度の大小
上では周期表における電気陰性度の大小の規則性について説明しました。
その中には電気陰性度の大小について、特に覚えていてほしい元素が存在します。ここでは、このことについて解説したいと思います。
覚えてほしいのは次の関係です。
\[{\rm F}>{\rm O}>{\rm N}={\rm Cl}>{\rm C}>{\rm H}\]
語呂合わせはF>O>N(フォン)=Cl>C>H(狂っちゃう)
で覚えてください。
この関係を覚えておくと問題を解くときに役に立つことが多々あるので確実に覚えてください!
特に\({\rm F}\)(フッ素)、\({\rm O}\)(酸素)、\({\rm N}\)(窒素)の電気陰性度が高いことと、\({\rm H}\)(水素)の電気陰性度が低いことは水素結合の部分で重要になってくるのでしっかり覚えてください。(水素結合については「水素結合とは(水などの例・沸点・エネルギー・距離と強さの比較)」の記事で詳しく解説しているので是非参考にしてください。)
5. まとめ
最後に電気陰性度についてまとめておこうと思います。
- 原子が共有電子対を自分の方に引っ張る強さのことを電気陰性度といい、電気陰性度が高い原子がより強く共有電子対を自分側に引き寄せる。
- 原子間の電気陰性度の差によって生じる電荷の偏りを極性といい、極性を持つ分子を極性分子という。
- 極性を持たない分子を無極性分子という。
- 電気陰性度は同周期では右側に、同族では上側にいくにしたがって大きくなる。
- 希ガスの電気陰性度は考慮しない
- 電気陰性度の大小、\[{\rm F}>{\rm O}>{\rm N}={\rm Cl}>{\rm C}>{\rm H}\] を語呂合わせF>O>N(フォン)=Cl>C>H(狂っちゃう)で覚える。
以上が電気陰性度のまとめです。
電気陰性度はイオン化エネルギーや電子親和力と混同しやすいので「イオン化エネルギーと電子親和力のまとめ」の記事と合わせてしっかり区別できるようしてください。
電気陰性度は結合の部分と密接に関係しているので電気陰性度とちゃんと理解することで結合の部分も理解しやすくなると思います。
この記事を読んでマスターしましょう!















電気陰性度とイオン化エネルギー・電子親和力の模式図は抜群です。2点確認があります。多忙のなか恐縮ですが、貴方回答をよろしくお願いします。
1.イオン結合の上では、電気陰性度はどう考えたらいいか。(模式図があれば共有結合を持ち出さずとも、統一的にイメージがつかめるのでは)
2 金属のイオン化傾向と電気陰性度との関連はどう考えたらいいか。了