東大塾長の山田です。
このページでは,「熱化学方程式を使った計算問題の解き方」を解説します。
熱化学方程式を使った計算問題は解き方が決まっているので,覚えてしまえば簡単に解けます。今回は、その解答の手順を,例題を用いながら詳しく説明していくので,是非参考にしてください!
1. 熱化学方程式を使った計算問題の解き方
「反応熱の計算(生成熱・燃焼熱・溶解熱・中和熱・結合エネルギー)」の記事で「熱化学方程式」について説明しました。
ここでは、熱化学方程式を使った計算問題の解き方を例題を用いて紹介していきます。
このような問題があったとき、以下の手順で解答を導き出します。
- 求める反応熱を \( Q \rm{kJ/mol} \) などと文字で置き、その反応熱を含む熱化学方程式を作る。
- 問題文で与えられた反応熱を含む熱化学方程式を作る。
- ②で作った熱化学方程式から連立方程式などと同じ要領で①で作った熱化学方程式と同じ形を作る。
- ③で作った熱化学方程式の反応熱にあたる部分が求める反応熱となるので解答が得られる。
文章だけではわかりにくいので実際に例題をこの手順に沿って解いていきましょう。
① まず、アセチレンの燃焼熱を \( Q \rm{kJ/mol} \) とおく。そして、アセチレンの燃焼熱を含む熱化学方程式、つまり、アセチレンの燃焼の化学反応式を作る。
\( \displaystyle C_2H_2(気)+\frac{5}{2}O_2(気)=2CO_2(気)+H_2O(液)+ Q \rm{kJ} \cdots (1) \)
② 次に、問題文で与えられた反応熱(二酸化炭素の生成熱、水の生成熱、アセチレンの生成熱)を含む熱化学方程式を作る。
\( \displaystyle C(黒)+O_2(気)=CO_2(気)+ 394 \rm{kJ} \cdots (2) \)
\( \displaystyle H_2(気)+\frac{1}{2}O_2(気)=H_2O(液)+ 286 \rm{kJ} \cdots (3) \)
\( \displaystyle 2C(黒)+H_2(気)=C_2H_2(気)- 227 \rm{kJ} \cdots (4) \)
③ ②で作った熱化学方程式を足し、引きして(1)と同じ形の熱化学方程式を作る。(1)の熱化学方程式と同じ形は(2)×2+(3)ー(4)をすることで得られる。

④ ③で作った熱化学方程式をみると、アセチレンの燃焼熱が \( 1301 \rm{kJ/mol} \) となることがわかる。よって、この問題の答えは \( \color{red}{ Q = 1301 \rm{kJ/mol} } \) となる。
2. 熱化学方程式の問題
では、「1. 熱化学方程式を使った計算問題の解き方」で示した手順をもとに,いくつか問題を解いてみましょう。
問題1
二酸化炭素の生成熱を \( 394 \rm{kJ/mol} \)、水の生成熱を \( 286 \rm{kJ/mol} \)、エタンの生成熱を \( 84 \rm{kJ/mol} \) とするとき、エタンの燃焼熱を求めよ。
【解答】
① まず、エタンの燃焼熱を \( Q \rm{kJ/mol} \) とおきます。そして、エタンの燃焼熱を含む熱化学方程式、つまり、エタンの燃焼の化学反応式を作ります。
\( \displaystyle C_2H_6(気)+\frac{7}{2}O_2(気)=2CO_2(気)+3H_2O(液)+ Q \rm{kJ} \cdots (1) \)
② 次に、問題文で与えられた反応熱(二酸化炭素の生成熱、水の生成熱、エタンの生成熱)を含む熱化学方程式を作ります。
\( \displaystyle C(黒)+O_2(気)=CO_2(気)+ 394 \rm{kJ} \cdots (2) \)
\( \displaystyle H_2(気)+\frac{1}{2}O_2(気)=H_2O(液)+286 \rm{kJ} \cdots (3) \)
\( \displaystyle 2C(黒)+3H_2(気)=C_2H_6(気)+ 84 \rm{kJ} \cdots (4) \)
③ ②で作った熱化学方程式を足し、引きして(1)と同じ形の熱化学方程式を作ります。(1)の熱化学方程式と同じ形は(2)×2+(3)×3ー(4)をすることで得られます。

④ ③で作った熱化学方程式をみると、エタンの燃焼熱が \( 1562 \rm{kJ/mol} \) となることがわかります。
答‥1562 kJ/mol
問題2
一酸化炭素の燃焼熱を \( 280 \rm{kJ/mol} \)、水の生成熱を \( 286 \rm{kJ/mol} \)、酢酸の燃焼熱を \( 870 \rm{kJ/mol} \) とするとき、一酸化炭素から酢酸を生成するときの生成熱を求めよ。
【解答】
① まず、酢酸の生成熱を \(Q \rm{kJ/mol} \) とおきます。そして、酢酸の生成熱を含む熱化学方程式、つまり、一酸化炭素からの酢酸の生成の化学反応式を作ります。
\( \displaystyle 2CO(気)+2H_2(気)=CH_3COOH(気)+ Q \rm{kJ} \cdots (1) \)
② 次に、問題文で与えられた反応熱(一酸化窒素の燃焼熱、水の生成熱、酢酸の燃焼熱)を含む熱化学方程式を作ります。
\( \displaystyle CO(気)+\frac{1}{2}O_2(気)=CO_2(気)+ 280 \rm{kJ} \cdots (2) \)
\( \displaystyle H_2(気)+\frac{1}{2}O_2(気)=H_2O(液)+ 286 \rm{kJ} \cdots (3) \)
\( \displaystyle CH_3COOH(気)+2O_2(気)=2CO_2(気)+2H_2O(液)+ 870 \rm{kJ} \cdots (4) \)
③ ②で作った熱化学方程式を足し、引きして(1)と同じ形の熱化学方程式を作ります。(1)の熱化学方程式と同じ形は(2)×2+(3)×2ー(4)をすることで得られます。
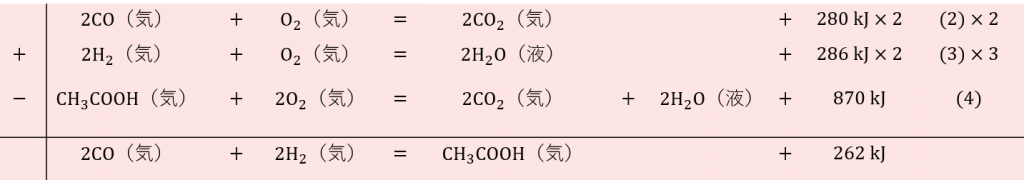
④ ③で作った熱化学方程式をみると、一酸化炭素からの酢酸の生成熱が \( 262 \rm{kJ/mol} \) となることがわかります。
答‥262 kJ/mol
問題3
一酸化窒素の生成熱を \( -90.3 \rm{kJ/mol} \)、一酸化窒素の燃焼熱を \( 57.1 \rm{kJ/mol} \)とするとき、二酸化窒素の生成熱を求めよ。
【解答】
① まず、二酸化窒素の生成熱を \( Q \rm{kJ/mol} \) とおきます。そして、二酸化窒素の生成熱を含む熱化学方程式、つまり、二酸化窒素の生成の化学反応式を作ります。
\( \displaystyle \frac{1}{2}N_2(気)+O_2(気)=NO_2(気)+ Q \rm{kJ} \cdots (1) \)
② 次に、問題文で与えられた反応熱(一酸化窒素の生成熱、一酸化窒素の燃焼熱)を含む熱化学方程式を作ります。
\( \displaystyle \frac{1}{2}N_2(気)+\frac{1}{2}O_2(気)=NO(気)- 90.3 \rm{kJ} \cdots (2) \)
\( \displaystyle NO(気)+\frac{1}{2}O_2(気)=NO_2(液)+ 57.1 \rm{kJ} \cdots (3) \)
③ ②で作った熱化学方程式を足し、引きして(1)と同じ形の熱化学方程式を作ります。(1)の熱化学方程式と同じ形は(2)+(3)をすることで得られます。
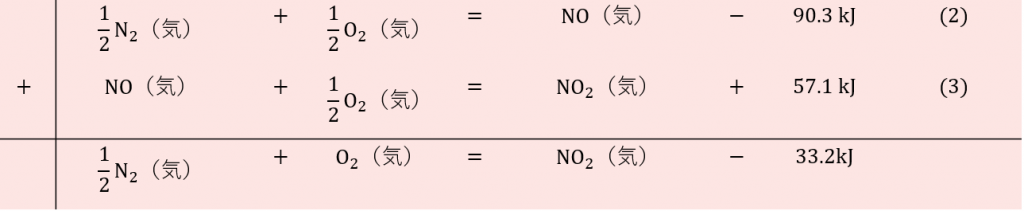
④ ③で作った熱化学方程式をみると、二酸化窒素の生成熱が \( -33.2 \rm{kJ/mol} \) となることがわかります。
答‥-33.2 kJ/mol
3. 熱化学方程式の解き方まとめ
さいごに熱化学方程式の計算問題の解き方についてまとめます。
① 求める反応熱を \( Q \rm{kJ/mol} \)などと文字で置き、その反応熱を含む熱化学方程式を作る。
② 問題文で与えられた反応熱を含む熱化学方程式を作る。
③ ②で作った熱化学方程式から連立方程式などと同じ要領で①で作った熱化学方程式と同じ形を作る。
④ ③で作った熱化学方程式の反応熱にあたる部分が求める反応熱となるので解答が得られる。
熱化学方程式の計算問題は解き方を覚えれば簡単に解くことができます。
多くの問題をこなし、確実に得点できるようにしっかりマスターしてください!
















二酸化炭素の生成熱が \( 394 \rm{kJ/mol} \)、水の生成熱が \( 286 \rm{kJ/mol} \)、アセチレンの生成熱が \( – 227 \rm{kJ/mol} \) であったとき、アセチレンの燃焼熱を求めよ。