東大塾長の山田です。
このページでは,「ヘスの法則」について解説しています。
ヘスの法則は熱化学方程式やエネルギー図に関する問題を解くうえで重要な法則です。
今回はヘスの法則を,具体例を用いて理解しやすいように説明したので、この記事を読んでしっかり内容をマスターしてください!
1. 熱とエネルギー
1.1 熱とエネルギーの違い
熱化学の分野では、生成熱や燃焼熱などの「~熱」と表されるものと、結合エネルギーやイオン化エネルギーなどの「~エネルギー」と表されるものがあります。
これらには、明確な違いがあります。ここでは、これらの違いについて説明していきます。
熱化学における「熱」という言葉は、ある化学反応をしたときに放出するエネルギーのことを指します。
一方で、熱化学における「エネルギー」という言葉は、ある物質を不安定な状態にするために加えるエネルギーのことを指します。
すべての物質は安定の状態でいようとします。それを不安定な状態にするためには、その分熱量を加える必要があります。
1.2 エネルギーの大小
エネルギーの大きさと物質の安定性には関係性があり、エネルギーが高い物質は不安定、エネルギーが低い物質は安定となります。
また、物質の状態によってエネルギーの大小が決まっており、具体的には次のようになります。
イオン>原子>単体>化合物>完全燃焼後に残った物質>水和物
このように、イオンが一番エネルギーが高く不安定、水和物が一番エネルギーが低く安定であると考えることができます。
これは、エネルギー図をつくるときにも役に立ちます。
2. エネルギー図
各物質がもつ化学エネルギーの大きさの相対的な関係を示した図のことをエネルギー図といいます。
エネルギー図では、エネルギーが小さい物質ほど下に、エネルギーが大きい物質ほど上に表記します。
以下では、エネルギー図の書き方について解説していきます。
まず、エネルギー図を作るにあたって、熱化学方程式を考えます。
ここでは、メタンの燃焼熱を例に進めていきましょう。
メタンの燃焼熱の熱化学方程式は次のようになります。
\( \displaystyle CH_4(気) + 2O_2(気) = CO_2(気) + 2H_2O(液) + 891 \rm{kJ/mol} \)
この方程式より、エネルギーの大小は、「反応物のエネルギーの総和」>「生成物のエネルギーの総和」となるので、次のように書けます。

ここに、反応熱を書き加えます。メタンの燃焼熱は次のようになります。
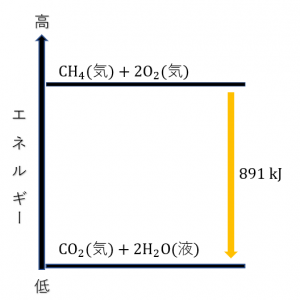
最後にやじるしを書き、その隣に燃焼熱の値を書き込みます。しかし、「熱」と「エネルギー」でやじるしの書き方が変わります。
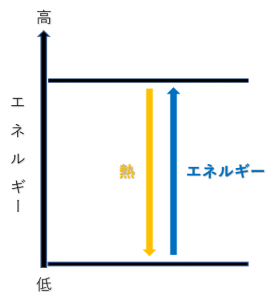
「熱」は下向きのやじるし、「エネルギー」は上向きのやじるしで表します。
3. ヘスの法則
物質が変化するときに出入りする総熱量は、「変化する前の物質の種類と状態」および「変化した後の物質の種類と状態」だけで決まり、その変化の経路や方法には無関係である、という法則のことをヘスの法則といいます。
ヘスの法則は、総熱量保存の法則とも呼ばれます。
言葉だけではわかりにくいので、具体例を用いて説明します。
変化する前の物質を黒鉛と気体の酸素、変化した後の物質を二酸化炭素とします。
この変化には次の2通りが考えられます。
【1つ目】
\( 1 \rm{mol} \) の \( C(黒)\)を完全燃焼させます。この反応の熱化学方程式は次のようになります。
\( \displaystyle C(黒) + O_2(気) = CO_2(気) + 394 \rm{kJ} \)
【2つ目】
まず、\( 1 \rm{mol} \) の \( C(黒) \)から、\( 1 \rm{mol} \) の \( CO(気) \)を生成します。その後、生成した\( 1 \rm{mol} \) の \( CO(気) \)を完全燃焼させます。
この2つの反応の熱化学方程式は次のようになります。
\( \displaystyle C(黒) + \frac{1}{2} O_2(気) = CO(気) + 111 \rm{kJ} \)
\( \displaystyle CO(気) + \frac{1}{2} O_2(気) = CO(気) + 283 \rm{kJ} \)
1つ目の反応における反応熱(\( 394 \rm{KJ} \))は、2つ目の2つの反応の反応熱の総和(\( 283 + 111 = 394 \rm{kJ} \))と等しくなります。
このような関係をヘスの法則というのです。
これらをエネルギー図にすると、次のようになります。
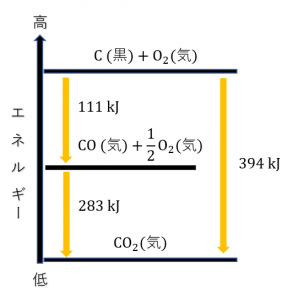
5. まとめ
さいごにヘスの法則についてまとめます。
- 熱化学における「熱」という言葉は、ある化学反応をしたときに放出するエネルギーのことを指す。一方で、熱化学における「エネルギー」という言葉は、ある物質を不安定な状態にするために加えるエネルギーのことを指す。
- エネルギーが高い物質は不安定、エネルギーが低い物質は安定となる。
- 物質の状態におけるエネルギーはエネルギーが大きい順に、「イオン>原子>単体>化合物>完全燃焼後に残った物質>水和物」である。
- 各物質がもつ化学エネルギーの大きさの相対的な関係を示した図のことをエネルギー図といい、エネルギー図では、エネルギーが小さい物質ほど下に、エネルギーが大きい物質ほど上に表記する。
- エネルギー図において、「熱」は下向きのやじるし、「エネルギー」は上向きのやじるしで表す。
- 物質が変化するときに出入りする総熱量は、「変化する前の物質の種類と状態」および「変化した後の物質の種類と状態」だけで決まり、その変化の経路や方法には無関係である、という法則のことをヘスの法則という。ヘスの法則は、総熱量保存の法則とも呼ばれる。
ヘスの法則の考え方は熱化学方程式やエネルギー図に関する問題を解くうえで、かなり重要です。
ですが、考え方自体はすごく単純で理解しやすいと思います。しっかりマスターしてください!















とてもわかりやすく参考になりました。ありがとうございました。