東大塾長の山田です。
このページでは酸化数、半反応式について解説しています。
酸化数の定義、半反応式の作り方など詳しく説明しています。是非参考にしてください。
1. 酸化・還元
酸化・還元の定義には「酸素、水素に関する定義」、「電子に関する定義」、「酸化数に関する定義」の3パターンが考えられます。1では「酸素、水素に関する定義」と「電子に関する定義」について解説します。「酸化数に関する定義」については2で解説します。
1.1 電子に関する定義
物質が電子を失う反応のことを酸化、物質が電子を得る反応のことを還元といいます。
亜鉛を例に考えてみましょう。亜鉛\(Zn\)が電子を放出し亜鉛イオン\(Zn^{2+}\)になったとするとき(\(Zn→Zn^{2+}+2e^-\))、亜鉛\(Zn\)は電子を放出しているので「¥(Zn¥)は酸化している」ことになります。
また、亜鉛イオン\(Zn^{2+}\)が電子を得て亜鉛\(Zn\)になったとするとき(\(Zn^{2+}+2e^-→Zn\))、亜鉛イオン\(Zn^{2+}\)は電子を得ているのでで「\(Zn^{2+}\)は還元している」ことになります。
酸化と還元は必ず同時に起こっているので、まとめて酸化還元反応といいます。酸化還元反応は電子の授受です。
1.2 酸素、水素に関する定義
原子\(A\)が酸素原子\(O\)と結合しているとしたとき、酸素原子\(O\)は他の多くの原子に比べ電気陰性度が大きくなります。そのため、共有電子対は酸素原子\(O\)の方に引き付けられます。
そのため、原子\(A\)は酸素\(O\)に電子\(e^-\)を奪われたことになります。したがって、「酸素原子\(O\)と結合する(酸素原子\(O\)を得る)=電子\(e^-\)を失う=酸化される」ということになります。
物質が酸素原子を得る反応→酸化
物質が酸素原子を失う反応→還元
次に、原子\(A\)が水素原子\(H\)と結合しているとしたとき、水素原子\(H\)は他の多くの原子に比べ電気陰性度が小さくなります。そのため、共有電子対は原子\(A\)の方に引き付けられます。
したがって、水素原子\(H\)が離れると原子\(A\)はせっかく手に入れた電子を失うことになります。
よって、「水素原子\(H\)と失う=電子\(e^-\)を失う=酸化される」ということになります。
物質が水素原子を失う反応→酸化
物質が水素原子を得る反応→還元
2. 酸化数
物質の持つ電子が基準よりも多いか少ないかを表した値のことを酸化数といいます。
2.1 酸化数に関する酸化・還元
1では「酸素・水素に関する酸化・還元」と「電子に関する酸化・還元」について説明しましたが、ここでは「酸化数に関する酸化・還元」について説明します。
酸化された物質は、マイナスの電荷を持った電子\(e^-\)を失うので、プラスに帯電します。電子\(e^-\)を1つ失うと酸化数は\(+1\)、2つ失うと酸化数は\(+2\)というように変化します。
一方、還元された物質は、マイナスの電荷を持った電子\(e^-\)を得るので、マイナスに帯電します。電子\(e^-\)を1つ得ると酸化数は\(-1\)、2つ得ると酸化数は\(-2\)というように変化します。
物質を構成する原子の酸化数が増加する反応→酸化
物質を構成する原子の酸化数が減少する反応→還元
2.2 酸化数の規則
原子の酸化数を決定するにはいくつかの規則があります。ここでは、その規則について説明していこうと思います。
2.2.1 単体の酸化数
単体は、2つの原子の電気陰性度に差がないので共有電子対は原子間の真ん中に存在します。そのため、原子は電子\(e^-\)を得ることも失うこともないので酸化数は0になります。
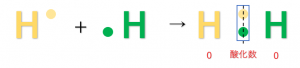
例:\(Na\)(\(Na : 0\))、\(H_2\)(\(H : 0\))、\(O_2\)(\(O : 0\))
2.2.2 化合物の酸化数
まず、化合物全体では酸化数は0になります。
化合物は異なる原子同士が結合してできているので、原子間には電気陰性度に差が生じます。例としてフッ化水素\(HF\)について考えてみましょう。電気陰性度はフッ素\(F\)の方が大きくなります。したがって、共有電子対は電気陰性度の大きな\(F\)原子に引き付けられ、\(F\)原子は電子\(e^-\)を得ていると考えることができます。
しかし、化合物全体で見たときには電子の総数に変化はないため化合物の酸化数は0となります。
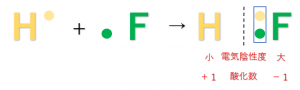
例:\(H_3PO_4\)(\(H : +1\)、\(P : +5\)、\(O : -2\))
2.2.3 単原子イオンの酸化数
単原子イオンの酸化数はそのイオンの電荷と等しくなります。
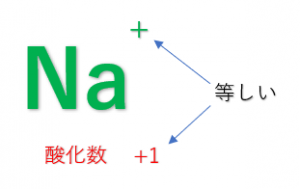
例:\(Na^{+1}\)(\(Na : +1\))、\(Fe^{+2}\)(\(Fe : +2\))、\(Cl^{-1}\)(\(Cl : -1\))
2.2.4 多原子イオンの酸化数
多原子イオンの酸化数も単原子イオンの酸化数と同様に考えられます。
構成する原子の酸化数の総和が他原子イオンの電荷と一致します。
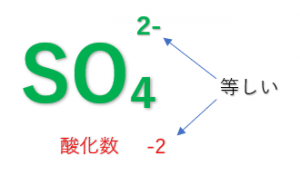
例:\({NH_4}^{+1}\)(\(N : -3、H : +1\))、\({SO_4}^{2-}\)(\(S : +6、O : -2\))
2.2.5 水素原子の酸化数
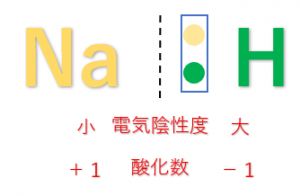
水素原子\(H\)は、他の非金属元素に比べると電気陰性度が小さくなるので共有電子対は結合している原子に引き付けられます。そのため、酸化数は+1となります。
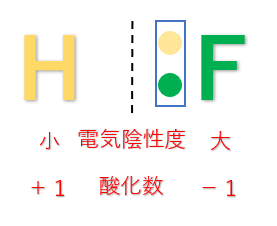
ただし、金属元素と結合するときは金属元素よりも電気陰性度が大きくなるため共有電子対が水素原子の方に引き付けられ、酸化数は-1となります。
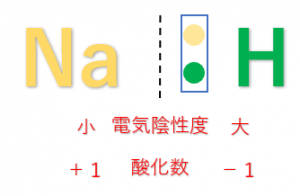
2.2.6 酸素原子\(O\)の酸化数
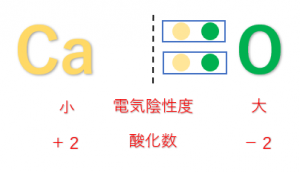
酸素原子\(O\)は電気陰性度が大きく、2組の共有電子対を引き付けます。したがって、酸化数は-2となります。
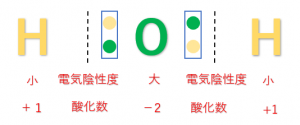
ただし、過酸化水素\(H_2O_2\)のような過酸化物(-O-O-構造)をもつときは、片方の共有電子対しか引き付けないため酸化数は-1となります。
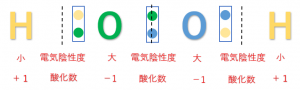
2.2.7 ハロゲンの酸化数
ハロゲンは電気陰性度が大きいため、共有電子対を引き付けます。そのため、酸化数は-1となります。

2.2.8 アルカリ金属(水素以外の1族元素)・2族元素の酸化数
アルカリ金属や2族元素は電気陰性度が小さいため、共有電子対が結合している原子に引き付けられます。そのため、酸化数はそれぞれ+1、+2となります。
2.3 酸化数の求め方
ここでは、化合物中の元素の酸化数の求め方について解説していきます。酸化数を求めるにあたって2つのルールがあります。
1つ目のルールは単体であるのか、化合物であるのか、イオンであるのかを決定することです。これらが決まれば2.2で説明した規則に従うことができます。
単体の場合→単体の酸化数は0
化合物の場合→化合物全体の酸化数は0
イオンの場合→イオン全体の酸化数は電荷に等しい
2つ目のルールは、わかっている元素の酸化数を代入していき1つ目のルールと合わせて求める元素の酸化数を決定するということです。
2.2で説明したように水素原子や酸素原子はあらかじめ酸化数がわかっています。これを使って求める元素の酸化数を求めます。
①アルカリ金属の酸化数は+1、2族元素の酸化数は+2、ハロゲンの酸化数は-1
②水素原子\(H\)の酸化数は+1
③酸素原子\(O\)の酸化数は-2
④ハロゲン(ハロゲン化物中)の酸化数は-1、硫黄原子\(S\)の酸化数は-2
化合物中に含まれる元素について、①から順番に酸化数を決定する。
それでは、上の2つのルールに従い実際に酸化数を求めてみましょう。
例:リン酸\(H_3PO_4\)
まず、1つ目のルールよりリン酸は化合物であるのでリン酸全体では酸化数は0になります。
次に、2つ目のルールを考慮します。①に含まれる元素はリン酸中に存在しないので②を考えます。②よりリン酸中の水素原子の酸化数は+1となります。次に、③よりリン酸中の酸素原子の酸化数は-2となります。
したがって、リン酸中のリンの酸化数は+5と決定できます。
例:水素化ナトリウム\(NaH\)
まず、1つ目のルールより水素化ナトリウムは化合物であるので水素化ナトリウム全体では酸化数は0になります。
次に、2つ目のルールを考慮します。①より水素化ナトリウム中のナトリウムの酸化数は+1となります。
したがって、水素化ナトリウム中の水素原子の酸化数は-1と決定できます。
例:硫酸イオン\({SO_4}^2-\)
まず、1つ目のルールより硫酸イオンはイオンであるので電荷を考えると硫酸イオン全体では酸化数は-2になります。
次に、2つ目のルールを考慮します。①に含まれる元素は硫酸イオン中に存在しないので②を考えます。②に含まれる元素も硫酸イオン中に存在しないので③を考えます。③より硫酸イオン中の酸素原子の酸化数は-2となります。
したがって、硫酸イオン中の硫黄原子の酸化数は+6となります。
このように2つのルールを考慮して各元素の酸化数を決定します。
3. 酸化剤・還元剤
自分自身が還元されることにより、相手を酸化する物質のことを酸化剤といいます。したがって、還元されやすい物質ほど強い酸化剤となります。
例えば、周期表の右上に位置するフッ素\(F\)や塩素\(Cl\)、酸素\(O\)の原子は、電子親和力が大きく電子を受け取って陰イオンになりやすい原子です。したがって、これらの元素の単体は還元されやすく、強い酸化剤となります。
また、自分自身が酸化されることにより、相手を還元する物質のことを還元剤といいます。したがって、酸化されやすい物質ほど強い還元剤となります。
例えば、リチウム\(Li\)やナトリウム\(Na\)などのアルカリ金属、カルシウム\(Ca\)やバリウム\(Ba\)などのアルカリ土類金属の原子は、イオン化エネルギーが小さく電子を放出しやすいため陽イオンになりやすい原子です。したがって、これらの元素の単体は酸化されやすく、強い還元剤となります。
3.1 半反応式の作り方
ヨウ素\(I_2\)と硫化水素\(H_2S\)の酸化還元反応は次のように表すことができます。
\(H_2S+I_2→S+2HI\)
このように、酸化剤と還元剤を用いて酸化還元反応を表した式のことを酸化還元反応式といいます。(この式において、酸化剤は\(I_2\)、還元剤は\(H_2S\)となります。)
酸化還元反応式は、次のような酸化剤に関する反応式と還元剤に関する反応式を組み合わせることで作ることができます。
\(\begin{align}
酸化剤 &:I_2 + 2e^-→2I^- \\
\\
還元剤 &:H_2S→S + 2H^+ +2e^- \\
\\
\end{align}\)
このように、酸化還元反応式を作るときに必要な酸化剤・還元剤に関する反応式のことを半反応式といいます。
ここでは、半反応式の作り方について解説します。(酸化還元反応式の作り方については「酸化還元反応式の作り方」の記事で解説しているので参照してください。)
今回は\({MnO_4}^-\)が\(Mn^{2+}\)に変化するときの反応を例に説明していきます。
【半反応式を作る手順】
①酸化剤(還元剤)の反応前、反応後の化学式がどのようになるかを書く
まず、\({MnO_4}^-\)が\(Mn^{2+}\)へと変化する反応であることから反応前の化学式を左辺、反応後の化学式を右辺に書きます。
\({MnO_4}^- → Mn^{2+}\)
②両辺の水素原子\(H\)、酸素原子\(O\)以外の原子の数を合わせる。
今回の反応では\(Mn\)の数が両辺で等しいので上の式のままで大丈夫です。(\({Cr_2O_7}^{2-}\)が\(Cr^{3+}\)に変化するような反応では、②で\(Cr\)の数を合わせる必要があります。)
\({MnO_4}^- → Mn^{2+}\)
③両辺の酸素原子\(O\)の数を\(H_2O\)を用いて合わせる。
②までに作った式の左辺と右辺の比べると、右辺は酸素原子が4つ不足しているので右辺に4つの\(H_2O\)を加えます。
\({MnO_4}^- → Mn^{2+} + 4H_2O\)
④両辺の水素原子\(H\)の数を水素イオン\(H^+\)を用いて合わせる。
③までに作った式を比べると、左辺は水素原子\(H\)が8つ不足しているので左辺に水素イオン\(H^+\)を8つ加えます。
\({MnO_4}^- + 8H^+ → Mn^{2+} + 4H_2O\)
⑤両辺の電荷を電子\(e^-\)を用いて合わせる。
④までに作った式を比べると左辺の電荷は+7、右辺の電荷は2+となっています。これより、左辺に電子\(e^-\)を5つ加えることで両辺の電荷を合わせます。
\({MnO_4}^- + 8H^+ + 5e^-→ Mn^{2+} + 4H_2O\)
これで半反応式の完成です。
ここで、酸素の半反応式は3.2の表から次のようになることがわかるのですが、これは酸性水溶液中での反応です。
\(O_2 +4H^+ + 4e^- → 2H_2O\)
中性、塩基性水溶液中での反応を考える際にはこの式の両辺に\(OH^-\)を加えます。加える量としては左辺、もしくは右辺にある水素イオンがなくなる分を加えます。この場合は両辺に4つの\(OH^-\)を加えます。加えた後の式は次のようになります。
\(O_2 + 2H_2O + 4e^- →4OH^-\)
4つの水素イオンと4つの水酸化物イオンが結合し水になっています。
3.2 覚えるべき酸化剤と還元剤
3.1で半反応式の作り方について解説しましたが、半反応式の作り方の手順①からわかるように半反応式は反応前の化学式と反応後の化学式を覚えていないと作ることができません。以下に、高校化学で出題される酸化剤、還元剤の反応前・反応後の化学式を示しておくので必ず覚えてください!
【酸化剤】
| 酸化剤名 | 反応前の化学式 | 反応後の化学式 |
| 二クロム酸カリウム (硫酸性水溶液中) |
\({Cr_2O_7}^{2-}\) | \(Cr^{3+}\) |
| 過マンガン酸カリウム (硫酸性水溶液中) |
\({MnO_4}^-\) | \(Mn^{2+}\) |
| 過マンガン酸カリウム (中性・塩基性水溶液中) |
\({MnO_4}^-\) | \(MnO_2\) |
| 酸化マンガン(Ⅳ) | \(MnO_2\) | \(Mn^{2+}\) |
| 濃硝酸 | \(HNO_3\) | \(NO_2\) |
| 希硝酸 | \(HNO_3\) | \(NO\) |
| 熱濃硫酸 | \(H_2SO_4\) | \(SO_2\) |
| オゾン | \(O_3\) | \(O_2\) |
| 酸素 | \(O_2\) | \(H_2O\) |
| 過酸化水素 | \(H_2O_2\) | \(H_2O\) |
| 二酸化硫黄 | \(SO_2\) | \(S\) |
| ハロゲンの単体 | \(X_2\)(\(X_2:F_2,Cl_2,Br_2,I_2\)) | \(X^-\) |
【還元剤】
| 還元剤名 | 反応前の化学式 | 反応後の化学式 |
| 硫化水素 | \(H_2S\) | \(S\) |
| シュウ酸 | \(H_2C_2O_4\) | \(CO_2\) |
| 水素 | \(H_2\) | \(H^+\) |
| チオ硫酸ナトリウム | \({S_2O_3}^{2-}\) | \({S_4O_6}^{2-}\) |
| 陽性の強い金属の単体 | \(Na\) \(Ca\) |
\(Na^+\) \(Ca^{2+}\) |
| 塩化スズ(Ⅱ) | \(Sn^{2+}\) | \(Sn^{4+}\) |
| 硫化鉄(Ⅱ) | \(Fe^{2+}\) | \(Fe^{3+}\) |
| 二酸化硫黄 | \(SO_2\) | \({SO_4}^{2-}\) |
| 過酸化水素 | \(H_2O_2\) | \(O_2\) |
上の表からわかるように、過酸化水素\(H_2O_2\)と二酸化硫黄\(SO_2\)は、反応する相手によっては酸化剤にも還元剤にもなります。
4. 代表的な酸化剤・還元剤の詳細
4.1 代表的な酸化剤の詳細
4.1.1 \(KMnO_4\)
過マンガン酸カリウム\(KMnO_4\)は水によく溶け、水溶液中で\({MnO_4}^-\)を生じます。
\({MnO_4}^-\)は強い酸化作用を示し、\(KMnO_4\)は、主に硫酸酸性水溶液中で用いられます。このとき、硝酸や塩酸は用いることができません。この理由は、硝酸を用いると、硝酸自身が酸化剤として働き、塩酸を用いると\(Cl^-\)が還元剤として働くので求めたい酸化還元反応などを妨げてしまうことがあるからです。
硫酸酸性水溶液中では、\({MnO_4}^-\)は次のように反応します。
\({MnO_4}^- + 8H^+ + 5e^-→ Mn^{2+} + 4H_2O\)
\({MnO_4}^-\)は赤紫色であるのに対し、\(Mn^{2+}\)はほぼ無色であるため、水溶液の色の変化によって酸化還元反応の進行の様子を知ることができます。
一方で、\(H^+\)がわずかしかない中性、または塩基性水溶液中では\({MnO_4}^-\)は\(MnO_2\)に還元されます。この反応を表す式は次のようになります。
\({MnO_4}^- + 2H_2O+ + 3e^-→ MnO_2 + 4OH^-\)
酸化マンガン(Ⅱ)\(MnO_2\)は黒褐色の沈殿です。
4.1.2 \(K_2Cr_2O_7\)
二クロム酸カリウム\(K_2Cr_2O_7\)は赤橙色の結晶で、水に溶け水溶液中でニクロム酸イオン\({Cr_2O_7}^{2-}\)を生じます。\({Cr_2O_7}^{2-}\)は強い酸化作用を示し、\(K_2Cr_2O_7\)は、主に硫酸酸性水溶液中で用いられます。この反応の半反応式は次のようになります。
\({Cr_2O_7}^{2-} + 14H^+ + 6e^- → 2Cr^{3+} + 7H_2O\)
\({Cr_2O_7}^{2-}\)は赤橙色であるのに対し、\(Cr^{3+}\)は緑色であるため、水溶液の色の変化によって酸化還元反応の進行の様子を知ることができます。
4.1.3 ハロゲンの単体
ハロゲンの単体は酸化作用を示します。その酸化力は、原子番号が小さくなるほど強くなり以下のようになります。
\(F_2>Cl_2>Br_2>I_2\)
この酸化力の大小から酸化還元反応が起こるかがわかります。ハロゲン\(A\)と\(B\)があったとして、酸化力が\(A>B\)であったとします。このとき、次式の正反応は起こりますが、逆反応は起こりません。
\(2B^- + A_2 → 2A^- + B_2\)
逆に、ハロゲン化物イオンは、還元作用を示します。その還元力は、原子番号が大きいほど強くなり以下のようになります。
\(I^->Br^->Cl^->F^-\)
これは、ハロゲン単体の酸化力とは逆になっていることがわかり、上の式がハロゲン化物イオンの還元力の観点からみても成り立つことがわかります。
4.2 代表的な還元剤の詳細
4.2.1 \(H_2S\)
硫化水素\(H_2S\)は無色で腐卵臭のある気体です。火山ガスや硫黄泉に含まれるなど、天然に多く存在しているので、自然界には\(H_2S\)が関わる酸化還元反応がたくさんあります。
\(H_2S\)の還元剤としての働きを示す半反応式は次のようになります。
\(H_2 → S + 2H^+ + 2e^-\)
硫黄原子の酸化数は、-2から+6の範囲内で複数の値をとることができます。
5. まとめ
最後に酸化数についてまとめておこうと思います。
単体の場合→単体の酸化数は0
化合物の場合→化合物の酸化数は0
イオンの場合→イオン全体の酸化数は電荷と等しい
アルカリ金属の酸化数は+1、2族元素の酸化数は+2、ハロゲンの酸化数は-1、水素原子\(H\)の酸化数は+1、酸素原子\(O\)の酸化数は-2、ハロゲン(ハロゲン化物中)の酸化数は-1、硫黄原子\(S\)の酸化数は-2
【酸化剤】
| 酸化剤名 | 反応前の化学式 | 反応後の化学式 |
| 二クロム酸カリウム (硫酸性水溶液中) |
\({Cr_2O_7}^{2-}\) | \(Cr^{3+}\) |
| 過マンガン酸カリウム (硫酸性水溶液中) |
\({MnO_4}^-\) | \(Mn^{2+}\) |
| 過マンガン酸カリウム (中性・塩基性水溶液中) |
\({MnO_4}^-\) | \(MnO_2\) |
| 酸化マンガン(Ⅳ) | \(MnO_2\) | \(Mn^{2+}\) |
| 濃硝酸 | \(HNO_3\) | \(NO_2\) |
| 希硝酸 | \(HNO_3\) | \(NO\) |
| 熱濃硫酸 | \(H_2SO_4\) | \(SO_2\) |
| オゾン | \(O_3\) | \(O_2\) |
| 酸素 | \(O_2\) | \(H_2O\) |
| 過酸化水素 | \(H_2O_2\) | \(H_2O\) |
| 二酸化硫黄 | \(SO_2\) | \(S\) |
| ハロゲンの単体 | \(X_2\)(\(X_2:F_2,Cl_2,Br_2,I_2\)) | \(X^-\) |
【還元剤】
| 還元剤名 | 反応前の化学式 | 反応後の化学式 |
| 硫化水素 | \(H_2S\) | \(S\) |
| シュウ酸 | \(H_2C_2O_4\) | \(CO_2\) |
| 水素 | \(H_2\) | \(H^+\) |
| チオ硫酸ナトリウム | \({S_2O_3}^{2-}\) | \({S_4O_6}^{2-}\) |
| 陽性の強い金属の単体 | \(Na\) \(Ca\) |
\(Na^+\) \(Ca^{2+}\) |
| 塩化スズ(Ⅱ) | \(Sn^{2+}\) | \(Sn^{4+}\) |
| 硫化鉄(Ⅱ) | \(Fe^{2+}\) | \(Fe^{3+}\) |
| 二酸化硫黄 | \(SO_2\) | \({SO_4}^{2-}\) |
| 過酸化水素 | \(H_2O_2\) | \(O_2\) |
反応前の化学式と反応後の化学式を覚えておけば半反応式はこの記事で説明した手順に沿っていけば導き出すことができます。しかし、覚えていなければ次に説明する酸化還元反応に関する問題に取り掛かることができません。
最後にもまとめましたが、酸化剤・還元剤がどのように反応するかはかなり重要なので確実に覚えてください!















物質が電子を失う反応→酸化
物質が電子を得る反応→還元