東大塾長の山田です。
このページではイオン化傾向について解説しています。
イオン化傾向に関する金属の反応性や性質を詳しく説明しています。是非参考にしてください。
1. イオン化傾向
金属(金属単体の原子)が水または水溶液中で陽イオンになろうとする性質のことをイオン化傾向といいます。
イオン化傾向の大きな金属ほど、相手の物質に電子を与え、自分自身は電子を失い陽イオンになりやすくなります。つまり、イオン化傾向の大きな金属ほど、酸化されやすく強い還元力を持ちます。
2. イオン化列と覚え方
イオン化傾向は各金属元素によって異なります。金属元素をイオン化傾向の大きな順に並べたものをイオン化列といいます。イオン化列は次のようになります。
\(Li>K>Ca>Na>Mg>Al>Zn>Fe>Ni>Sn>Pb>\)
\(H_2>Cu>Hg>Ag>Pt>Au\)
\(Li\)がイオン化傾向が一番大きく、\(Au\)がイオン化傾向が一番小さくなります。
このイオン化列において左にいけばいくほどイオン化傾向は大きくなるので、陽イオンになりやすいです。また、水素\(H_2\)は金属ではありませんが、金属と同様に陽イオンになる性質を持っているため、比較のためイオン化列に加えられます。
金属は電子\(e^-\)を放出して陽イオンになる性質をもっているので還元剤です。そのため、イオン化傾向が大きい金属ほど反応性が高くなります。
問題を解くうえでイオン化列の正しい順番を覚えなければなりません。そこで、イオン化列を覚えるための語呂合わせを紹介します。

このように語呂合わせは「リッチに貸そうかな まああてにすんな ひどすぎる借金」となります。対応する原子は上の通りです。
イオン化列の正しい順番を覚えていなければ問題を解くことはできません。曖昧に覚えるのではなく確実にこの順番は覚えるようにしてください。
3. イオン化傾向と金属の反応性
イオン化傾向と金属の反応性には関連があります。ここでは、それぞれの金属がどの物質とどのように反応するのか説明しています。
3.1 常温の水との反応
イオン化傾向が\(Na\)よりも大きい金属は常温の水と反応して、水素\(H_2\)を発生して水酸化物となります。これにより、反応後の水溶液は塩基性を示し、フェノールフタレイン溶液によって赤く呈色します。
\(2K + 2H_2O → 2KOH + H_2\)
\(Ca + 2H_2O → Ca(OH)_2 + H_2\)
\(Na\)、\(K\)は水と激しく反応しますが、\(Li\)は水と穏やかに反応します。
3.2 熱水や高温の水蒸気との反応
\(Mg\)は、常温の水とは反応しませんが、熱水(沸騰水)とは反応して水素を発生して水酸化物をとなります。
また、\(Mg\)よりイオン化傾向が小さい\(Al\)、\(Zn\)、\(Fe\)は、常温の水や熱水とは反応しませんが、高温の水蒸気とは反応し、水素を発生して水酸化物となります。
・\(Mg\)は熱水と反応
\(Mg + 2H_2O → Mg(OH)_2 + H_2\)
・\(Al\)、\(Zn\)、\(Fe\)は高温の水蒸気と反応
\(2Al+ 3H_2O → Al_2O_3 + 3H_2\)
\(3Fe + 4H_2O → Fe_3O_4 + 4H_2\)
3.3 酸との反応
水素\(H_2\)よりもイオン化傾向の大きい金属、\(Li\)~\(Pb\)までの金属は、水素より強い還元力をもつので水素イオン\(H^+\)を水素\(H_2\)に還元することができます。そのため、このような金属は塩酸や希硫酸と反応し、水素を発生しながら溶け塩化物や硫酸塩の水溶液となります。
一方で、水素よりもイオン化傾向の小さい金属、\(Cu\)~\(Au\)までの金属は、塩酸や希硫酸と反応せずこれらに溶けることはありません。
\(2Na + 2HCl → 2NaCl + H_2\)
\(Ni + 2HCl → NiCl_2 + H_2\)
ここまで、水素よりイオン化傾向が大きい金属は塩酸や希硫酸と反応すると説明しましたが、\(Pb\)は他の金属とは反応の進み方が異なります。
鉛が塩酸と希硫酸とは以下のように反応します。
\(Pb + 2HCl → PbCl_2 + H_2\)
\(Pb + H_2SO_4 → PbSO_4 + H_2\)
反応の仕方は他の金属と変わりありませんが、反応により生成した\(PbCl_2\)と\(PbSO_4\)は難溶性の塩です。そのため、\(Pb\)が塩酸や希硫酸と反応すると、これらの塩が\(Pb\)の表面を被膜として覆ってしまうためそれ以上溶けることができなくなります。
従って、他の金属と比べ鉛の酸との反応性は極端に低くなります。
3.4 酸化力のある酸との反応
\(Cu\)、\(Hg\)、\(Ag\)、\(Pt\)、\(Au\)など、水素よりもイオン化傾向の小さい金属は、常温の水や熱水、高温の水蒸気、塩酸や希硫酸とは反応しません。その中で、\(Cu\)、\(Hg\)、\(Ag\)は、熱濃硫酸や濃硝酸、希硝酸などの酸化力のある酸とは反応します。
熱濃硫酸の場合には二酸化硫黄、濃硝酸の場合には二酸化窒素、希硝酸の場合には一酸化窒素を発生して溶け、硫酸塩や硝酸塩の水溶液となります。
しかし、\(Pt\)や\(Au\)は、熱濃硫酸、濃硝酸、希硝酸などの酸化力のある酸とも反応しません。ただ、\(Pt\)や\(Au\)は、極めて強い酸化力をもつ王水(王水とは、濃硝酸と濃塩酸の体積比が1:3の混合物のことである)とは反応して溶けます。
・\(Cu\)、\(Hg\)、\(Ag\)は熱濃硫酸、濃硝酸、希硝酸と反応する。
①熱濃硫酸
\(Cu + 2H_2SO_4 → CuSO_4 + 2H_2O + SO_2\)
\(2Ag + 2H_2SO_4 → Ag_2SO_4 + 2H_2O + SO_2\)
②濃硝酸
\(Cu + 4HNO_3 → Cu(NO_3)_2 + 2H_2O + 2NO_2\)
\(Ag + 2HNO_3 → AgNO_3 + H_2O + NO_2\)
③希硝酸
\(3Cu + 8HNO_3 → 3Cu(NO_3)_2 + 4H_2O + 2NO\)
\(3Ag + 4HNO_3 → 3AgNO_3 + 2H_2O + NO\)
・\(Pt\)、\(Au\)は、王水と反応する。
水素よりイオン化傾向の大きい金属も基本的にはこれらの酸に溶けます。しかし、一部の金属は溶けないものもあります。その例が、\(Al\)、\(Fe\)、\(Ni\)です。これら三つの金属は濃硝酸には溶けません。これらの金属に濃硝酸を作用させると、金属の表面に緻密な酸化物の被膜が形成され、それ以上反応が進行しなくなります。そのため、酸化が内部まで進まなくなり、内部が濃硝酸から保護される状態になります。このような状態のことを不動態といいます。
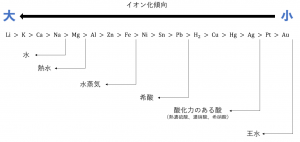
最後に金属の反応性とイオン化傾向の関係をまとめると以下のようになります。水に溶けるのは、\(Li\)~\(Na\)、熱水に溶けるのは\(Li\)~\(Mg\)までというように見ます。
4. イオン化傾向と金属の存在状態
4.1 天然での金属の存在状態
天然における金属の存在状態は、イオン化傾向と密接な関係があります。ここでは、イオン化列をもとに考えていきましょう。
イオン化傾向が\(Mg\)よりも大きい金属は、天然で酸化物、塩化物、炭酸塩、硫酸塩などの様々な化合物やイオン(水溶液中で陽イオン)として存在しています。
また、イオン化傾向が\(Al\)から\(Ag\)までの間にある金属は、天然で主に、酸化物や硫化物として存在しています。ただし、\(Cu\)、\(Hg\)、\(Ag\)は天然で単体として存在することもあります。
\(Pt\)、\(Au\)は天然で単体として存在します。

4.2 金属の製錬
私たちは金属の多くを単体で利用します。しかし、4.1で説明したようにほとんどの金属は天然で化合物の状態で存在しています。そのため、化合物を還元して単体を得ます。このような技術を製錬といいます。
比較的イオン化傾向が小さく、比較的還元が容易な\(Cu\)は、銅鉱石から得た硫化物を強熱することで製錬することができます。また、\(Cu\)よりはイオン化傾向が大きく、\(Cu\)よりは還元が難しい\(Fe\)は鉄鉱石(酸化物)を炭素や一酸化炭素で還元することで製錬することができます。イオン化傾向が大きく、還元が難しい\(Al\)はボーキサイトから得た酸化物を溶融塩電解(融解液の電気分解)することで製錬することができます。
5. 金属単体と金属イオンの反応
亜鉛板を希硫酸中に入れると、これまでに説明してきたように亜鉛板は水に融解します。このとき、次のような反応が起こっています。
亜鉛板は融解して\(Zn^{2+}\)となります。
\(Zn → Zn^{2+} + 2e^-‥‥①\)
\(Zn\)が\(Zn^{2+}\)になることで発生した2つの\(2e^-\)は、希硫酸中に存在している\(H^+\)とくっつき気体の\(H_2\)となり空気中へ出ていきます。
\(2H^+ + 2e^- → H_2‥‥②\)
①+②をすることで次の関係式を得ます。
\(Zn + 2H^+ → Zn^{2+} + H_2‥‥③\)
このような反応を酸化還元反応といいますが、詳しい解説は「酸化還元反応式の作り方」の記事を参照してください。
このように、\(Zn\)が還元剤として働き電子を放出し、\(H^+\)が酸化剤として働いて電子を受け取っています。
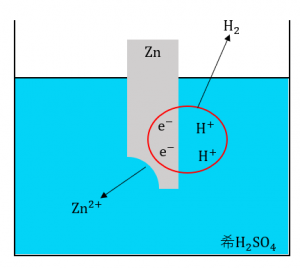
③の反応式はイオン化傾向の関係から左方向には進みません。これは、\(Zn\)のイオン化傾向が\(H_2\)よりも大きいことが原因です。このような関係をもとに、金属単体と金属イオンの反応について考えてみましょう。
金属\(A\)と金属\(B\)があるとします。イオン化傾向は\(A>B\)であったとすると、金属\(A\)の方が金属Bよりも還元力が強くなります。つまり、金属\(A\)自体は酸化してイオンになりやすいということになります。
これらを考慮して金属\(A\)を金属イオン\(B^{n+}\)を含む水溶液中に浸したときの反応を考えてみると、金属\(A\)が溶解し、金属\(B\)が析出します。この反応の式は次のようになります。
\(nA + mB^{n+} → nA^{m+} + mB‥‥④\)
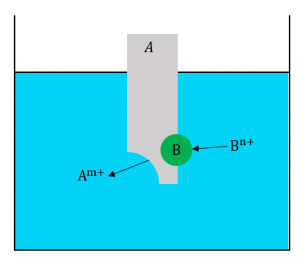
一方で、金属\(B\)を金属イオン\(A^{m+}\)を含む水溶液中に浸しても、イオン化傾向は\(A>B\)であるため何も反応は起こりません。つまり、④式の逆反応は起こらないということです。
例として、\(Zn\)板を硫酸銅(Ⅱ)\(CuSO_4\)水溶液に浸したときを考えます。\(Zn\)と\(Cu\)のイオン化傾向を考えると、\(Zn>Cu\)であるので、\(Zn\)は水溶液中に溶けだし亜鉛イオン\(Zn^{2+}\)になります。
\(Zn → Zn^{2+} + 2e^-‥‥⑤\)
一方、水溶液中の銅イオン\(Cu^{2+}\)は亜鉛が放出した電子を受けとって\(Zn\)板上に\(Cu\)が析出します。
\(Cu^{2+} + 2e^- → Cu‥‥⑥\)
この反応の式は⑤、⑥式を足すことで⑦のようになります。
\(Zn + Cu^{2+} → Zn^{2+} + Cu‥‥⑦\)
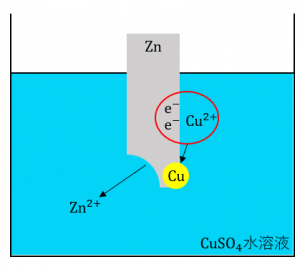
イオン化傾向の大小から⑦式が左方向に進むことはないので、\(Cu\)板を\(Zn^{2+}\)イオンを含む水溶液に浸しても反応は起こりません。
6. 金属の腐食とメッキ
金属の表面が、空気や水にさらされることで空気中や水中の酸素などによって酸化され、単体から酸化物や水酸化物、炭酸塩に変化します。このような現象を金属が腐食する(さびる)といいます。
このような金属の腐食を防ぐ方法の1つに、金属の表面を別の金属の薄膜で覆う方法があります。この方法をめっきといいます。
鉄はさびやすい欠点があり、空気中で\(Fe_2O_3\)や\(FeO(OH)\)などに変化します。鉄の腐食を防ぐめっきの例として、ブリキやトタンがあります。
6.1 トタン
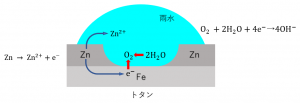
\(Fe\)(鋼板)の表面を\(Zn\)で覆ったものをトタンといいます。\(Zn\)は\(Fe\)よりイオン化傾向が大きく、\(Fe\)より酸化されやすい金属ですが、酸化されて表面に酸化被膜が形成されることで、その緻密な酸化被膜が内部を保護します。よって、トタンは鋼板よりもさびにくくなります。
もし、トタンに傷がつき\(Fe\)が露出したときを考えましょう。このとき、傷がついた部分に雨水が付着すると、水中に溶けている酸素が金属から電子を奪おうとします。このとき、イオン化傾向が大きいほうが陽イオンになりやすいので\(Zn\)が酸化され水中にイオンとして溶け出します。したがって、傷がついても\(Fe\)は酸化されにくく(さびにくく)なります。
6.2 ブリキ
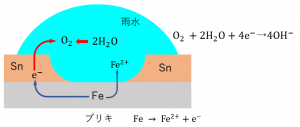
\(Fe\)(鋼板)の表面を\(Sn\)で覆ったものをブリキといいます。\(Sn\)は\(Fe\)よりイオン化傾向が小さく、\(Fe\)より酸化されにくい金属です。さらに、酸化されて表面に酸化被膜が形成されることで、その酸化被膜が内部を保護します。よって、ブリキは鋼板よりもさびにくくなります。
もし、ブリキに傷がつき\(Fe\)が露出したときを考えましょう。このとき、傷がついた部分に雨水が付着すると、水中に溶けている酸素が金属から電子を奪おうとします。このとき、イオン化傾向が大きいほうが陽イオンになりやすいので\(Fe\)が酸化され水中にイオンとして溶け出します。したがって、トタンと違って傷がつくと\(Fe\)は酸化されて(さびて)しまいます。したがって、ブリキは傷がつきにくいところでのみ使われます。
7. まとめ
最後にイオン化傾向についてまとめておこうと思います。
\(Li>K>Ca>Na>Mg>Al>Zn>Fe>Ni>Sn>Pb>\)
\(H_2>Cu>Hg>Ag>Pt>Au\)
語呂合わせは「リッチに貸そうかな まああてにすんな ひどすぎる借金」である。
イオン化傾向が\(A>B\)である金属\(A\)、金属\(B\)について金属\(A\)を金属イオン\(B^{n+}\)を含む水溶液中に浸したとき次のような反応が起こる。
\(nA + mB^{n+} → nA^{m+} + mB\)
この反応の逆反応は起こらない。
金属が水素イオンを含む溶液に溶解するかはイオン化傾向を理解することによって簡単にわかります。また、これから学ぶ電池の仕組みを理解するのにもイオン化傾向の知識が必要です。
イオン化列を覚えていればこのような問題も簡単に解くことができます。比較的理解しやすい分野であると思うのでこの記事を読んでしっかりマスターしてください!















熱濃硫酸と銀の反応式で銀の係数が1になっています。
ご指摘いただきありがとうございます。
ご指摘箇所は訂正いたしました。
[…] 編集部あなんの茶のみ話、前回の続きです。1.電池による発電レモンや備長炭で発電できるって、どういうこと?を書いてみようと思います。いろいろ調べてみると、発言者によって言語が少しずつ違う場合があり、素人は混乱します。電子を受け取るとか、電子を放出するとかいいますが、何が何から受け取るの?何がどこへ放出するの?というベタなことを考えながらしか理解できない。中学生向けでは話がはしょられすぎ、高校生向けでは元素記号や式がでてきて複雑すぎ。そんな頭を使ってシンプルに書き出すのに苦労します(複雑になると私学文系脳が拒否反応を起こすんです)。よくあるレモン電池で考えてみます。そもそもレモンの果汁には、いろんなイオン(電荷を帯びた原子)が含まれていて電気をよく通すとのこと。これが世に言う電解質。この電解質にぐさっと刺してあるのが、前回の例ではアルミ板と銅板。別の実験では亜鉛と銅板だったりします。この二つの金属には、どんな違いがあるのでしょう。アルミ版と亜鉛版のセットではダメなんですか。レモンは酸っぱい。この酸で金属が微妙に溶けますよね(アルミなんて、いかにも溶けそう)。金属は、溶けるときにマイナスの電気をもつ電子(電気のもと)を出し、プラスのイオン(電荷を帯びた原子)になります。その「なりやすさ」が金属によって違うんです。これをイオン化傾向って言うんでしたっけ?ですよね。引用 […]