東大塾長の山田です。
このページではダニエル電池について解説しています。
ダニエル電池はボルタ電池の欠点を改善して作られたものです。ダニエル電池の仕組みやボルタ電池との違いを詳しく説明しています。是非参考にしてください。
1. ダニエル電池
亜鉛\(Zn\)板を硫酸亜鉛\(ZnSO_4\)の薄い水溶液に浸したものと、銅\(Cu\)板を硫酸銅(Ⅱ)\(CuSO_4\)の濃い水溶液に浸したものを組み合わせた電池のことをダニエル電池といいます。
ダニエル電池は、ボルタ電池の欠点を改善することによって作られた世界初の実用的な電池です。
まず、ダニエル電池の仕組みについて説明していきましょう。
【ダニエル電池の仕組み】
① イオン化傾向の大きい金属板が溶ける。
まずは、イオン化傾向の大きい金属板が溶けます。亜鉛\(Zn\)と銅\(Cu\)では、イオン化傾向は亜鉛\(Zn\)の方が大きくなります。(イオン化傾向については、「イオン化傾向とは(覚え方・電池・金属と腐食・大きさの表)」の記事で詳しく解説しているので参照してください。)したがって、亜鉛\(Zn\)板が溶け出します。
このとき、亜鉛\(Zn\)が酸化されて亜鉛イオン\(Zn^{2+}\)になり電子を放出します。すなわち、\(Zn\)板は電子を放出する電極(負極)になります。負極で起こっている反応は次のようになります。
\(Zn →Zn^{2+} + 2e^-\)
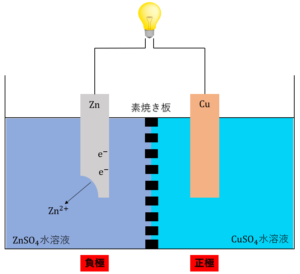
② ①で発生した電子がもう片方の金属板の方へ流れる。
次に、①で発生した電子\(e^-\)が銅\(Cu\)板側に流れ込みます。
このとき、電子が通過することで(電流が発生し)豆電球が点灯します。
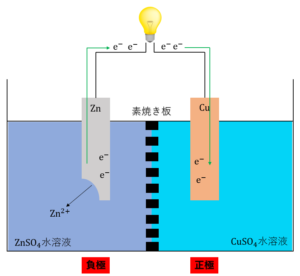
③ 流れてきた\(e^-\)が溶液中のイオン化傾向の小さい陽イオンとくっつく。
銅\(Cu\)板では、電解液中の銅(Ⅱ)イオン\(Cu^{2+}\)が流れてきた電子\(e^-\)を受け取り、還元されて銅\(Cu\)になります。すなわち、\(Cu\)板は電子を受け取る電極(正極)になります。正極で起こっている反応は次のようになります。
\(Cu^{2+} + 2e^- →Cu\)
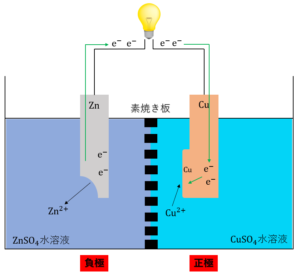
以上①~③がダニエル電池の仕組みです。
ダニエル電池の構成を表す電子式は次のとおりです。
\((-) Zn|ZnSO_4 aq|CuSO_4 aq|Cu (+)\)
また、この電池全体では次の酸化還元反応が起こります。
\(Zn + Cu^{2+} →Zn^{2+} + Cu\)
2. ボルタ電池との違い
ボルタ電池とダニエル電池はともに\(Zn\)板から\(Cu\)板に流れてきた\(e^-\)を水溶液中の陽イオンが受け取ります。しかし、この2つの電池では\(e^-\)を受け取る陽イオンが異なります。
ボルタ電池では、「ボルタ電池とは(仕組み・分極の原理など)」の記事で説明しているように\(Cu\)板に流れてきた\(e^-\)を\(H^+\)が受け取り、還元され\(H_2\)になります。このため、発生した\(H_2\)が\(Cu\)板のまわりに溜まってしまい、電圧が急激に低下してしまうというのが欠点でしたね。
一方で、ダニエル電池では、\(Cu\)板に流れてきた\(e^-\)を水溶液中の\(Cu^{2+}\)が受け取り、\(Cu\)単体を生成します。生成する物質が電極と一緒になるので、くっついても正極で起こる反応には何の影響も与えません。したがって、ダニエル電池は分極を起こすことはなく継続的に電気を得ることができるのです。
3. 素焼き板
ダニエル電池では、正極側と負極側で異なった電解液が用いられ、両電解液は素焼き板で仕切られます。この仕切りには、セロハンやセロハンチューブ、イオン交換膜などを用いることもできます。
素焼き板を使うのは2つの目的があります。
1つ目は、2つの溶液(\(ZnSO_4\)、\(CuSO_4\))が混ざることを防ぐということです。2つの電解液が混ざっては意味がないのでこれは重要ですね。
2つ目は、イオンを透過させることで電荷のバランスを調整するということです。ダニエル電池を使い続けると、正極では次第に\({SO_4}^{2-}\)が、負極では\(Zn^{2+}\)が増加していきます。このとき、正極では\({SO_4}^{2-}\)が増加していくのでマイナスに電荷が偏ります。また、負極では\(Zn^{2+}\)が増加していくのでプラスに電荷が偏ります。
この電荷の偏りを素焼き板が調整します。素焼き板はイオンを通す性質を持っています。これより、\({SO_4}^{2-}\)が素焼き板を通り負極側に、\(Zn^{2+}\)が素焼き板を通り正極側に移動します。これにより、電気的なバランスが整えられるのです。
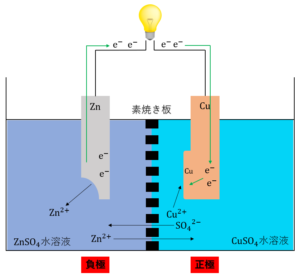
4. 起電力と濃度の関係
ダニエル電池は、電解液の濃度を変化させることで大きな起電力を得ることができます。ダニエル電池を放電すると、負極側の電解液中では\(Zn^{2+}\)が増大し、正極側の電解液中では\(Cu^{2+}\)が減少します。
そのため、負極側の\(ZnSO_4\)水溶液の濃度を低く、正極側の\(CuSO_4\)水溶液の濃度を高くするとより大きな起電力を得ることができるので電流はより長く流れ続けます。
最初から\(Zn^{2+}\)が多く存在すると\(Zn\)板が溶けずらくなってしまうし、\(Cu^{2+}\)が少ないと早い段階で\(Cu^{2+}\)がすべて単体の\(Cu\)になってしまい、それ以上反応が進まなくなるので得られる起電力は小さくなってしまいますよね。
5. まとめ
最後に、ダニエル電池についてまとめておこうと思います。
ボルタ電池‥‥\(Cu\)板に流れてきた\(e^-\)を\(H^+\)が受け取り、還元され\(H_2\)になる。
ダニエル電池‥‥\(Cu\)板に流れてきた\(e^-\)を\(Cu^{2+}\)が受け取り、還元され単体の\(Cu\)になる。
①2つの溶液(\(ZnSO_4\)、\(CuSO_4\))が混ざることを防ぐ。
②イオンを透過させることで電荷のバランスを調整する。
負極側の\(ZnSO_4\)水溶液の濃度を低く、正極側の\(CuSO_4\)水溶液の濃度を高くする。
ボルタ電池との違いは出題されやすいところです。この記事でダニエル電池をマスターするとともにボルタ電池についてもしっかり復習しておくようにしてください!















① イオン化傾向の大きな金属である亜鉛板が溶ける。
② ①で発生した電子がもう片方の金属である銅板の方へ流れる。
③ 流れてきた\(e^-\)が溶液中のイオン化傾向の小さい陽イオンである銅イオンとくっつく。