東大塾長の山田です。
このページでは「化学の基本法則」について解説しています。
具体例を用いながら理解しやすいように説明しているので,ぜひ参考にしてください!
1. 質量保存の法則
「化学反応の前後で物質の総質量は変化しない」という法則を質量保存の法則といいます。
この法則は、1774年にフランスのラボアジエにによって発見されました。
中和や燃焼、熱分解など様々な化学反応がありますが、反応にかかわるすべての物質の質量の和と、反応の結果としてできた生成物の質量の和は常に同じになります。
ここで、水素と酸素による水の生成反応を例に説明します。水素と酸素の反応の化学反応式は下のようになります。
\( \displaystyle 2H_2 + O_2 → 2H_2 O \)
「物質量molの超解説」の記事で説明したように、「化学反応式の係数比=モル比」となります。
つまり、水の生成反応では \( 2mol \) の \( H_2 \) と \( 1mol \) の \( O_2 \) から \( 2mol \) の \( H_2 O \) が生成することを表しています。
ここで、\( 2mol \) の \( H_2 \) と \( 1mol \) の \( O_2 \) が反応して \( 2mol \) の \( H_2 O \) が生成するとしましょう。
\( H_2 \)、\( O_2 \)、\( H_2 O \) の分子量はそれぞれ \( 2〔g/mol〕\)、\( 32〔g/mol〕 \)、\( 18〔g/mol〕 \) であるから、反応物(\( H_2 \),\( O_2 \))の質量の合計は
\( \displaystyle 2[g/mol] \times 2[mol] + 32[g/mol] \times 1[mol] = 36[g] \)
となります。
一方、生成物(\( H_2 O \))の質量の合計は
\( \displaystyle 18[g/mol] \times 2[mol] = 36[g] \)
となります。
これからわかるように、反応物の質量の合計と生成物の質量の合計はともに \( 36g \) となり、質量保存の法則が成り立つことがわかります。
2. 定比例の法則
「同じ化合物であれば、その作られ方によらず、化合物を構成する成分元素の質量比は常に一定である」という法則を定比例の法則といいます。
この法則は、1799年にプルーストによって発見されました。
ここでは、二酸化炭素を例に説明していきましょう。
二酸化炭素は炭素原子 \( C \) 1個と酸素原子 \( O \) 2個で形成されています。
二酸化炭素の質量と二酸化炭素に含まれる炭素の質量の関係をグラフで表すと,次のようになります。
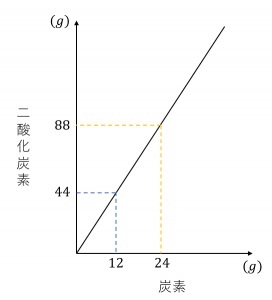
炭素の質量が12の時、二酸化炭素の質量は44になっています。
また、二酸化炭素の質量から炭素の質量を引くと酸素の質量は32とわかります。
ここから、炭素・酸素・二酸化炭素の質量の比は \(「12:32:44」=「3:8:11」\) となります。
次に、炭素の質量が24の時を考えます。
グラフより二酸化炭素の質量は88だとわかります。
二酸化炭素の質量から炭素の質量を引いて、酸素の質量は64とわかります。
ここから、炭素・酸素・二酸化炭素の質量の比は \(「24:64:88」=「3:8:11」\) となります。
二酸化炭素を構成する成分元素(炭素と酸素)の質量が変化しても、質量の組成(比)は常に一定になっています。
また、炭素を燃焼させてできる二酸化炭素も、動物の呼吸中に含まれる二酸化炭素も、炭素と酸素の質量比は3:8になります。
3. 原子説
ドルトンは質量保存の法則や定比例の法則から、物質は最終的に粒からできていると考えました。
そして、物質には最後の最後は分割できない粒があり、その粒こそ原子であるとしたのです。
これが、1803年にドルトンが、質量保存の法則と定比例の法則を説明できる仮説として提唱した原子説です。
原子説とは以下のものです。
ちなみに、上記の③が定比例の法則の説明、④が質量保存の法則の説明になっています。
4. 倍数比例の法則
「A、Bの2元素からなる化合物が2種類以上あるとき、一定量のAと化合しているBの質量はこれらの化合物の間では簡単な整数比が成り立つ」という法則を倍数比例の法則といいます。
この法則は、1803年にドルトンが、原子説の考え方に基づいて倍数比例の法則を予想し、これを実験で確認したことで発見されました。
言葉で言われただけではわかりにくいので、具体例を出して説明しましょう。
例えば、炭素と酸素の化合物には、一酸化炭素と二酸化炭素があります。
この一酸化炭素と二酸化炭素の炭素の質量を \( 12g \) と固定すると、
| 炭素 | 酸素 | |
| 一酸化炭素 | \(12g\) | \(16g\) |
| 二酸化炭素 | \(12g\) | \(32g\) |
すると、酸素の質量は \( 16g \) と \( 32g \) になります。
このように、\( 16g : 32g = 1 : 2 \) と簡単な整数比になります。
これを、倍数比例の法則というのです。
\( CuO \) と \( Cu_2 O \) でも考えてみましょう。
酸素の質量を \( 16g \) と固定すると、
| 酸素 | 銅 | |
| 酸化銅(I) | \(16g\) | \(128g\) |
| 酸化銅(II) | \(16g\) | \(64g\) |
このとき、銅の質量は \( 128g : 64g = 2 : 1 \) という簡単な整数比になります。
4.1 定比例の法則と倍数比例の法則の違い
定比例の法則と倍数比例の法則は名前も似ているし、法則の内容もよく似ていて区別するのが難しいです。
そこで、ここではしっかり区別できるように説明したいと思います。
定比例の法則は「炭素を燃焼させてできる二酸化炭素も、動物の呼吸中に含まれる二酸化炭素も炭素元素と酸素元素の質量比は同じである」ということを表しています。
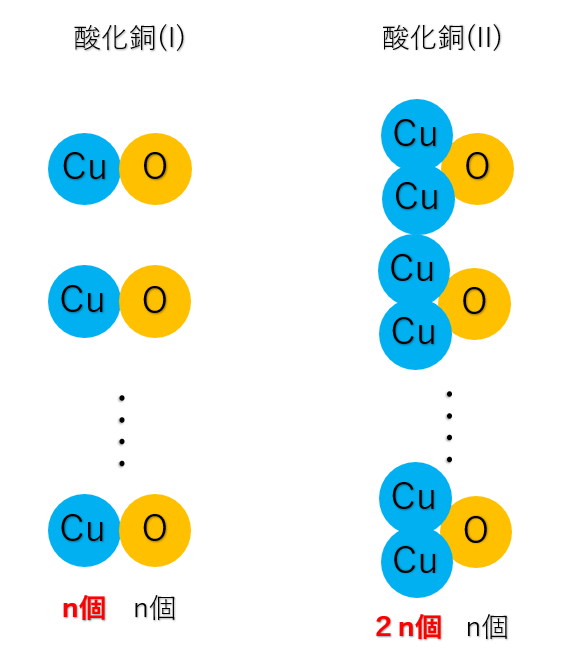
一方、倍数比例の法則は原子の存在を強めるために提唱された法則です。
このように酸素が同じ質量なら、\( CuO \) と \( Cu_2 O \) と化学式で表せるので、\( Cu(II) : Cu(I) = 1 : 2 \) であることは明らかです。
このような2つ区別の仕方は次のようになります。
1種類の化合物の成分元素の質量比を表すのが定比例の法則
2種類以上の化合物の成分元素を比較しているのが倍数比例の法則
定比例の法則は、\( C O_2 \) なら \( CO_2 \) 1種類の \( C : O \) の質量比が同じであると説明しています。
一方、倍数比例の法則は \( CO \) と \( CO_2 \) の2種類の比較を論じています。
これが2つの大きな違いです。しっかり覚えてください。
5. 気体反応の法則
「気体同士が反応したり、反応によって気体が生成するとき、それらの気体の体積の間には簡単な整数比が成り立つ」という法則を気体反応の法則といいます。
この法則は、1808年にゲーリュサックが発見しました。
これは、気体の状態方程式を知っている我々からすると、\( PV = nRT \) のうち \( P \),\( T \) 一定なら \( V = kn \) となるので、体積はモルに比例するので、\( 2H_2 + O_2 → 2H_2 O \) の反応で、体積比が \( 2 : 1 : 2 \) になることは簡単にわかります。
当時ゲーリュサックは原子説でこの法則を説明しようとしましたが、原子説ではこの法則は説明できませんでした。
というのは、水素という原子2個と酸素という原子1個から、水蒸気という複合原子2個を生成させることは、酸素という原子を分割しない限り起こりえないのです。
つまり、原子説では次のような矛盾が生じるのです。
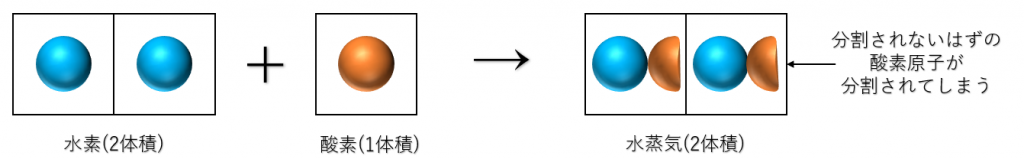
(当時は、\( H \) は陽性の元素であるから、\( H \) 同士がくっついて分子になるなんてありえないと思われていました。同じ元素の物質が化合するとは思われていなくて、当時水素や窒素、酸素は単原子気体だと思われていました。)
上記の気体反応は、次で解説するアボガドロの分子説で説明できます。
アボガドロの分子説では、いくつかの原子が結びついてできている分子の存在を仮定し、化学反応するときには、分子は原子に分割されると考えられます。
つまり、分子説では、次のように矛盾なく説明できるようになります。
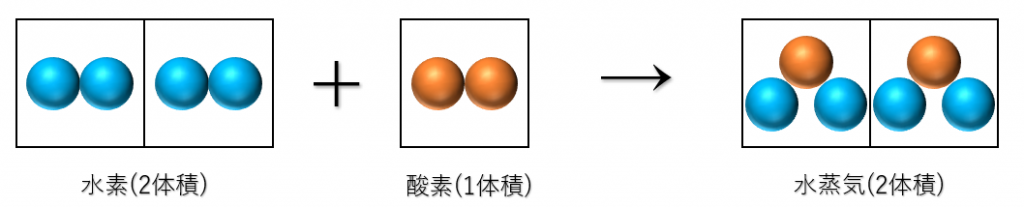
6. 分子説
1811年に、アボガドロが、質量保存の法則、定比例の法則、倍数比例の法則はもとより、気体反応の法則をも説明できる仮説として分子説を提唱しました。
分子説とは以下の通りです。
①それぞれの気体は、何個かの原子が結合した分子という粒子からできている。
②すべての気体は、同温・同圧のとき、同体積中には同数の分子を含む。
分子説の考え方により、上で述べた気体反応の法則と原子説の矛盾がなくなったのです。
【アボガドロの法則】
上記の「②すべての気体は、同温・同圧のとき、同体積中には同数の分子を含む。」は、のちに研究者たちにより正しいことが認められ、現在ではアボガドロの法則として知られています。
標準状態で \( 22.4L \) の気体中には、気体の種類にかかわらず、\( 6.02 \times 10^{23} \) 個の分子が含まれる。
7. まとめ
最後に化学の基礎法則についてまとめておこうと思います。
| 法則名 | 発見者 | 内容 |
|---|---|---|
| 質量保存の法則 | ラボアジエ | 化学反応の前後で物質の総質量は変化しない」という法則を質量保存の法則 |
| 定比例の法則 | プルースト | 同じ化合物であれば、その作られ方によらず、化合物を構成する成分元素の質量比は常に一定である |
| 原子説 | ドルトン |
①すべての物質は、それ以上分割できない最小の粒子から構成されている。その最小の粒子を原子という。 ②同じ元素の原子は質量や性質が同じで、異なる元素の原子はこれらが異なる。 ③化合物は、異なる2種類以上の原子が、一定の割合で結びついてできている。 ④化学変化は原子の組み合わせの変化であり、化学変化の前後でなくなったり新しくうまれたりすることはない。 |
| 倍数比例の法則 | ドルトン | A、Bの2元素からなる化合物が2種類以上あるとき、一定量のAと化合しているBの質量はこれらの化合物の間では簡単な整数比が成り立つ |
| 気体反応の法則 | ゲーリュサック | 気体同士が反応したり、反応によって気体が生成するとき、それらの気体の体積の間には簡単な整数比が成り立つ |
| 分子説 | アボガドロ |
①それぞれの気体は、何個かの原子が結合した分子という粒子からできている。 ②すべての気体は、同温・同圧のとき、同体積中には同数の分子を含む。 |
それぞれの法則の内容と発見した人の名前はよく出題されます。
特にどの法則を誰が発見したのか聞かれる問題は多いです。
また、原子説の矛盾している部分も問われることが多いです。しっかり覚えてください。
この分野は記述問題として出題されることも多いので、自分で説明できるように内容を理解しましょう!















①すべての物質は、それ以上分割できない最小の粒子から構成されている。その最小の粒子を原子という。
②同じ元素の原子は質量や性質が同じで、異なる元素の原子はこれらが異なる。
③化合物は、異なる2種類以上の原子が、一定の割合で結びついてできている。
④化学変化は原子の組み合わせの変化であり、化学変化の前後でなくなったり新しくうまれたりすることはない。