東大塾長の山田です。
このページでは中和滴定について解説しています。
中和滴定の基礎的な知識から二段階滴定、逆滴定などの少し難しい知識まで幅広く説明しています。是非参考にしてください。
1. 中和滴定
「塩の加水分解」の記事で説明した中和反応を用いて、酸や塩基の濃度や物質量を求める操作のことを中和滴定といいます。また、酸と塩基が過不足なく反応する点(中和の完了点)のことを中和点、指示薬の変色から判断して滴定を終えた点のことを終点といいます。
中和滴定は次の手順で行います。
①濃度が不明の酸(塩基)の水溶液をホールピペットを用いて、一定の体積だけコニカルビーカーに量り取ります。さらに、ビーカーの中の水溶液に少量の指示薬を加えます。
②これに、濃度がわかっている塩基(酸)の水溶液をビュレットから少しずつ滴下して加えていきます。
③ちょうど中和するまで(指示薬が変色するところ)加えたら、中和点までに加えた塩基(酸)の水溶液の体積を読み取ります。この実験の結果を2で解説する式に代入することで、酸(塩基)の水溶液の濃度が求まります。
2. 中和滴定における量の関係式
酸と塩基の中和反応は、\(H^++OH^-→H_2O\)です。これより、酸と塩基が過不足なく中和反応するには、次の関係式が成り立ちます。
\(酸の出す水素イオンH^+の物質量=塩基の出す水酸化物イオンOH^-の物質量\)
これは、酸の物質量と塩基の物質量が等しいのではなく、水素イオンの物質量と水酸化物イオンの物質量が等しいのです。上の関係式を酸や塩基の価数を使って表すと、
\(酸の価数 \times 酸の物質量=塩基の価数 \times 塩基の物質量\)
この式は次のようにも表すことができます。
\(酸の価数 \times 酸のモル濃度 \times 体積=塩基の価数 \times 塩基のモル濃度 \times 体積\)
すなわち、モル濃度\(C〔mol/L〕\)、体積\(V〔mL〕\)、\(a\)価の酸とモル濃度\(C’〔mol/L〕\)、体積\(V’〔mL〕\)、\(b\)価の塩基が過不足なく中和したとするとき、次の関係式が成り立ちます。
\(\displaystyle a \times C \times \frac{V}{1000}=b \times C’ \times \frac{V’}{1000}\)
これが中和滴定の際に用いる関係式です。
3. 中和滴定で用いる器具
ここでは、中和滴定を行うときに用いる器具について説明します。
| 器具の名称 | ホールピペット | ビュレット |
| 形状 | 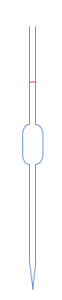 |
 |
| 用途 | 少量の液体を一定の体積(例えば、\(10mL\)、(\(20mL\)など)だけ正確に量り取るための器具 | 液体を少しずつ滴下し、滴下した液体の体積を正確に量るための器具 |
| 器具の名称 | メスフラスコ | コニカルビーカー |
| 形状 | 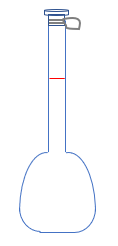 |
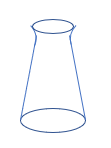 |
| 用途 | 液体を一定の体積(例えば、\(100mL\)、(\(200mL\)など)だけ量るための器具 | この中に酸(塩基)の水溶液を入れ、それにビュレットから塩基(酸)の水溶液を加えて、中和反応をさせるための器具 |
【洗浄方法】
これら4つの器具の洗浄方法には2通りあります。
①共洗いを用いる。
これから使用する水溶液で内部(内壁)を数回洗ってから用いる洗浄方法を共洗いといいます。共洗いで洗浄するのは、ホールピペットとビュレットです。
純水で洗った後、残った純水により使用する水溶液の濃度が薄まることを避けるために共洗いを行います。共洗い後はぬれたまま使って構いません。
②純水で洗う。
メスフラスコとコニカルビーカーは純水で洗浄します。
メスフラスコにはあとから純水が加えられるため、純水が残っていても問題ありません。また、コニカルビーカーは一定量の溶質が量り取られるので、濃度が薄まっても滴下量に変化はなく滴定の結果には影響を与えません。
【乾燥方法】
ホールピペット、ビュレット、メスフラスコは乾燥させるときに加熱乾燥してはいけません。体積を正確に量るガラス器具は、熱膨張による変形を避けるため加熱乾燥はしません。
一方で、コニカルビーカーは体積を正確に量るガラス器具ではないので、加熱乾燥しても大丈夫です。
4. 滴定曲線
4.1 滴定曲線と指示薬
加えた酸(塩基)の水溶液の滴下量(体積)と、混合水溶液のpHの変化の関係を、滴下量を横軸、pHを縦軸に取り表した曲線のことを滴定曲線といいます。
滴定曲線は、中和点付近でpHが大きく変化します。これは、中和点付近では、滴下したわずかな酸や塩基がpHに大きな影響を与えるからです。
中和滴定で用いる標準溶液や試料はともに無色であることが多いです。そのため、単に滴定をしただけではどこが中和点であるのか目で見て判断することができません。そこで、特定のpHで色が変化する物質である指示薬を用いて、中和が完了したのかを確認します。
また、滴定曲線はpHが急激に大きく変化する範囲が異なります。(詳しい曲線は以下で説明します。)中和滴定では、その指示薬として、曲線の垂直部分に変色域をもつ指示薬を選びます。
では、高校化学でよく用いられる指示薬を2つ紹介していきます。
4.1.1 フェノールフタレイン
フェノールフタレインの変色域は、だいたい\(pH8.3~pH10\)です。これより、pHがこの範囲より酸性側であれば無色、塩基性側だと赤色に変色します。
4.2.2 メチルオレンジ
メチルオレンジの変色域は、だいたい\(pH3.1~pH4.4\)です。これより、pHがこの範囲より酸性側であれば赤色、塩基性側だと黄色に変色します。
中和滴定をするときには、中和点がどこになるかを考慮してどちらかの指示薬を選択します。実際に、どちらにすればいいか解説していきましょう。
4.2 強酸と強塩基の中和の滴定曲線
まず、強酸と強塩基による中和について考えてみましょう。例として、強酸が\(HCl\)、強塩基が\(NaOH\)の時を考えます。強酸の水溶液に強塩基の水溶液を加えていった滴定では、中和点は中性を示します。(これは、生成した塩の液性を考えればわかります。詳しくは、「塩の加水分解」の記事を参照してください。)
中和点の直前では、塩酸がわずかに残っていると水溶液は酸性を示します。一方で、中和点を過ぎ、水酸化ナトリウムがわずかに過剰に加えられたときは水溶液は塩基性を示します。これからわかるように、中和点付近ではpHの値は大きく変化します。これらを考慮して作った滴定曲線は次のようになります。
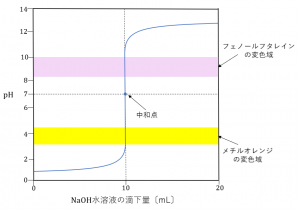
この図を見てわかるように、強酸と強塩基の中和の中和点の前後で、フェノールフタレインの変色域とメチルオレンジの変色域をどちらも通過しています。これより、この実験では、どちらの指示薬も用いることができます。
一般に、強酸の水溶液と強塩基の水溶液の中和滴定では、指示薬にフェノールフタレインもメチルオレンジも使うことができます。
4.3 弱酸と強塩基の中和の中和滴定
次に、弱酸と強塩基による中和について考えましょう。例として、弱酸が\(CH_3COOH\)、強塩基が\(NaOH\)の時を考えます。弱酸の水溶液に強塩基の水溶液を加えていった滴定では、中和点は塩基性を示します。
中和点を過ぎ、水酸化ナトリウムがわずかに過剰に加えられたときは水溶液は塩基性を示します。中和点付近ではpHの値は塩基性側にかたよった範囲で大きく変化します。これらを考慮して作った滴定曲線は次のようになります。
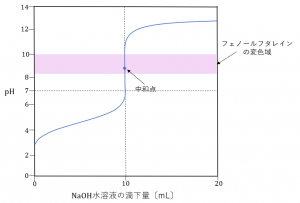
この図を見てわかるように、弱酸と強塩基の中和の中和点の前後で、フェノールフタレインの変色域を通過しています。これより、この実験では、フェノールフタレインを用いることができます。
一般に、弱酸の水溶液と強塩基の水溶液の中和滴定では、指示薬にフェノールフタレインを使います。
4.4 弱塩基と強酸の中和の中和滴定
最後に、弱塩基と強酸による中和について考えましょう。例として、弱塩基が\(NH_3\)、強酸が\(HCl\)の時を考えます。弱塩基の水溶液に強酸の水溶液を加えていった滴定では、中和点は酸性を示します。
中和点を過ぎ、塩酸がわずかに過剰に加えられたときは水溶液は酸性を示します。中和点付近ではpHの値は酸性側にかたよった範囲で大きく変化します。これらを考慮して作った滴定曲線は次のようになります。
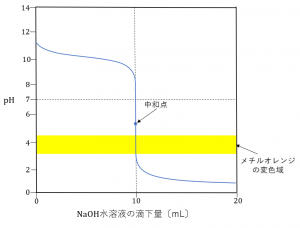
この図を見てわかるように、弱塩基と強酸の中和の中和点の前後で、メチルオレンジの変色域を通過しています。これより、この実験では、メチルオレンジを用いることができます。
一般に、弱塩基の水溶液と強酸の水溶液の中和滴定では、指示薬にメチルオレンジを使います。
5. 二段階滴定
2価の酸や塩基には、中和点が2つ存在します。このことを利用した中和滴定を二段階滴定といいます。以下では、具体的な例を用いて解説していきます。
5.1 炭酸ナトリウム\(Na_2CO_3\)の塩酸\(HCl\)による二段階滴定
炭酸ナトリウム\(Na_2CO_3\)は、1価の強塩基である水酸化ナトリウムと2価の弱酸である炭酸の正塩で、その水溶液は比較的強い塩基性を示します。そのため、この水溶液は塩酸などの強酸と中和反応します。この\(Na_2CO_3\)水溶液と塩酸の中和反応は、次式のように2段階で起こります。
\(Na_2CO_3+HCl→NaCl+NaHCO_3‥‥①\)
\(NaHCO_3+HCl→NaCl+H_2O+CO_2‥‥②\)
この中和滴定の滴定曲線は以下のようになります。
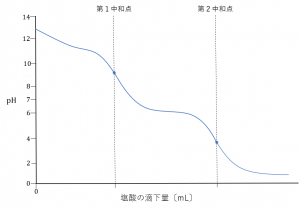
まず、滴定を開始してから第一中和点に達するまで(第一段階)の反応を考えましょう。ここでは、上で示した①式の反応が起こっています。
炭酸ナトリウム\(Na_2CO_3\)は、一気に炭酸\(H_2CO_3\)になるのではなく、一旦炭酸水素ナトリウム\(NaHCO_3\)に変化します。このように、炭酸ナトリウムは段階的に中和されます。
また、強塩基性の水溶液に強酸を加えているので中和点は\(pH=7\)付近になると予想できますが、この滴定では\(NaHCO_3\)が生じ、水溶液中で電離して弱塩基性を示すの若干塩基性になります。したがって、第一中和点はフェノールフタレインの変色で判断することができます。
次に、第一中和点から第二中和点に達するまで(第二段階)の反応を考えましょう。ここでは、上で示した②式の反応が起こっています。
第二段階では、第一段階で生じた\(NaHCO_3\)が反応します。このとき生成する\(H_2CO_3\)はすぐに\(H_2O\)と\(CO_2\)に分離します。また、弱塩基性の水溶液に強酸を加えているので中和点の\(pH\)は酸性にかたよります。したがって、第二中和点はメチルオレンジの変色で判断することができます。
では、この反応の量的な関係を考えましょう。最初に\(Na_2CO_3\)が\(a〔mol〕\)あったとします。第一段階では、次のように反応し、\(a〔mol〕\)の\(HCl\)が消費され、\(a〔mol〕\)の\(NaHCO_3\)が生成します。
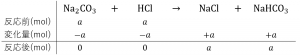
また、第二段階では次のように反応し、\(a〔mol〕\)の\(HCl\)が消費されます。
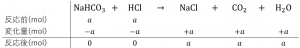
これより、第一段階で消費する\(HCl\)の物質量と第二段階で消費する\(HCl\)の物質量は等しいということがわかります。
5.2 水酸化ナトリウム\(NaOH\)と炭酸ナトリウム\(Na_2CO_3\)混合水溶液の塩酸\(HCl\)による二段階滴定
水酸化ナトリウム\(NaOH\)は1価の強塩基です。また、炭酸ナトリウム\(Na_2CO_3\)は、5.1で説明したようにその水溶液は比較的強い塩基性を示します。そのため、この混合水溶液は塩酸などの強酸と中和反応します。この混合水溶液と塩酸の中和反応は、次式のように2段階で起こります。
\(NaOH+HCl→NaCl+H_2O‥‥③\)
\(Na_2CO_3+HCl→NaCl+NaHCO_3‥‥④\)
\(NaHCO_3+HCl→NaCl+H_2O+CO_2‥‥⑤\)
この中和滴定の滴定曲線は以下のようになります。
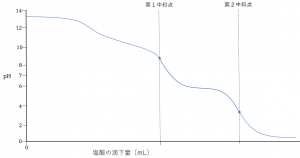
まず、滴定を開始してから第一中和点に達するまで(第一段階)の反応を考えましょう。ここでは、上で示した③式と④式の反応が起こっています。
炭酸ナトリウムは5.1と同様に反応します。
ちなみに、第一段階では④式の反応よりも③式の反応が先に起こります。これは、\(NaOH\)が電離して生じる\(OH^-\)と\(Na_2CO_3\)が電離して生じる\({CO_3}^{2-}\)を比較したときに、\(OH^-\)の方が\(H^+\)を受け取りやすいからです。
③式の反応がほぼ終了してから、④式の反応が始まりますが、③式の反応の終了時点ではpHの変化はごくわずかでその変化は滴定曲線上には描かれません。
では、この反応の量的な関係を考えましょう。最初に\(Na_2CO_3\)が\(a〔mol〕\)、\(NaOH\)が\(b〔mol〕\)あったとします。第一段階では、次のように反応し、\(a+b〔mol〕\)の\(HCl\)が消費され、\(a〔mol〕\)の\(NaHCO_3\)が生成します。
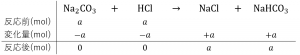
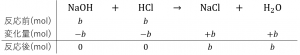
第一中和点は、フェノールフタレインの変色で判断することができます。
また、第二段階では次のように反応し、\(a〔mol〕\)の\(HCl\)が消費されます。

第二中和点は、メチルオレンジの変色で判断することができます。
これより、第一中和点までに用いた\(HCl\)の物質量(\(a+b〔mol〕\))と第一中和点から第二中和点までに用いた\(HCl\)の物質量(\(a〔mol〕\))がわかれば、\(NaOH\)の物質量と\(Na_2CO_3\)の物質量が求まることがわかります。
6. 逆滴定
気体(\(NH_3やCO_2\))や固体(\(CaCO_3\))など、通常の中和滴定を行いにくい物質を滴定するための特殊な滴定方法を逆滴定といいます。
6.1 逆滴定の手順
ここでは、逆滴定の流れについて説明していきます。例として、アンモニア\(NH_3\)を用います。
まず、酸である硫酸\(H_2SO_4\)(塩酸\(HCl\)でもよい)を大量に用意します。
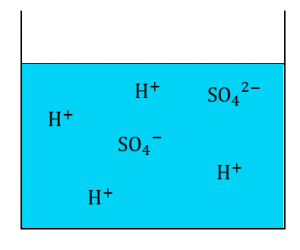
ここにアンモニア\(NH_3\)を完全に吸収させます。
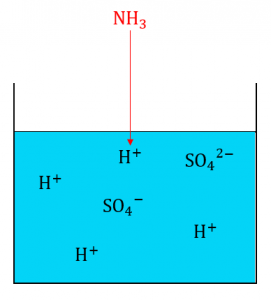
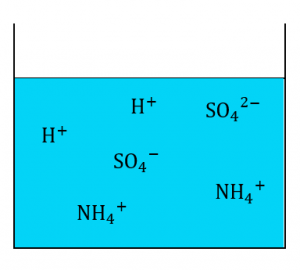
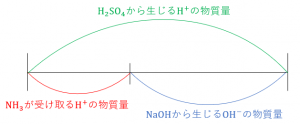
すると、\(NH_3\)は水中に存在する\(H^+\)の一部と反応し\({NH_4}^+\)が生成します。ここに指示薬(メチルオレンジまたはメチルレッド)を入れ、\(NH_3\)と反応しなかった\(H^+\)を水酸化ナトリウム\(NaOH\)で滴定します。
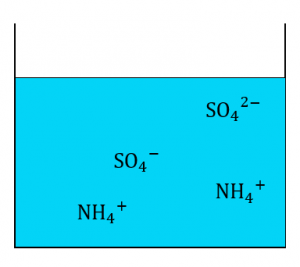
上図が完全に中和した状態です。\(H^+\)はすべて\(OH^-\)と合わさり水になります。
これより、量がわかっている\(H_2SO_4\)と\(NaOH\)から\(NH_3\)の物質量を求めることができます。
6.2 アンモニアの逆滴定
アンモニアの逆滴定について説明していきます。
まず、気体である物質量\(x〔mol〕\)のアンモニアを、濃度\(M〔mol/L〕\)、体積\(V〔mL〕\)の希硫酸に通し、希硫酸中にアンモニアを完全に吸収させます。
\(H_2SO_4+2NH_3→(NH_4)_2SO_4‥‥⑥\)
次に、アンモニアと反応せずに残った硫酸を、濃度\(M’〔mol/L〕\)の水酸化ナトリウムで滴定します。その時の水酸化ナトリウムの滴下量は\(V’〔mL〕\)とします。
\(H_2SO_4+2NaOH→Na_2SO_4+2H_2O‥‥⑦\)
この滴定には、指示薬にメチルオレンジまたはメチルレッドを使います。指示薬にフェノールフタレインを用いると、変色が起こるまでに⑥式で生成した\((NH_4)_2SO_4\)が\(NaOH\)と反応し、正しい滴定ができなくなってしまうので用いることができません。
これより、この逆滴定において求められる関係式は次のようになります。
\(\displaystyle 2 \times M \times \frac{V}{1000}=1 \times M’ \times \frac{V’}{1000} + 1 \times x\)
6.3 二酸化炭素の逆滴定
二酸化炭素の逆滴定について説明していきます。
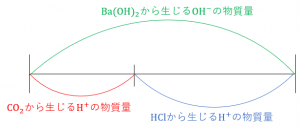
まず、気体である物質量\(y〔mol〕\)の二酸化炭素を、濃度\(M〔mol/L〕\)、体積\(V〔mL〕\)の水酸化バリウム水溶液に通し、水酸化バリウム水溶液中に二酸化炭素を完全に吸収させます。
\(Ba(OH)_2+CO_2→BaCO_3+H_2O‥‥⑧\)
次に、二酸化炭素と反応せずに残った水酸化バリウムを、濃度\(M’〔mol/L〕\)の塩酸水溶液で滴定します。その時の塩酸水溶液の滴下量は\(V’〔mL〕\)とします。
\(Ba(OH)_2+2HCl→Ba(Cl)_2+2H_2O‥‥⑨\)
この滴定には、⑧式が反応した後の反応液の上澄みを用い、指示薬にフェノールフタレインを使います。沈殿\(BaCO_3\)を残したまま、指示薬にメチルオレンジやメチルレッドを用いると、変色が起こるまでに⑧式で生成した\(BaCO_3\)が\(HCl\)と反応し、正しい滴定ができなくなってしまうので用いることができません。
これより、この逆滴定において求められる関係式は次のようになります。
\(\displaystyle 1 \times M’ \times \frac{V’}{1000} + 2 \times y = 2 \times M \times \frac{V}{1000}\)
7. 例題
これまでに解説してきたことに関する例題を紹介します。
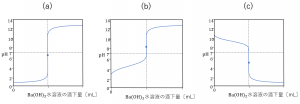
\(0.20 mol/L\)の塩酸\(10 mL\)に\(0.05 mol/L\)の水酸化バリウムを滴下して中和した。完全に中和するのに必要な水酸化バリウムは\(何mL\)になるか求めよ。また、この反応の滴定曲線を表しているのは以下の(a)~(c)のどのグラフか答えよ。
【解答1】
塩酸と水酸化バリウムの化学式を考えると、それぞれ\(HCl\)、\(Ba(OH)_2\)です。これより、塩酸は1価、水酸化バリウムは2価であることがわかるので求める水酸化バリウムの体積を\(x mL\)とすると、
\(\begin{align}
\displaystyle 1 \times 0.20 \times \times \frac{10}{1000} & = 0.05 \times 2 \times \frac{x}{1000} \\
\\
x & =20
\end{align}\)
また、塩酸は強酸、水酸化バリウムは強塩基です。よって、強酸と強塩基の中和滴定を表す滴定曲線を選べばいいので答えは(a)になります。
答‥20〔mL〕、(a)
炭酸ナトリウム\(Na_2CO_3\)と水酸化ナトリウム\(NaOH\)の混合溶液がある。まず、混合溶液\(25 mL\)にフェノールフタレインを加え、\(0.20 mol/L\)の塩酸で滴定したところ終点までに\(20 mL\)の塩酸を要した。次に、この滴定後にメチルオレンジを加え、同じ塩酸で滴定したところ終点までにさらに\(5 mL\)の塩酸を要した。最初の時点で混合溶液に含まれている炭酸ナトリウム、水酸化ナトリウムのモル濃度を求めよ。
【解答2】
まず、問題文から第一段階で要した塩酸は\(20 mL\)、第二段階で要した塩酸は\(5 mL\)であることがわかります。
第一段階では、次の2つの反応
\(NaOH+HCl→NaCl+H_2O\)
\(Na_2CO_3+HCl→NaCl+NaHCO_3\)
第二段階では、次の反応が起こっています。
\(NaHCO_3+HCl→NaCl+H_2O+CO_2\)
ここで、最初の時点で混合溶液に含まれている\(Na_2CO_3\)、\(NaOH\)のモル濃度をそれぞれ\(C_1\)、\(C_2\)とします。
第二段階で要した塩酸の体積が\(5 mL\)であったことから、第一段階で要した塩酸が水酸化ナトリウムと炭酸ナトリウムのそれぞれどちらにどれだけ使われたかを考えると、炭酸ナトリウムの中和に用いられた体積は第二段階で要した塩酸の体積と等しいから\(5 mL\)となります。よって、第一段階の水酸化ナトリウムの中和に用いられた塩酸の体積は\(15 mL\)となります。
したがって、炭酸ナトリウムと塩酸の中和、水酸化ナトリウムと塩酸の中和、それぞれの反応に関する関係式は次のようになります。
\(\displaystyle 1 \times 0.20 \times \frac{15}{1000} = 1 \times C_1 \times \frac{25}{1000}\)
\(\displaystyle 1 \times 0.20 \times \frac{5}{1000} = 1 \times C_2 \times \frac{25}{1000}\)
これより、\(C_1=0.12 mol/L\)、\(C_2=0.040 mol/L\)となります。
答‥炭酸ナトリウムのモル濃度:0.12〔mol/L〕、水酸化ナトリウム:0.040〔mol/L〕
\(0.30 mol/L\)の水酸化バリウム水溶液\(150 mL\)に、二酸化炭素\(CO_2\)を吸収させた。その後、\(0.60 mol/L\)の水酸化ナトリウム水溶液で滴定したところ\(50 mL\)滴下したところで色が変化した。水酸化バリウム水溶液に溶かした\(CO_2\)の物質量を求めよ。
【解答3】
溶かした\(CO_2\)の物質量を\(x mol\)とします。6.3で説明した二酸化炭素の逆滴定の関係式に問題文の値を代入すると、
\(\begin{align}
\displaystyle 1 \times 0.60 \times \frac{50}{1000}+ 2 \times x & = 2 \times 0.30 \times \frac{150}{1000}\\
\\
& = 0.030
\end{align}\)
答‥0.030〔mol〕
8. まとめ
最後に中和滴定についてまとめておこうと思います。
モル濃度\(C〔mol/L〕\)、体積\(V〔mL〕\)、\(a\)価の酸とモル濃度\(C’〔mol/L〕\)、体積\(V’〔mL〕\)、\(b\)価の塩基が過不足なく中和したとする。
\(\displaystyle a \times C \times \frac{V}{1000}=b \times C’ \times \frac{V’}{1000}\)
| 中和する酸と塩基の強弱 | 中和した水溶液の液性 | 用いる指示薬 |
| 強酸と強塩基 | 中性 | フェノールフタレイン、メチルオレンジ |
| 強酸と弱塩基 | 酸性 | メチルオレンジ |
| 弱酸と強塩基 | 塩基性 | フェノールフタレイン |
中和滴定は単純な計算から二段階滴定や逆滴定のように少し複雑な計算まで様々なものがあります。しかし、反応式を書きそれぞれの分子がどのような量的関係で反応しているかがわかれば難しくはありません。
この記事に書いてあることをしっかり理解していれば、自分で問題を解くときにも困ることはなくなると思います。
この記事を何度も読み返しマスターして、多くの問題を解き身に付けてください。















問2番逆じゃないですか?
>ホールピペット、ビュレット、メスフラスコは乾燥させるときに加熱乾燥してはいけません。体積を正確
>に量るガラス器具は、熱膨張による変形を避けるため加熱乾燥はしません。
これと同様の言説は、よく目にします。しかし、「加熱」とは具体的に何℃以上のことなのかを具体的に示したものは殆どありません。実際にラボで使用される計量用ガラス器具は今やホウケイ酸ガラスが頬とんどであり、この種の耐熱ガラスの熱膨張は100℃にしても極めて低く、歪点に至っては500℃以上です。
東京都立産業技術研究センターから出ている報文「ガラス製全量フラスコの精確性に及ぼす加熱の影響」では、250℃の加熱乾燥と放冷を5回繰り返しても、JISの規格を逸脱してしまうような体積変化は起こらなかったことが記載されています。
・加熱乾燥不可派は具体的データや条件を示さず言説を繰り返す。言い伝えを好む。
・加熱乾燥可派はデータと条件を提示して論拠とする。
勿論、文科省下の学習指導要領は現実的なサイエンスでは無く権力機構によるものなので、入試は入試、現実は現実と考え方を切り替えるのがお利巧なのかもしれない。
しかし、日本が科学立国の立場を失い先進国でも無くなった現実を考えると、データに基づいて修正を加えるという科学的方法論が失われてきたことが「乾燥温度」の例からも伺えると思う。
しょうもないとこで
突っかかってるところからも伺えるよね笑笑
人の粗探ししてるのも良いけど
伝え方とかの表現をもっと学んだら?
ガラスなんかより人としてのあり方を学ぶべきだと思うよ
問題3ですが、水酸化ナトリウムで滴定できますか?