東大塾長の山田です。
このページでは「金属結合」について解説しています。
金属結合は共有結合、イオン結合とは少し違った結合をとり、金属特有の特徴があったりするのでしっかりマスターしてください。
1. 金属結合
金属結合は「金属元素と金属元素」の間の結合のことをいいます。
ここでは、ナトリウムを例に説明したいと思います。
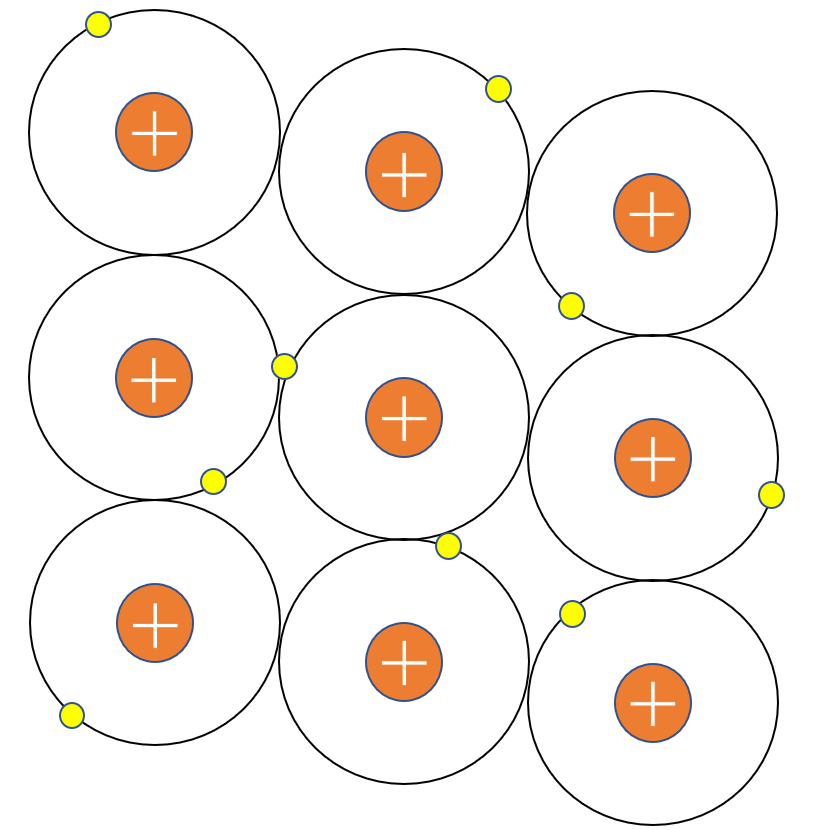
\({\rm Na}\)原子が下の図のように並んでいるとします。
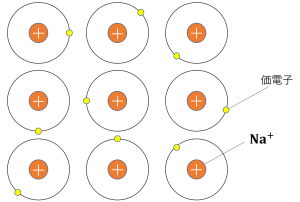
金属元素は第一イオン化エネルギーが小さく陽イオンになりやすくなります。(詳しくは「イオン化エネルギーと電子親和力まとめ」の記事を参照してください。)
\({\rm Na}\)の結晶を考えてみると、1個の\({\rm Na}\)原子のまわりには8個の\({\rm Na}\)原子が隣接していますが、これらの原子の最外殻軌道には余裕があります。
また、\({\rm Na}\)原子の1個の価電子は離れやすいことから、特定の原子に固定されずにまわりの他の原子の軌道を自由に動きまわり、いくつかの原子に共有されます。
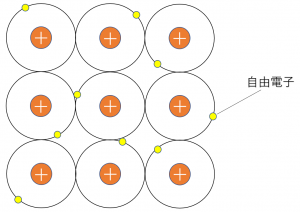
したがって、\({\rm Na}\)原子は価電子を放出した形の\({\rm Na^+}\)になるとともに、まわりの原子と価電子を互いに共有し合います。
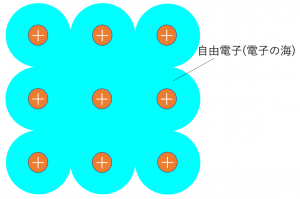
これは、電子の海に原子(イオン)が存在する状態ともいえます。
このような結合を金属結合といい、このときの固定されていない価電子のことを自由電子といいます。
2. 金属結合の特徴
続いて、金属結合の特徴について解説していきます。
2.1 金属結合の結合の強さ
まず、覚えておいてほしいことが1つあります。
例えば、共有結合は
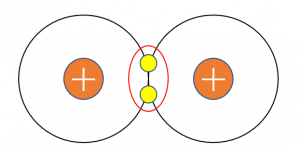
このように、共有結合は+と-の電気的な引力で結合しています。
したがって、共有結合にとって共有電子対(電子)はとても重要です。
次にイオン結合は
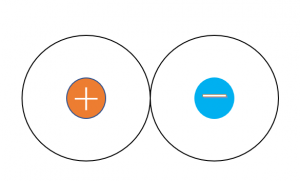
このように、陽イオンと陰イオンで、+と-がお互いに引き合います。
しかし、イオンとして存在することが出来るため共有結合より結合は弱くなります。
最後に金属結合です。

金属結合は、金属元素が陽イオンになりたがり、まわりの原子と価電子を互いに共有しあうと説明しました。
つまり、他のものよりも+-の関係が重要ではなくなります。
したがって、一番電子の重要度が小さくなります。
金属結合は化学結合(共有結合、イオン結合)の中で最も弱い結合になります。
また、水素結合やファンデルワールス力のような分子間力による結合は結合の中では基本的にかなり弱くなります。
特にファンデルワールス力はダントツで弱いです。(水素結合とファンデルワールス力についてはそれぞれ「水素結合とは(水などの例・沸点・エネルギー・距離と強さの比較)」、「ファンデルワールス力と状態方程式」の記事を参照してください。)
よって、結合の大きさは次のようになります。
共有結合>イオン結合>金属結合>分子間力による結合(水素結合、ファンデルワールス力)
2.2 金属結合と組成式
金属結合によって作られた物質は、金属イオンの数を最も簡単な整数比にした組成式というものを使って表します。(組成式の詳しい説明については「イオン結合とは(例・結晶・共有結合との違い・半径)」の記事を参照してください。)

金属はイオンが無限に繋がることによって作られているので組成式を使いますが、基本的に「単体」なので、イオン結合のときとは違い構成イオンの比については考える必要がありません。
3. 金属の性質
先ほど説明した自由電子はその名の通り自由に動き回ることが出来ます。
金属は、この電子の自由性を要因とする性質をもっています。ここでは、その性質について説明します。
3.1 電気伝導性
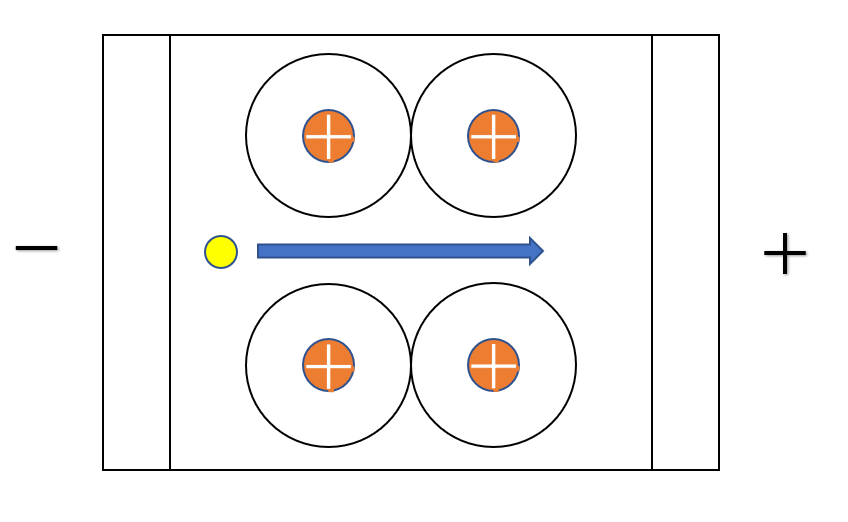
金属中を自由電子が移動することで電気のエネルギーが伝えられるので、金属は電気をよく通します。
これは、金属の自由電子が電圧が加わることにより、正極側に移動するからです。このように電子が流れることで電子と逆方向に電流が流れます。
また、「金、銀、銅、アルミニウム、鉄」の電気の伝えやすさについて聞かれる問題が出題されることがあるので伝えやすさの順番を覚えておいてください。
電気を伝えやすい順番に並べると
銀、銅、金、アルミニウム、鉄
となります。
銀は電気や熱を最も伝えやすい金属として有名です。
金は銀、銅と合わせて電気を通しやすいです。一方で鉄は金属の中では電気を通しにくい部類に入ります。
銅は導線など身近な道具で使われることが多いため、銅が一番電気を通しやすいと思いがちです。しかし、実際には銀が一番電気を通しやすくなります。
センター試験などでもこのことについて問われることがあるのでしっかり覚えてください。
3.2 熱伝導性
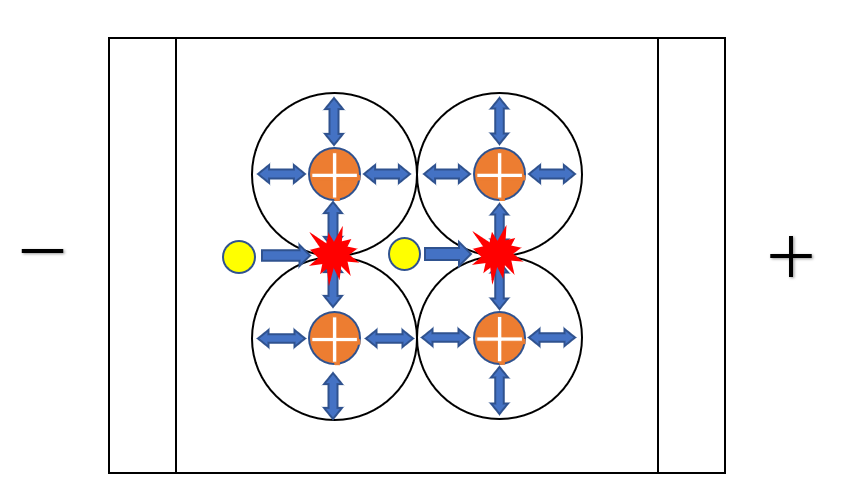
金属は熱伝導性が非常に高くなります。その理由は以下のようになります。
まず、熱すると原子が熱振動をします。これにより、それまで簡単に移動できていた自由電子が原子の運動によって、移動を邪魔され衝突します。
衝突することで原子の運動エネルギーを電子が受けて熱振動します。よって、まだ温まっていない低温部分にも自由電子によって振動が伝えられるので熱を伝えやすいのです。
3.3 光沢(金属光沢)がある
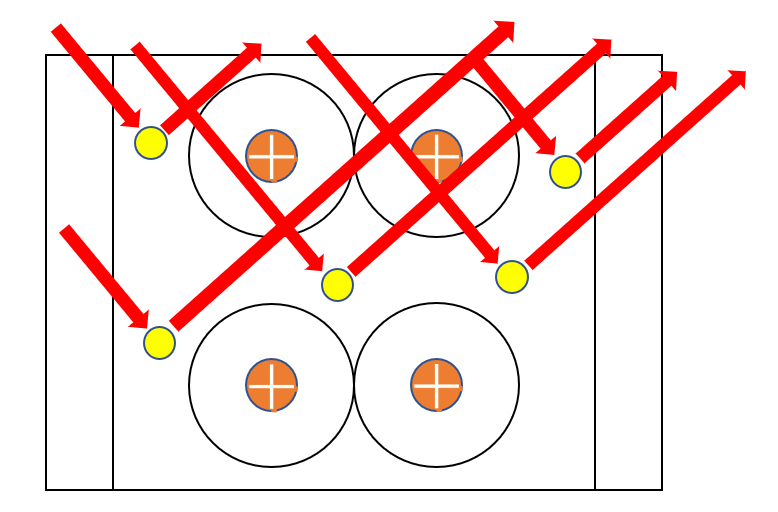
自由電子は光を反射します。
この性質により、金属は(光を反射するので)光沢をもっているように見えるのです。
3.4 展性・延性に富む
鉄をたたくと延びて広がるように、金属はたたくと薄く広がる性質と引っ張ると延びる性質をもっています。
たたくと薄く広がる性質を展性、引っ張ると延びる性質を延性といいます。
自由電子が陽イオンの位置に合わせて移動して結合を保とうとするのです。
4. まとめ
最後に金属結合についてまとめておこうと思います。
- 金属結合は「金属元素と金属元素」の間の結合のことをいう。
- まわりの原子と価電子を互いに共有し合うような結合を金属結合といい、固定されていない価電子のことを自由電子という。
- 結合の大きさは、共有結合>イオン結合>金属結合>分子間力による結合(水素結合、ファンデルワールス力)となる。
- 金属結合によって作られた物質は、金属イオンの数を最も簡単な整数比にした組成式というものを使って表します。
- 金属は電気、熱をよく通す。
- 金属は光沢がある。
- 金属は展性・延性をもつ。
以上が金属結合についてのまとめです。
金属結合は共有結合、イオン結合とともに大事なところです。
共有結合とイオン結合とは結合の仕方が少し違うのでしっかり理解しましょう!
金属の結晶については「金属結晶まとめ」の記事で詳しく解説するのでそちらを参照してください。















原子核にとって電子が重要であればあるほど結合は強くなる。