東大塾長の山田です。
このページでは、「同位体と同素体」について解説しています。
- 「同位体と同素体の違いは?」
- 「同素体って、例えば何があるの?」
といった疑問がすべて解決できるように、すべて解説しています。
同位体と同素体は混同しやすく間違いやすいので、問題になりやすいところです。
しかし、しっかり理解すれば違いは明らかなので絶対に間違えることはないと思います。
ぜひ、参考にしてください!
1. 同位体とは?
まずは同位体について解説します。
1.1 同位体の定義
同位体は陽子の数(原子番号)が同じで、中性子の数が異なる元素同士のことをいいます。
同位体は化学的性質(反応性など)にはあまり変化が見られません。
同位体の例として水素があります。
水素には、天然に下の図のように3つの同位体があります。(下の図において、青丸は陽子、赤丸は中性子、黄色の丸は電子を表しています。)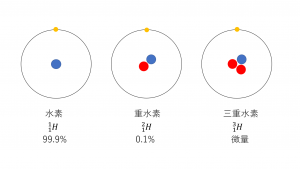
1.2 同位体の存在比
上の水素を見てわかるように、同位体は存在比が違っています。
そのため、同位体の存在比の計算問題が出題されることがあります。
例えば、塩素には質量数が35のものと37のものが存在し、それぞれ存在比は35のものは75%、37のものは25%となります。
よって、塩素の原子量は35×0.75+37×0.25=35.5となります。
このように、同位体が存在する原子の原子量は平均値で表されます。
上で示した水素は質量数1のものの存在比が99.9%と大きいので、原子量は1となります。
1.3 放射性同位体
同位体の中には原子核が不安定で放射線を出しながら崩壊(壊変)していくものがありこのような同位体のことを放射性同位体といいます。
放射性同位体は遺物の年代測定や医療などに利用されます。
2. 同素体とは?
次は同素体についての解説です。
2.1 同素体の定義
同じ元素からなる単体で化学的性質(反応性など)が異なる物質同士を互いに同素体といいます。
例として、酸素とオゾンが挙げられます。
この2つはどちらも同じ「O」という元素からできてるけれど、色や臭いなどの化学的性質は異なります。
この性質の違いは、結合の形や数によるものです。
2.2 覚えるべき同素体
同素体がある元素は同位体と違って、4つと限られているので必ず覚えましょう!
その覚えるべき元素は\({\rm S}\)(硫黄)、\({\rm C}\)(炭素)、\({\rm O}\)(酸素)、\({\rm P}\)(リン)です。
「SCOP」の元素記号の並びから「スコップ」と覚えましょう!
3. SCOPの説明
ここでは、\({\rm S}\)、\({\rm C}\)、\({\rm O}\)、\({\rm P}\)、それぞれの同素体の種類とその性質について説明していきます。
3.1 \({\rm S}\)(硫黄)
硫黄の同素体は単斜硫黄、斜方硫黄、ゴム状硫黄の3種類があります。
常温では斜方硫黄が最も安定で、単斜硫黄もゴム状硫黄も常温で放置しておくと斜方硫黄に変化します。
斜方硫黄は原子が8個つながった分子になっているため、分子量が大きく、酸素と異なり常温で固体として存在しています。
高温(95℃以上)では単斜硫黄が最も安定となります。
それぞれの同素体は次のような性質を持ちます。
| 斜方硫黄 | 単斜硫黄 | ゴム状硫黄 | |
|
化学式 |
\({\rm S_8}\) | \({\rm S_8}\) | \({\rm S}\) |
| 構造 | 環状 | 環状 | 高分子(鎖状) |
| 特徴 |
|
|
|
3.2 \({\rm C}\)(炭素)
炭素の同素体はダイヤモンド、黒鉛、フラーレンの3種類があります。
最近では、この3種類に加えてカーボンナノチューブも問題として問われることがあります。
ダイヤモンドは宝石として指輪などに使われ、黒鉛は鉛筆の芯の原料になっています。
フラーレンはナノテクノロジーで用いられます。
ダイヤモンドは、炭素原子の4個の価電子がすべて共有結合で連続的に結合した巨大分子であるので電気を導かないのに対して、黒鉛は炭素原子の4個の価電子のうち3個が連続的に結合してできた平面構造が重なったもので、共有結合に不対電子がすべて使われていないので自由電子が存在し、電気を導きます。
他にそれぞれの同素体は次のような性質を持ちます。
| ダイヤモンド | 黒鉛 | フラーレン | |
| 化学式 |
\({\rm C}\)(組成式) |
\({\rm C}\)(化学式) |
\({\rm C_{60}}\),\({\rm C_{70}}\),(\({\rm C_{80}}\)) |
| 構造 | \({\rm C}\)原子が四面体の頂点方向に共有結合 | \({\rm C}\)原子により形成された6角形の層が分子間力で結合 | \({\rm C}\)原子がサッカーボール型に結合 |
| 色 | 無色透明 | 黒色 | |
| 性質 |
|
|
|
3.3 \({\rm O}\)(酸素)
酸素の同素体は酸素とオゾンの2種類です。
酸素が無色無臭なのに対して、オゾンは淡青色で特異臭がするということを覚えておきましょう。(理論化学の段階ではこれを覚えておけばよいです)
他にも次のような性質を持ちます。
| 酸素 | オゾン | |
|
化学式 |
\({\rm O_2}\) | \({\rm O_3}\) |
| 色 | 無色 | 淡青色 |
| におい | 無臭 | 特異臭 |
| 形 | 直線型 | 折れ線型 |
| 特性 | 助燃性あり | 紫外線吸収効果 |
3.4 \({\rm P}\)(リン)
リンの同素体には黄リンと赤リンがあります。
黄リンは毒性があり、空気中で自然発火するので水の中に入れて保存します。
一方、赤リンはマッチの横についていて、マッチの火をつけるときに使う物質です。
これからもわかりますが、赤リンは不活性であるので空気中で安定です。
黄リンを真空中で加熱すると赤リンになります。
| 黄リン | 赤リン | |
| 化学式 | \({\rm P_4}\)(分子式) |
\({\rm P}\)(組成式) |
| 毒性 | あり | なし |
| 構造 | 正四面体 | 無定形 |
4.同位体と同素体の区別の仕方
ここでは、同位体と同素体が混同しないような区別の仕方を解説していきます。
- 同位体…原子番号は同じだけど質量数は同じ元素。つまり、周期表の同じ位置にある原子
- 同素体…同じ元素からできているが、性質が違うもの。つまり、同じ元素からなる単体
このように考えると少しは間違えることはなくなるかなと思います。
5.同位体と同素体のまとめ
ここでもう一度、同位体と同素体についてまとめておこうと思います。
-
同位体とは陽子の数(原子番号)が同じで、中性子の数が異なる元素同士のことで、化学的性質(反応性など)にはあまり変化が見られない。
- 同位体は存在比が違っており、存在比の計算問題が問われることがある。
- 同位体の中の原子核が不安定で放射線を出しながら崩壊(壊変)していくもののことを放射性同位体という。
- 同じ元素からなる単体で、色や臭い、反応性などの化学的性質が異なる物質同士を互いに同素体という。
- 同素体は\({\rm S}\)(硫黄)、\({\rm C}\)(炭素)、\({\rm O}\)(酸素)、\({\rm P}\)(リン)の4つに限られており、「SCOP」の並びから「スコップ」と覚える!
- 硫黄の同素体は単斜硫黄、斜方硫黄、ゴム状硫黄の3種類がある。
- 炭素の同素体はダイヤモンド、黒鉛、フラーレンの3種類がある。カーボンナノチューブについても覚えておく。
- 酸素の同素体は酸素とオゾンの2種類がある。
- リンの同素体には黄リンと赤リンの2種類があります。
同位体と同素体は名前が似ていて混同しやすいですが、しっかりと意味を理解すれば違いは明らかです。
なので間違えないようになるまでこの記事を熟読し、確実にマスターしましょう!















なるほど
Wikiの記事では同素体は多元素存在する様ですが何が正しいですか?