東大塾長の山田です。
このページでは「イオン結晶」「共有結合の結晶」「分子結晶」について解説しています。
イオン結晶に関しては学ぶべきことがたくさんあります。また、3つの結晶にもそれぞれ特徴があるので、この記事を読んでしっかりマスターしてください!
1. イオン結晶
まずはイオン結晶についての解説です。
1.1 性質
イオン結晶はイオン結合によって形成される結晶であるので、イオン結合の特徴に基づいた固有の性質を持っています。ここでは、その性質について解説します。
- 融点や沸点の高いものが多い
- 硬いが割れやすく、もろい
- 結晶は電気を導かないが、融解液や水溶液は電気を導く
- 水に溶けやすいものが多いが、溶けにくいものもある
例:\( {\rm NaCl} \)などは水溶性、\( {\rm BaSO_4} \)などは水に難溶性
イオン結晶はベンゼンなどの無極性溶媒には溶けにくい。
【①、②について】
イオン結合はかなり強い結合力をもっているので、イオン結晶には融点の高いものが多く、硬さも優れています。
しかし、イオン結晶に強い衝撃などの外力が加わると粒子がずれて同符号のイオンどうしが向かい合います。これにより反発力が生じるので、イオン結晶はもろく、結晶の特定な面に沿って割れてしまいます。(この性質をへき開性といいます。)

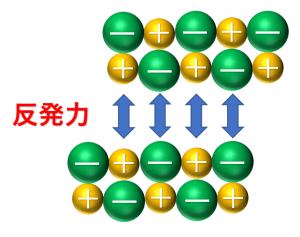
上ではイオン結晶は、強い衝撃などの外力を受けると、結晶の特定な面に沿って割れてしまうと説明しました。しかし、外力の受ける方向が変わるとイオン結晶が割れにくくなることがあります。
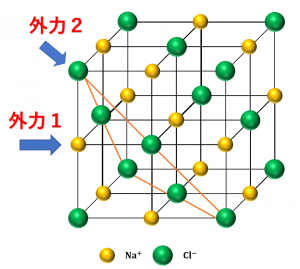
例えば、図1の外力1のように力が加わると、上でも説明したように単位格子の面に平行な面に沿って粒子のずれが生じ、同符号のイオンどうしが向かい合って反発力が生じるため、この面に沿って割れてしまいます。
しかし、図1のオレンジ色の線でつながれた図形を一つの面Aとしたときに外力2を加えたときを考えてみましょう。
面Aはずれますが、面Aは陰イオンのみで構成されており、面Aがずれたとしても同符号のイオン同士が向かい合うことはなく反発力は生じません。
よって、この面に沿って割れることはありません。
【③について】
イオン結晶は常温では基本的に固体のものが多く、基本的に電気伝導性がありません。これは、イオン結合によって比較的強固に結びついているためです。
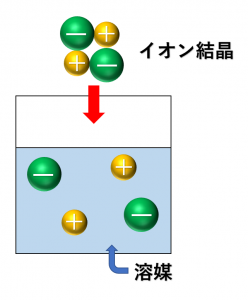
しかし、イオン結晶を水に溶かすと陽イオンと陰イオンに電離します。よって、水溶液は電気伝導性をもつようになります。
1.2 構造
イオン結晶では、陽イオンと陰イオンが交互に規則正しく立体的に配列し、イオン結合によって結晶格子を作っています。結晶格子とは、結晶の構成粒子の立体的な配列を示したもので、その最小の繰り返し単位のことを単位格子といいます。
イオン結晶の結晶格子には、塩化ナトリウム\({\rm NaCl}\)型や塩化セシウム\({\rm CsCl}\)型、\({\rm ZnS}\)型(閃亜鉛鉱型)、\({\rm CaF_2}\)型(蛍石型)などがあります。
①\({\rm NaCl}\)型
例:\({\rm NaCl}\)、\({\rm Kl}\)、\({\rm MgO}\)など
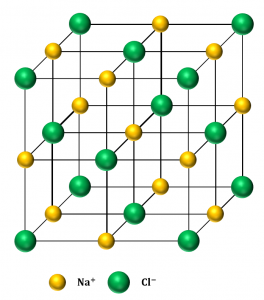
②\({\rm CsCl}\)型
例:\({\rm CsCl}\)、\({\rm CsBr}\)、\({\rm NH_4Cl}\)など
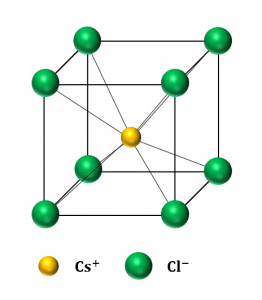
③\({\rm ZnS}\)型
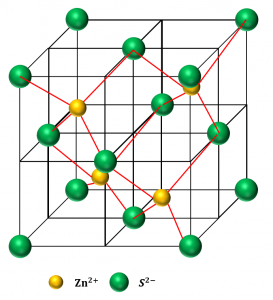
④\({\rm CaF_2}\)型
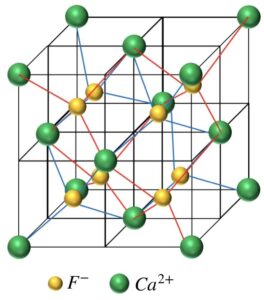
少しわかりにくくなってしまいましたが、\({\rm Ca^{2+}}\)は8つある立方体それぞれの中心に位置しています。
上で示した4つの型の図はそれぞれの結晶格子を、単位格子をベースとして各イオンの位置がわかりやすいように示したものです。
上の図では、それぞれのイオンは離れて描かれていますが、イオン結晶の結晶格子について、陽イオンと陰イオンの半径比などを考える際には、各イオンは球(剛体球)であり、陽イオンと陰イオンは互いに接していると仮定します。
1.3 イオンの配列
1.3.1 \({\rm NaCl}\)型

図6(図2と同じ)では、単位格子の各頂点と各面の中心に陰イオンがあり、単位格子の中心と各辺の中央に陽イオンがあります。
また、図7では逆に単位格子の各頂点と各面の中心に陽イオンがあり、単位格子の中心と各辺の中央に陰イオンがあります。
図6と図7は、結晶から切り出した位置がずれているだけで、どちらも同じ\({\rm NaCl}\)型の単位格子です。
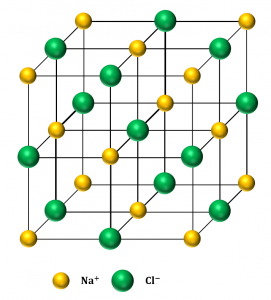
図6で陰イオンだけに注目してみると、陰イオンは面心立方格子(単位格子の各頂点と各面の中心に粒子が配置されている)と同じ配列をしています。また、図7で陽イオンだけに注目してみると、陽イオンも面心立方格子と同じ配列をしていることがわかります。
1.3.2 \({\rm CsCl}\)型

図8(図3と同じ)では、単位格子の中心に陽イオンがあり、各頂点に陰イオンがあります。また、図9では逆に単位格子の中心に陰イオンがあり、各頂点に陽イオンがあります。
図8と図9は、結晶から切り出した位置がずれているだけで、どちらも同じ\({\rm CsCl}\)型の単位格子となります。
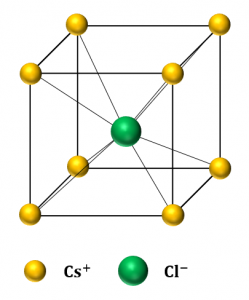
図8で陰イオンだけに注目してみると、陰イオンは単純立方格子(単位格子の各頂点だけに粒子が配置されている)と同じ配列をしています。また、図9で陽イオンだけに注目してみると、陽イオンもまた単純立方格子と同じ配列を繰り返していることがわかります。
1.4 配位数
結晶中のある1個の粒子に注目したとき、その粒子の最も近い位置に存在する周囲の粒子数のことを配位数といいます。
①\({\rm NaCl}\)型
\({\rm NaCl}\)型の結晶格子について\({\rm NaCl}\)を例に配位数を考えてみましょう。
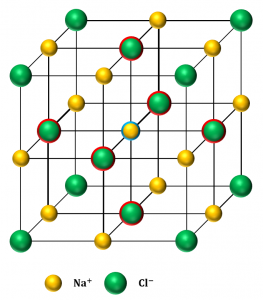
\({\rm NaCl}\)の結晶格子において、1個のナトリウムイオン\({\rm Na^+}\)には図10の通り、前後、上下、左右に6個の塩化物イオン\({\rm Cl^-}\)が隣接しています。
このとき、\({\rm Na^+}\)の配位数は6となります。
また、1個の\({\rm Cl^-}\)の配位数を考えると図7を見ればわかるように\({\rm Na^+}\)の配位数と同様に考えられ、\({\rm Cl^-}\)の配位数も6となります。
すなわち、\({\rm NaCl}\)では、\({\rm Na^+}\)と\({\rm Cl^-}\)の配位数はともに6となります。
②\({\rm CsCl}\)型
\({\rm CsCl}\)型の結晶格子について\({\rm CsCl}\)を例に配位数を考えてみましょう。
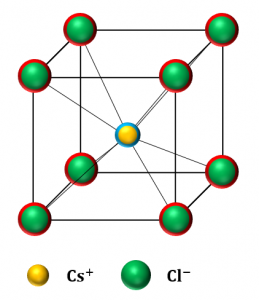
\({\rm CsCl}\)の結晶格子において、1個のセシウムイオン\({\rm Cs^+}\)には図11の通り、8個の塩化物イオン\({\rm Cl^-}\)が隣接しています。
このとき、\({\rm Cs^+}\)の配位数は8となります。
また、1個の\({\rm Cl^-}\)の配位数を考えると図9を見ればわかるように\({\rm Cs^+}\)の配位数と同様に考えられ、\({\rm Cl^-}\)の配位数も8となります。
すなわち、\({\rm CsCl}\)では、\({\rm Cs^+}\)と\({\rm Cl^-}\)の配位数はともに8となります。
1.5 イオン間の距離
【第1近接距離】
配位数でも説明しましたが、\({\rm NaCl}\)の結晶格子において、単位格子の中心にある\({\rm Na^+}\)イオンに注目すると、図12の通り、前後、上下、左右に6個の\({\rm Cl^-}\)が隣接しています
このときの\({\rm Na^+}\)イオンと\({\rm Cl^-}\)イオンとの距離を\({\rm a}\)とおくと、\({\rm a}\)は1つのイオンと最も近いイオンとの距離(第1近接距離)になります。
これは、単位格子の一辺の長さを\({\rm l}\)とすると\({\rm a}\)は\({\rm l}\)の半分になります。
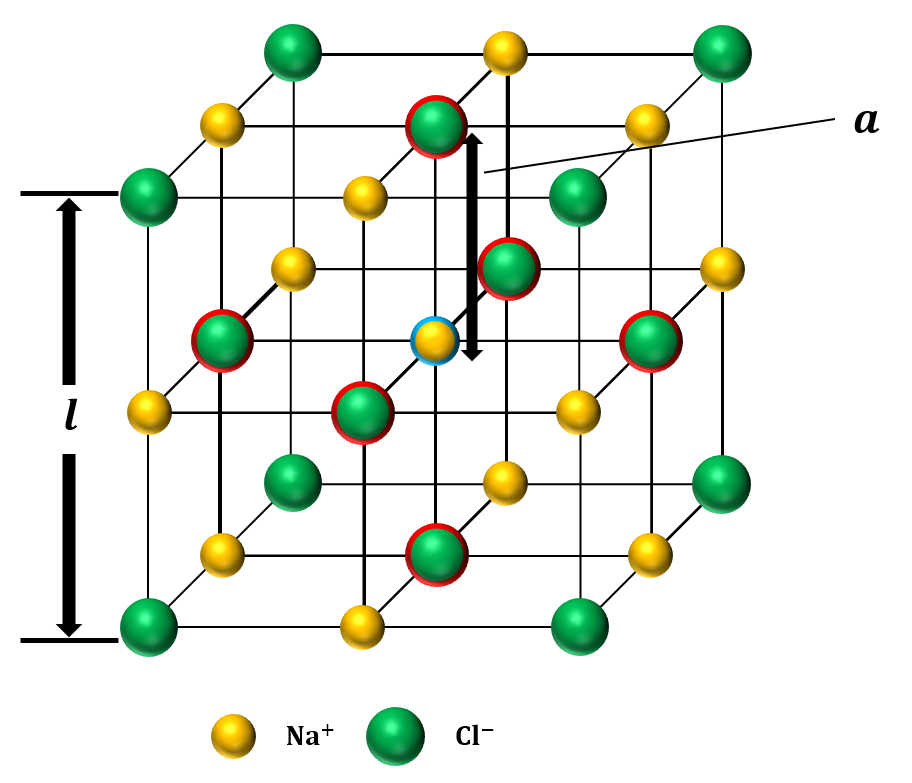
【第2近接距離】
次に、\({\rm NaCl}\)の結晶格子において、1つのイオンと2番目に近いイオンとの距離(第2近接距離)について考えてみましょう。
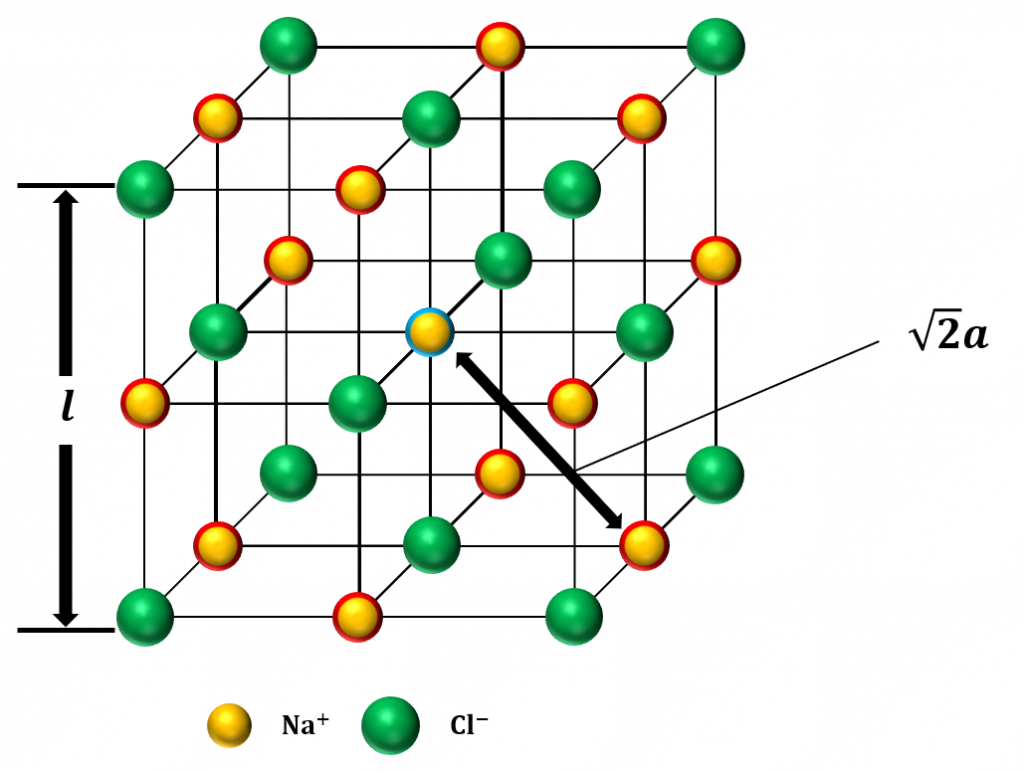
例えば、単位格子の中心にある\({\rm Na^+}\)イオンに注目すると、図13の通り、2番目に近い距離にあるイオンは、各辺の中心にある12個の\({\rm Na^+}\)イオン(赤丸で囲まれた陽イオン)です。
また、単位格子の中心の\({\rm Na^+}\)イオンと各辺の中心の\({\rm Na^+}\)イオンとの距離は\(\sqrt{2}{\rm a}\)です。
【第3近接距離】
次に、\({\rm NaCl}\)の結晶格子において、1つのイオンと3番目に近いイオンとの距離(第3近接距離)について考えてみましょう。
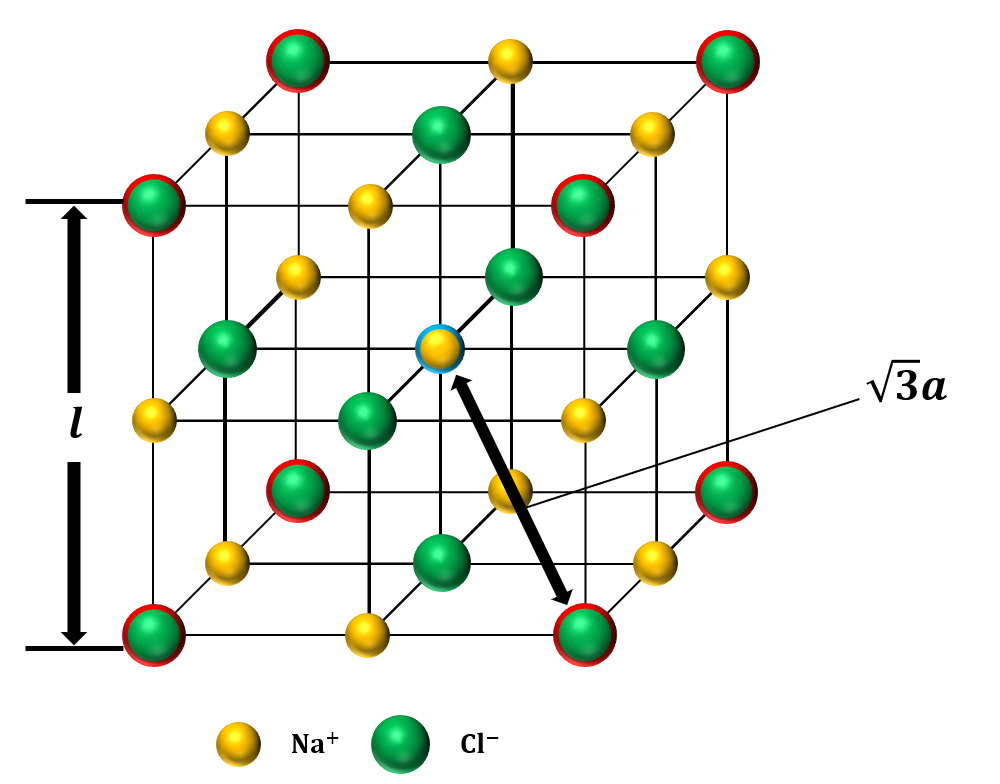
例えば、単位格子の中心にある\({\rm Na^+}\)イオンに注目すると、図14の通り、3番目に近い距離にあるイオンは、単位格子の各頂点にある8個の\({\rm Cl^+}\)イオン(赤丸で囲まれた陰イオン)です。
また、単位格子の中心の\({\rm Na^+}\)イオンと各辺の中心の\({\rm Na^+}\)イオンとの距離は\(\sqrt{3}{\rm a}\)です。
1.6 単位格子中に含まれるイオンの総数
単位格子中に含まれる陽イオン、陰イオンそれぞれのイオンの総数を求めてみましょう。
まず、\({\rm NaCl}\)の単位格子です。図2の図において単位格子の外にあるイオンを切り落とした図を考えます。それが、図15です。

この図を基に\({\rm NaCl}\)の単位格子中には、塩化物イオン\({\rm Cl^-}\)は何個分含まれるのか見ていきましょう。
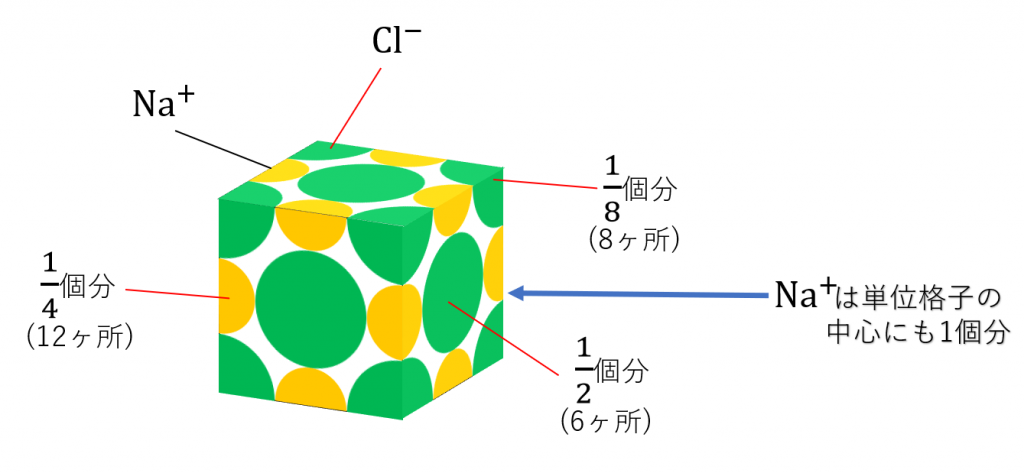
\({\rm Cl^-}\)は8つの頂点にそれぞれ\(\frac{1}{8}\)個分ずつ(各頂点に位置するイオンは、周囲の8個の単位格子に属しているため、1個の単位格子中には\(\frac{1}{8}\)個分ずつ含まれることになる)と、6つの面の中心にそれぞれ\(\frac{1}{2}\)個分ずつ(各面の中心に位置するイオンは、向かい合う2個の単位格子に属しているため、1個の単位格子中には\(\frac{1}{2}\)個分ずつが含まれることになる)あります。
つまり、合計で(\(\frac{1}{8}\times8+\frac{1}{2}\times6=\))4個分含まれています。
次に、ナトリウムイオン\({\rm Na^+}\)の数を求めます。
\({\rm NaCl}\)の組成式からわかるように、\({\rm Na^+}\)と\({\rm Cl^-}\)の個数比は1:1となるので、\({\rm Na^+}\)も単位格子中に4個分含まれているはずです。
実際に数えてみると、\({\rm Na^+}\)は、各辺の中心に\(\frac{1}{4}\)個分ずつ(ここに位置するイオンは、周囲の4個の単位格子に属しているため、1個の単位格子中には\(\frac{1}{4}\)個分ずつが含まれることになる)と単位格子の中心に丸々1個分あります。
つまり、合計で(\(\frac{1}{4}\times12+1=\))4個分含まれることになります。
次に、\({\rm CsCl}\)の単位格子に含まれるイオンの数を数えてみましょう。
\({\rm NaCl}\)のときと同様に考えると、\({\rm Cl^-}\)は8つの頂点にそれぞれ\(\frac{1}{8}\)個分ずつあります。
つまり、合計で(\(\frac{1}{8}\times8=\))1個分含まれています。
次に、セシウムイオン\({\rm Cs^+}\)の数を求めます。
\({\rm CsCl}\)の組成式からわかるように\({\rm Cs^+}\)と\({\rm Cl^-}\)の個数比は1:1となるので、\({\rm Cs^+}\)も単位格子中に1個分含まれているはずです。
実際に数えてみると、\({\rm Cs^+}\)が単位格子の中心だけに丸々1個分あるのがわかります。
1.7 イオン結晶の安定性
1.7.1 \({\rm NaCl}\)型
イオン結晶の安定性を考えるにあたって\({\rm NaCl}\)の単位格子の一つの面に着目して考えてみましょう。
下図(a)のように、陽イオン(黄色の円)の半径が一定以上の大きさのときは、陰イオン(緑色の円)同士は接触していないので、結晶は安定して存在しています。下図(b)のように、陰イオン同士が接触した状態では、結晶はぎりぎり安定して存在しています。下図(c)のように、陽イオンと陰イオンが接触していない状態では、陰イオン同士が非常に強く反発してしまい、結晶は不安定となるから存在することが出来ません。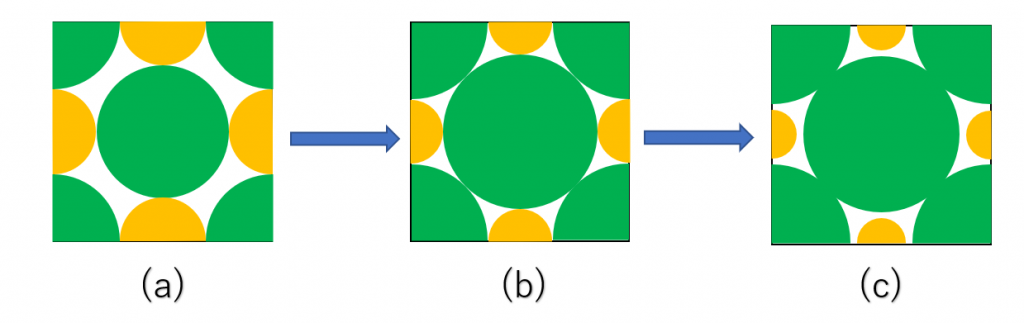
ここで、イオン結晶が上図(b)のようなぎりぎり安定な状態にあるときの陽イオンの半径\({\rm r_+}\)と陰イオンの半径\({\rm r_-}\)の比\(\frac{\rm r_+}{\rm r_-}\)を限界イオン半径比といいます。
ここで、実際に\({\rm NaCl}\)の限界イオン半径比を求めてみましょう。
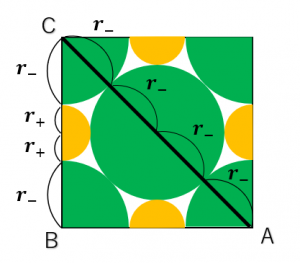
図17を見ると、陰イオン同士、陽イオンと陰イオンはそれぞれ接しています。このとき、線分\(BC\)、\(AC\)それぞれの長さは
\( BC=2{\rm r_+}+2{\rm r_-} AC=4{\rm r_-} \)
となります。ここで、この四角形は正方形であることから \( BC:AC=1:\sqrt{2} \) となることから
\( \displaystyle \frac{2{\rm r_+} + 2{\rm r_-}}{4{\rm r_-}} = \frac{1}{\sqrt{2}} \)
となるので
\( \displaystyle \frac{\rm r_+}{\rm r_-}=\sqrt{2}-1 \)
がわかります。
上の図(a)、(b)、(c)で説明したように(b)の状態よりも陰イオンが小さくなる、つまり \( \displaystyle \frac{\rm r_+}{\rm r_-} \) が大きくなったとき、\( \displaystyle {\rm NaCl} \) のイオン結晶は安定となります。
一方で、(b)の状態よりも陽イオンが小さくなる、つまり \(\displaystyle \frac{\rm r_+}{\rm r_-} \) が小さくなったとき、\( {\rm NaCl} \) のイオン結晶は不安定となります。
これより、以下のことがわかります。
\( \displaystyle \frac{\rm r_+}{\rm r_-} ≧ \sqrt{2}-1 \) のとき、\( {\rm NaCl} \) 型の結晶構造は安定である。
\( \displaystyle \frac{\rm r_+}{\rm r_-} < \sqrt{2} – 1 \) のとき、\( {\rm NaCl} \) 型の結晶構造は不安定である。
1.7.2 \({\rm CsCl}\)型
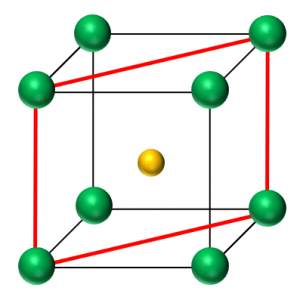
\({\rm CsCl}\) 型のイオン結晶の限界イオン半径比を考えるには、図18の赤線で囲まれた面に着目して考えます。
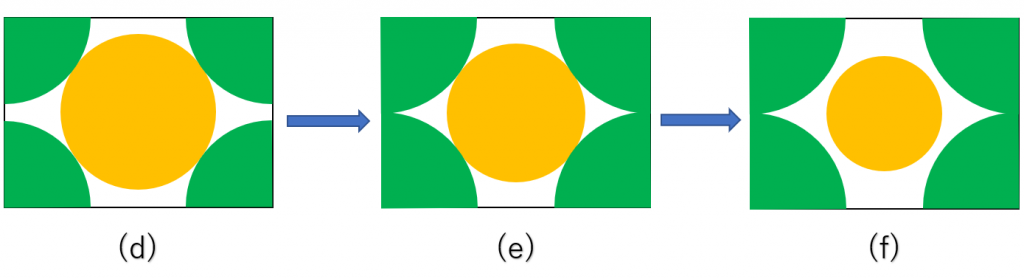
下図(d)のように、陽イオン(黄色の円)の半径が一定以上の大きさのときは、陰イオン(緑色の円)同士は接触していないので、結晶は安定して存在しています。
下図(e)のように、陰イオン同士が接触した状態では、結晶はぎりぎり安定して存在しています。
下図(f)のように、陽イオンと陰イオンが接触していない状態では、陰イオン同士が非常に強く反発してしまい、結晶は不安定となるから存在することが出来ません。
ここで、\({\rm NaCl}\)型のときと同様に限界イオン半径比を求めてみましょう。
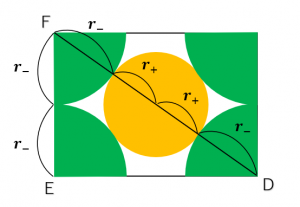
図19を見ると、陰イオン同士、陽イオンと陰イオンはそれぞれ接しています。このとき、線分\(DF\)、\(EF\)それぞれの長さは
\( \displaystyle DF=2{\rm r_+}+2{\rm r_-} EF=2{\rm r_-} \)
となります。ここで、切り取った面の立方体で対応する部分を考えると \( \displaystyle EF:DF = 1:\sqrt{3} \) となることから
\( \displaystyle \frac{2{\rm r_+}+2{\rm r_-}}{2{\rm r_-}}=\sqrt{3} \)
となるので
\( \displaystyle \frac{\rm r_+}{\rm r_-}=\sqrt{3}-1 \)
がわかります。
上の図(d)、(e)、(f)で説明したように(e)の状態よりも陰イオンが小さくなる、つまり \( \displaystyle \frac{\rm r_+}{\rm r_-} \) が大きくなったとき、\( {\rm CsCl} \) のイオン結晶は安定となります。
一方で、(e)の状態よりも陽イオンが小さくなる、つまり \( \displaystyle \frac{\rm r_+}{\rm r_-} \) が小さくなったとき、\( {\rm CsCl} \) のイオン結晶は不安定となります。
これより、以下のことがわかります。
\( \displaystyle \frac{\rm r_+}{\rm r_-} ≧ \sqrt{3}-1 \) のとき、\( {\rm CsCl} \) 型の結晶構造は安定である。
\( \displaystyle \frac{\rm r_+}{\rm r_-} < \sqrt{3}-1 \) のとき、\( {\rm CsCl} \) 型の結晶構造は不安定である。
1.7.3 イオン半径の比と結晶の型
上で求めた限界イオン半径比と同様に \( {\rm ZnS} \) の結晶構造について考えると、\( \displaystyle \frac{\rm r_+}{\rm r_-} ≧ \frac{\sqrt{6}}{2}-1 \) のとき、\( {\rm ZnS} \) 型の結晶構造が安定であることがわかります。
これまでの結果から、\( \displaystyle \frac{\rm r_+}{\rm r_-} ≧ \sqrt{3}-1 \) のとき、\( {\rm ZnS} \) 型、\( {\rm NaCl} \) 型、\( {\rm CsCl} \) 型の全てが安定な構造をとれることになります。
しかし、実際には \( \displaystyle \frac{\rm r_+}{\rm r_-} ≧ \sqrt{3}-1 \) のとき、イオン結晶の構造は\( {\rm CsCl} \) 型になる可能性が高くなります。
この理由は、イオン結晶では1つのイオンができるだけ多くの反対符号のイオンに取り囲まれたほうが安定である、つまり、配位数が多いほうが安定となることにあります。
このように考えることで、イオン半径の比を求めることで結晶の型を予想することが出来ます。
| イオン半径の比(\(\frac{\rm r_+}{\rm r_-}\))の範囲 | 予想される結晶の型(配位数) |
| \( \displaystyle \frac{\sqrt{6}}{2}-1 ≦ \frac{\rm r_+}{\rm r_-} < \sqrt{2}-1 \) | 閃亜鉛鉱 \( {\rm ZnS} \) 型(4) |
| \( \displaystyle \sqrt{2}-1 ≦ \frac{\rm r_+}{\rm r_-} < \sqrt{3}-1 \) | 塩化ナトリウム \( {\rm NaCl} \) 型(6) |
| \( \displaystyle \sqrt{3}-1 ≦ \frac{\rm r_+}{\rm r_-} < 1 \) | 塩化セシウム \( {\rm CsCl} \) 型(8) |
ちなみに、高校で学習するイオン結晶では、陽イオン半径に比べて陰イオン半径の方が多いことが多いので、ここまでのイオン結晶の安定性に関する検討では、\( {\rm r_-}>{\rm r_+} \) と仮定しています。
イオン結晶の半径比に関する問題は、これまでにも入試問題で出題されたことがあります。
答えを覚えておく必要はありませんが、自分でしっかりと導き出せるように練習しておきましょう!
2. 共有結合の結晶
ここでは、共有結合の結晶について解説します。
炭素\({\rm C}\)やケイ素\({\rm Si}\)は原子価が4(=最大)のため、多数の原子が共有結合だけで結びついて大きな結晶を作ることができます。このように、多数の原子が共有結合によってつながってできた結晶を共有結合の結晶といいます。この結晶は1つの巨大分子とみなすことができます。
しかし、ここで、ある疑問が生じます。4で詳しく説明しますが、分子結晶も共有結合で構成されているのです。そのため、どうやってこの二つを見分ければいいかわからなくなります。
そこで、共有結合の結晶となるものを覚えてしまってください。大学受験で覚えておくべき共有結合の結晶は4つしかありません。
\({\rm SiO_2}\)、\({\rm Si}\)、\({\rm C}\)、\({\rm SiC}\)
塩に シ ク シク
この4つが共有結合の結晶です。よって、残りの共有結合でつながっているものは分子結晶となります。
共有結合の結晶は、すべての構成原子が共有結合で結びついているので、融点が高くて非常に硬く、水に難溶で、一般に電気を通しません。以下では、具体的に共有結合の結晶について解説していきます。
2.1 炭素\({\rm C}\)(ダイヤモンド、黒鉛)
ダイヤモンドと黒鉛はどちらも炭素\({\rm C}\)の同素体で、共有結合の結晶を形成しますが両者の性質は大きく異なります。
2.1.1 ダイヤモンド
ダイヤモンド\({\rm C}\)は、炭素\({\rm C}\)原子がもつ4つの価電子が隣り合う\({\rm C}\)原子の価電子と共有結合し、正四面体の構造が繰り返された立体網目状構造をしています。
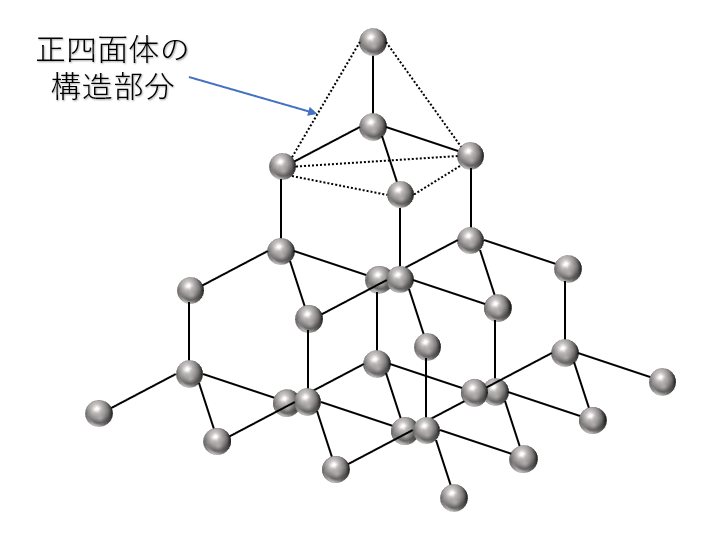
したがって、ダイヤモンドは極めて硬く、融点も非常に高くなります。
また、伝導に必要な価電子がすべて共有結合をつくるために使われているので、電気伝導性も低く、光を遮る価電子がなく可視光はすべて通過するため、色は無色透明です。
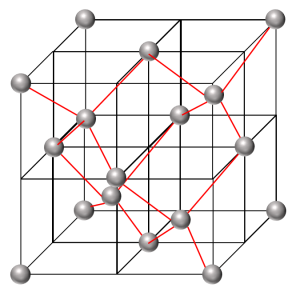
また、ダイヤモンドの単位格子は上図のようになり、\({\rm C}\)原子は単位格子中に8個あり、配位数は4となります。
2.1.2 黒鉛
黒鉛\({\rm C}\)は、炭素原子がもつ4つの価電子のうち3つのみを使って隣り合う炭素原子の価電子と共有結合し、正六角形の構造が繰り返された平面層状構造を作っています。
また、この平面層状構造同士が分子間力によって緩く結合しています。
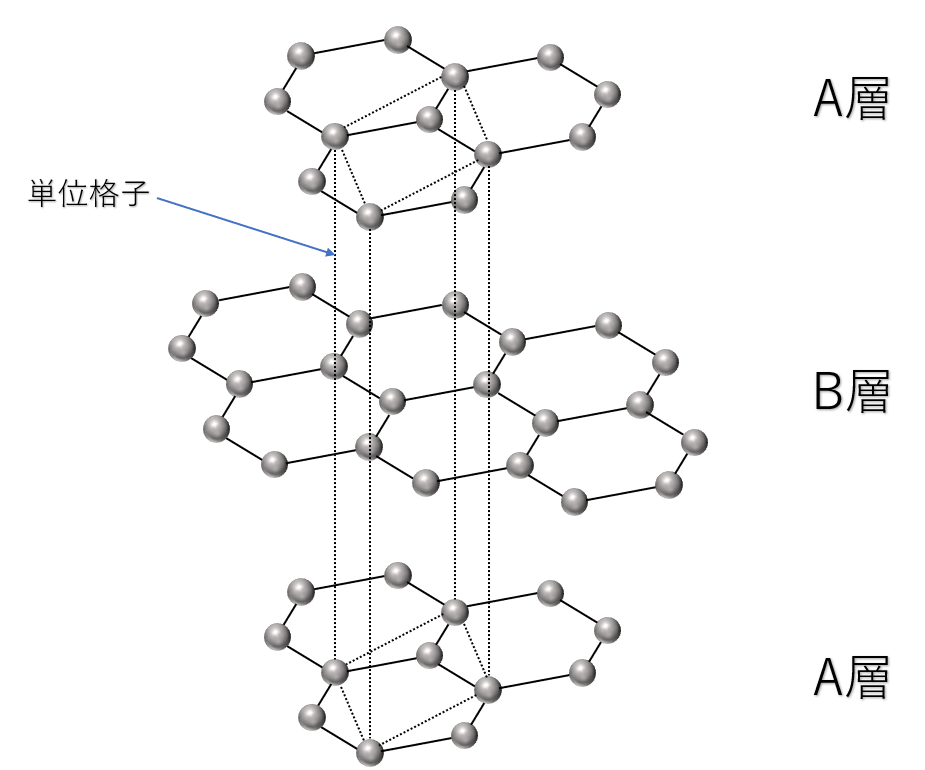
したがって、黒鉛は比較的柔らかく、また層の部分から薄くはがれやすいです。
また、伝導に必要な価電子が1つ残っているので、電気伝導性があり、光を遮る価電子が1つ残っているので可視光は一部しか透過せず、色は黒色となります。
2.2 ケイ素\({\rm Si}\)
ケイ素\({\rm Si}\)も炭素同様14族元素なので、4つの価電子をもっています。
したがって、ダイヤモンドのように正四面体構造が繰り返された共有結合の結晶を形成します。
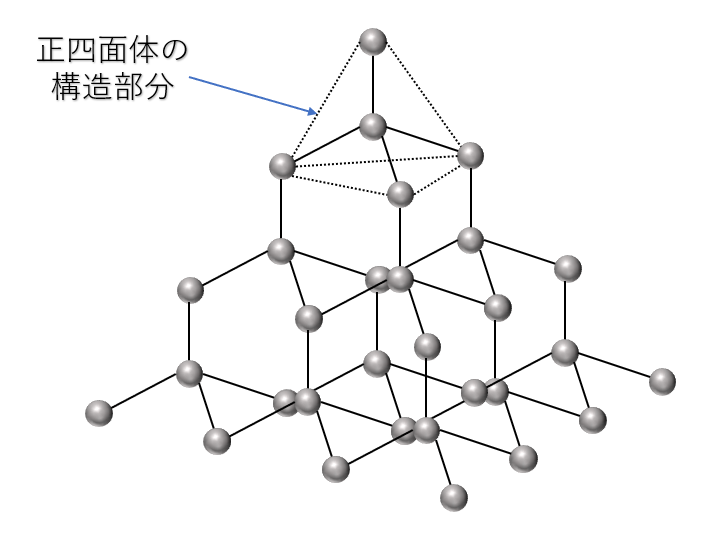
\({\rm Si}-{\rm Si}\)結合は、ダイヤモンドの\({\rm C}-{\rm C}\)結合に比べて弱く切れやすいのでやや電気を通します。
(これを半導体といいます ⇔ ダイヤモンドは絶縁体です)
したがって、純度の高いケイ素はパソコン関係の部品や太陽光発電のパネルなどに用いられます。
2.3 二酸化ケイ素\({\rm SiO_2}\)
二酸化ケイ素\({\rm SiO_2}\)の共有結合の結晶は、ケイ素\({\rm Si}\)の共有結合の結晶に\({\rm O}\)原子を組み込んだ構造になっています。
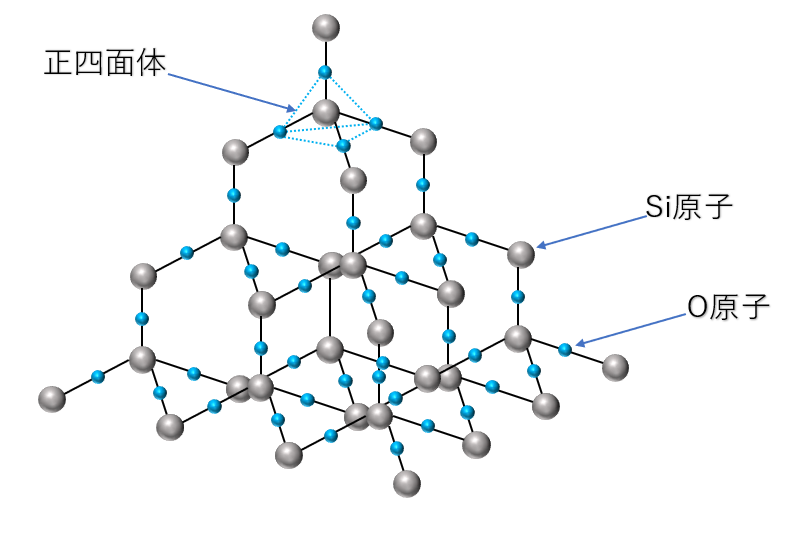
ここで、組成式は\({\rm SiO_4}\)になるのではないかという疑問が生じるかもしれません。
しかし、上図を見るとわかるように、酸素原子は2つのケイ素原子と結びついているので、1つのケイ素原子に対して\(\frac{1}{2}\)となるのです。
よって、\(\frac{1}{2}\)が4個で2個分となり、組成式は\({\rm SiO_2}\)となります。
二酸化ケイ素\({\rm SiO_2}\)は、ダイヤモンド同様、硬くて融点が高く、電気も通しません。
天然に水晶や石英として存在していて、その多くは光ファイバーや時計の部品などとして利用されています。
3. 分子間力
分子間に働く引力のことを分子間力といいます。分子間力には、ファンデルワールス力や水素結合など、いくつかの種類があります。
高校化学では、ファンデルワールス力と水素結合を知っていれば問題ないので、ここではファンデルワールス力について説明します。
(水素結合については「水素結合とは(水などの例・沸点・エネルギー・距離と強さの比較)」の記事を参照してください。)
3.1 ファンデルワールス力
ファンデルワールス力とは、電荷の偏りが原因となって生じる引力(反発力)のことをいいます。
極性のあるなしにかかわらず、分子の中では常に電子の移動が起こっているため、世の中に存在するすべての分子にわずかな電荷の偏りが生じています。
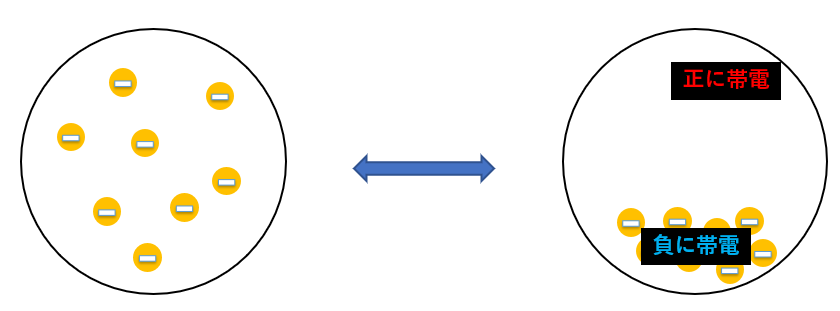
この電荷の偏りによって生じたわずかなプラスとわずかなマイナスが引き合うことにより、弱い結合が形成されることがあります。
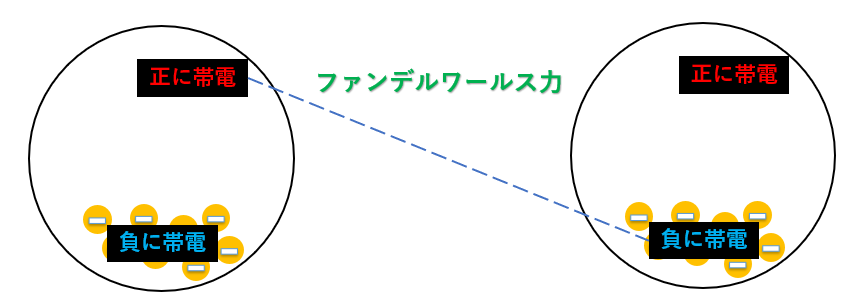
このときのプラス・マイナス間に働く引力をファンデルワールス力といいます。
先ほど述べたように、わずかな電荷の偏りはすべての分子において発生するため、この力も基本的にすべての分子間に存在しています。
しかし、ファンデルワールス力は非常に弱い力なので、その他の化学結合と比べてこの結合はかなり弱くなります。
3.2 ファンデルワールス力の特徴
ファンデルワールス力を考えるうえで重要なポイントが2つあり、いずれもテストでよく出題されるところなのでしっかり覚えてください。
①構造や性質が似ている分子であれば、一般に、分子量が大きくなるほど分子間に働くファンデルワールス力は大きくなる。
②表面積の大きな分子ほど、分子間に働くファンデルワールス力は大きくなる。
4. 分子結晶
ドライアイス\({\rm CO_2}\)・ヨウ素\({\rm I_2}\)・氷\({\rm H_2O}\)など、多数の分子が分子間力によって引き合って、規則正しく配列してできた結晶を分子結晶といいます。
4.1 ドライアイスの分子結晶

\({\rm CO_2}\)分子が分子間力で規則正しく配列してできた白色の結晶がドライアイスです。常温で容易に昇華(固体↔気体)します。
4.2 ヨウ素の分子結晶
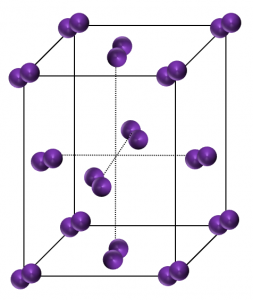
\({\rm I_2}\)分子が分子間力で規則正しく配列すると黒紫色の結晶ができます。穏やかに加熱を行うことで昇華します。
5. まとめ
最後にイオン結晶・共有結合の結晶・分子結晶についてまとめます。
- イオン結晶は融点や沸点の高いものが多く、硬いが割れやすく、もろい。結晶では電気を導かないが、融解液や水溶液は電気を導く。水に溶けやすいものが多いが、溶けにくいものもある。
- イオン結晶の結晶格子には、塩化ナトリウム\({\rm NaCl}\)型や塩化セシウム\({\rm CsCl}\)型、\({\rm ZnS}\)型(閃亜鉛鉱型)、\({\rm CaF_2}\)型(蛍石型)などがある。
- 結晶中のある1個の粒子に注目したとき、その粒子の最も近い位置に存在する周囲の粒子数のことを配位数という。
- イオン結晶がぎりぎり安定な状態にあるときの陽イオンの半径\({\rm r^+}\)と陰イオンの半径\({\rm r^-}\)の比\(\frac{\rm r^+}{\rm r^-}\)を限界イオン半径比という。
- \( \displaystyle \frac{\sqrt{6}}{2}-1 ≦ \frac{\rm r_+}{\rm r_-} < \sqrt{2}-1 \) のとき、閃亜鉛鉱 \( {\rm ZnS} \) 型、\( \displaystyle \sqrt{2}-1 ≦ \frac{\rm r_+}{\rm r_-} < \sqrt{3}-1 \) のとき、塩化ナトリウム \( {\rm NaCl} \) 型、\( \displaystyle \sqrt{3}-1 ≦ \frac{\rm r_+}{\rm r_-} < 1 \) のとき、塩化セシウム \( {\rm CsCl} \) 型になる。
- 多数の原子が共有結合によってつながってできた結晶を共有結合の結晶という。
- 共有結合の結晶となるものは\({\rm SiO_2}\)、\({\rm Si}\)、\({\rm C}\)、\({\rm SiC}\)である。
- 分子間に働く引力のことを分子間力という。分子間力には、ファンデルワールス力や水素結合などがある。
- ファンデルワールス力とは、電荷の偏りが原因となって生じる引力(反発力)のことをいう。
- 分子量が大きくなるほど分子間に働くファンデルワールス力は大きくなる。また、表面積の大きな分子ほど、分子間に働くファンデルワールス力は大きくなる。
- 多数の分子が分子間力によって引き合って、規則正しく配列してできた結晶を分子結晶という。
イオン結晶、共有結合の結晶、分子結晶それぞれの特徴について出題されることがよくあります。
違いは明確なのでしっかりと理解すれば間違えることはなくなります。
マスターできるまでこの記事を読みこんでください!















わかりやすい解説をありがとうございます。
一つ誤字の報告です。「共有結合の結晶」の「共有結合の覚え方」の見出しが、「共有結語の覚え方」になってます。気になったので一応コメントに残します。
ご指摘いただきありがとうございます。
ご指摘箇所は訂正いたしました。
図5のCaF2の格子ですが、図中の黄Ca2+と緑F-は逆ではないですか
ご指摘いただきありがとうございます。
ご指摘箇所は訂正いたしました。