東大塾長の山田です。
このページでは「共有結合」について解説しています。
共有結合にはちゃんと結合のルールがあり、この記事を読めばマスターできるようになっているので、是非参考にしてください!
1. 共有結合とは?
原子間の結合において、2つの原子がいくつかの価電子を互いに共有し合うことによってできる結合のことを共有結合といいます。
また、電子式で描いたときにペアになる電子をもたない電子を不対電子といいます。共有結合は2つの原子がお互いの不対電子を共有することで形成されます。
共有結合は、電子を受け取ろうとする傾向の強い原子間の結合であり、共有結合は非金属元素の原子間の結合となります。
ちなみに、イオン結合は非金属元素と金属元素の原子間の結合、金属結合は金属元素の原子間の結合となります。
(イオン結合、金属結合についての詳しい説明はそれぞれ「イオン結合とは(例・結晶・共有結合との違い・半径)」「金属結合とは(例・特徴・金属結晶・立方格子)」で解説しているのでそちらも参考にしてください。)
ここで、共有結合について塩素を例に見てみましょう。
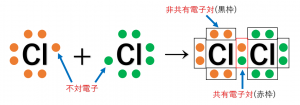
上の図のように原子間に共有され、共有結合にかかわる電子のペアを共有電子対、原子間に共有されてはおらず、直接には共有結合にかかわらない電子のペアを非共有電子対といいます。
塩素\({\rm Cl_2}\)や水素\({\rm H_2}\)、水\({\rm H_2O}\)などの分子を構成している原子間の結合は共有結合であり、いくつかの原子が共有結合によって結合してできた粒子が分子です。
また、\({\rm Cl_2}\)分子では、原子間が1つの共有電子対で結びついており、このような共有結合を単結合といいます。
2. 共有結合の例
ここでは、共有結合を使って結合している分子を紹介したいと思います。
それにあたり、分子が単結合、二重結合、三重結合のどれをとるのかにはルールがあるので説明していきます。
「原子構造と電子配置・価電子」の記事で説明しているように原子は「希ガスと同じ電子配置」をとるときに最も安定となります。したがって、原子はできるだけ希ガスと同じ電子配置になるように3つの結合のいずれかをとります。
このルールを意識して例を見ていきましょう。
2.1 \({\rm CH_4}\)(メタン)
メタン(\({\rm CH_4}\))は、1つの炭素原子(\({\rm C}\))と4つの水素原子(\({\rm H}\))が結合して作られます。
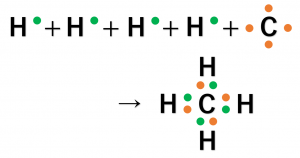
メタンの場合、\({\rm C}\)は4個、\({\rm H}\)が1個の不対電子を持つので、\({\rm C}\)と\({\rm H}\)が1個ずつ電子を出し合い共有結合を形成します。
2.2 \({\rm NH_3}\)(アンモニア)
アンモニア(\({\rm NH_3}\))は、1つの窒素原子(\({\rm N}\))と3つの水素原子(\({\rm H}\))が結合して作られます。
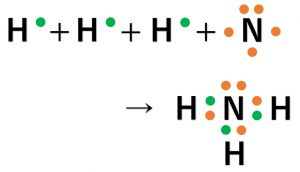
アンモニアの場合、\({\rm N}\)は3個、\({\rm H}\)が1個の不対電子を持つので、\({\rm N}\)と\({\rm H}\)が1個ずつ電子を出し合い共有結合を形成します。
2.3 \({\rm CO_2}\)(二酸化炭素)
二酸化炭素(\({\rm CO_2}\))は、1つの炭素原子(\({\rm C}\))と2つの酸素原子(\({\rm O}\))が結合して作られます。
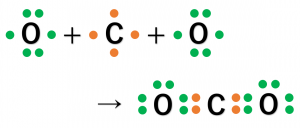
上で例として挙げた\({\rm Cl_2}\)、\({\rm CH_4}\)、\({\rm NH_3}\)は、それぞれの分子が1個ずつ電子を出し合うことで共有結合を作っていました。しかし、二酸化炭素の場合は、\({\rm O}\)は(それぞれ)2個、\({\rm C}\)は4個の不対電子を持つので、\({\rm O}\)と\({\rm C}\)は2個ずつ電子をだしあって共有結合を形成します。
\({\rm CO_2}\)分子では、原子間が2つの共有電子対で結びついており、このような共有結合を二重結合といいます。
このとき、下のようになると考える人がいます。
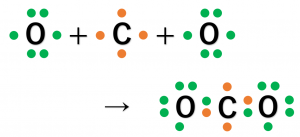
しかし、最初に述べたように原子は希ガスの電子配置をとるとき最も安定になるので、すべての原子が電子を8個持つように結合するためこのように結合すると炭素原子は電子を6個、酸素原子は電子を7個しか持ちません。
したがって、二酸化炭素は二重結合するときが最も安定となるから単結合となることはありません。
2.4 \({\rm N_2}\)(窒素分子)
窒素分子は(\({\rm N_2}\))は、窒素原子(\({\rm N}\))には不対電子が3個存在しており、それらを3個ずつ出し合って次のように結合します。
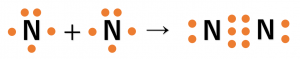
この場合も2つの\({\rm N}\)原子が安定な希ガスの電子配置となっています。
また、\({\rm N_2}\)分子では、原子間が3つの共有電子対で結びついており、このような共有結合を三重結合といいます。
3. 価標
下の図のように電子式で表した分子の結合状態において、共有電子対を1本の線で示した化学式を構造式といい、この線(下の図の赤い線)を価標といいます。
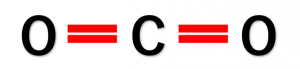

また、構造式において、それぞれの原子から出る価標の数を原子価といいます。原子価は、その原子がもつ不対電子の数に相当します。
| 元素名 | 水素 | フッ素 | 酸素 | 硫黄 | 窒素 | 炭素 |
| 不対電子の数 | 1個 | 1個 | 2個 | 2個 | 3個 | 4個 |
| 原子価 | 1個 | 1個 | 2個 | 2個 | 3個 | 4個 |
4. 配位結合
結合する原子間で、一方の原子から非共有電子対が提供されて、それを2つの原子が共有する共有結合を配位結合といいます。
言葉でいわれるだけだとわかりにくいと思うので、アンモニウムイオン\({\rm {NH_4}^+}\)(\({\rm NH_3}\)と\({\rm H^+}\)の配位結合)、オキソニウムイオン\({\rm {H_3O}^+}\)(\({\rm H_2O}\)と\({\rm H^+}\)の配位結合)を例に説明したいと思います。
まず、アンモニウムイオンです。
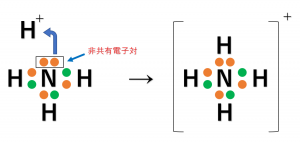
アンモニアが、窒素原子の非共有電子対を水素イオンに一方的に供与することで結合が形成されています。ちなみに、配位結合は基本的に「±0」の分子と「プラス」のイオンが結合します。したがって、全体としては「プラス」の電荷をもちます。
次に、オキソニウムイオンです。
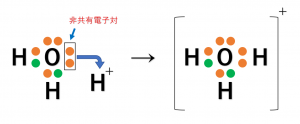
水が、酸素原子の非共有電子対を水素イオンに一方的に供与することで結合が形成されています。
5. 配位結合の構造式における表記の仕方
配位結合は共有結合の1つです。配位結合は一度できてしまうと共有結合と見分けがつかなくなります。
例えば、\({\rm {NH_4}^+}\)の4個のN-H結合は全く同じ性質を示し、どれがが配位結合による結合か区別できなくなります。
したがって、共有結合のように「価標」を使って表すことができます。
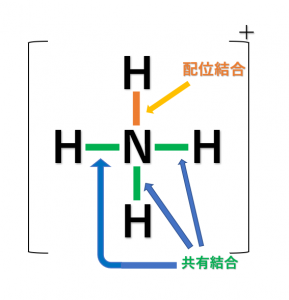
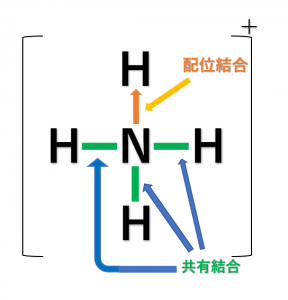
ちなみに、共有結合と区別して(電子対を一方的に供与していることを示す)矢印で表すこともあるので覚えておいてください。
6. まとめ
最後に共有結合についてまとめておこうと思います。
- 原子間の結合において、2つの原子がいくつかの価電子を互いに共有し合うことによってできる結合のことを共有結合という。
- 共有結合は非金属元素の原子間の結合である。
- 原子間に共有され、共有結合にかかわる電子のペアを共有電子対、原子間に共有されてはおらず、直接には共有結合にかかわらない電子のペアを非共有電子対という。
- 原子間が1つの共有電子対で結びついているような共有結合を単結合という。
- 原子間が2つの共有電子対で結びついているような共有結合を二重結合という。
- 原子間が3つの共有電子対で結びついているような共有結合を三重結合という。
- 電子式で表した分子の結合状態において、共有電子対を1本の線で示した化学式を構造式といい、この線を価標という。
- 構造式において、それぞれの原子から出る価標の数を原子価という。
- 結合する原子間で、一方の原子から非共有電子対が提供されて、それを2つの原子が共有する共有結合を配位結合という。
共有結合のルールを覚えておくと分子の形を覚えることなく考えて導き出せるようになります。
この分野は覚えることが多いですが、大事なところなのでしっかり覚えてください!
また、イオン結合、金属結合についても共有結合と区別できるようにそれぞれ「イオン結合とは(例・結晶・共有結合との違い・半径)」、「金属結合とは(例・特徴・金属結晶・立方格子)」の記事を見てマスターしてください!
共有結合の結晶については、イオン結合の結晶とともに「イオン結晶・共有結合の結晶・分子結晶」の記事で解説しているのでそちらを参照してください。















コメントを残す