東大塾長の山田です。
このページでは、「等温変化」について詳しく説明しています。ぜひ勉強の参考にしてください!
また、この内容を扱うにおいて熱力学第一法則の知識が不可欠です。
「熱力学第一法則の解説記事」の内容を理解してから読むと、より理解が深まるので,こちらも参考にしてください。
1. 等温変化について
1.1 等温変化とは
等温変化とは、文字通り、温度を一定に保って行う状態の変化のことです。
熱を伝えやすい素材でできたシリンダーにおいて、ゆっくりとピストンを動かして内部と外部の温度を等しくしておくような状態変化が主な例です。
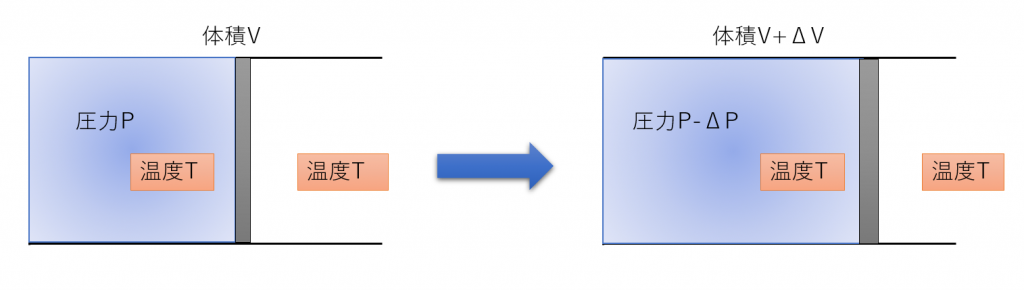
等温変化を行っているとき、状態方程式 \( PV = nRT \) から \( PV = 一定 \) が成立します(ボイルの法則)。
このときP-Vグラフにおける状態図は、双曲線となり、圧力と体積がともに変化します。
このとき、気体の温度が変化していないため、内部エネルギーの変化 \( \Delta U \) はゼロです(内部エネルギーは温度に依存するから)。
よって等温変化における熱力学第一法則は以下のようになります。
\( \displaystyle -W + Q = 0 \quad W=Q \)
上の式より、等温変化においては気体が加えた熱は、すべて気体が膨張(圧縮)するための仕事になる、ことが分かります!
以下では実際にP-Vグラフを用いて、変化の様子をとらえていきましょう!
1.2 P-Vグラフを用いた議論
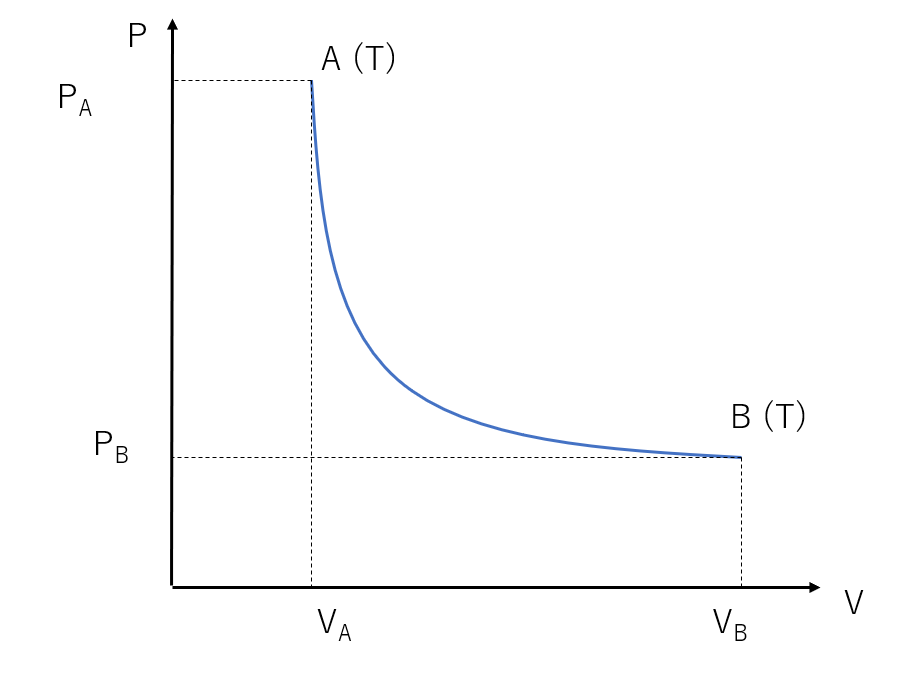
上のように、\( n \) [mol] の気体が状態A、Bを取る状況を考えてみましょう。ただしA・Bにおける温度を \( T \) [K] とします。
このとき、A⇒B と B⇒A は等温変化です。
また、A⇒Bのように気体が膨張していく過程を「等温膨張」、逆にB⇒Aのように気体が圧縮されていく過程を「等温圧縮」といいます。
二つの変化について同時に考察していきます。
状態方程式
AとBにおける状態方程式は
\( \begin{cases}
\displaystyle P_A V_A = nRT \\
\displaystyle P_B V_B = nRT
\end{cases} \)
内部エネルギー変化
内部エネルギー変化は温度変化のみに依存するから、それぞれの過程における内部エネルギー変化は、
\( \displaystyle \Delta U_{AB}=\Delta U_{BA}=0 \)
となります。
仕事
ここで、気体が外部にした仕事は、P-V図の面積となります。
P-Vグラフから仕事を求めるときは、符号ミスに気を付けてください。符号ミスも、仕事の定義をしっかりと考えれば起こることはありません。
今回は、初回なのでしっかりと積分形を用いて、仕事を表現します。
それぞれの過程における気体がした仕事は、
\( \begin{cases}
\displaystyle W_{AB} = \int_{V_A}^{V_B} P d V = nRT \int_{V_A}^{V_B} \frac{1}{V} dV \\
\displaystyle W_{BA} = \int_{V_B}^{V_A} P d V = nRT \int_{V_B}^{V_A} \frac{1}{V} dV
\end{cases} \)
となります。
上の積分計算を行うには、積分公式
\( \displaystyle \int \frac{1}{x} dx = \log | x | \)
を用いればよく、
\( \begin{cases}
\displaystyle W_{AB} = nRT \left( \log V_B – \log V_A \right) = nRT \log \frac{V_B}{V_A} \\
\displaystyle W_{BA} = nRT \left( \log V_A – \log V_B \right) = nRT \log \frac{V_A}{V_B}
\end{cases} \)
と表記することができます!
吸熱量
あとはこれを熱力学第一法則 \( Q = W \) に代入すると、
\( \begin{cases}
\displaystyle Q_{AB} = nRT \log \frac{V_B}{V_A} \\
\displaystyle Q_{BA} = nRT \log \frac{V_A}{V_B}
\end{cases} \)
が得られます!
気体がした仕事、吸熱量は求めることが要求される場合もあるので、導出過程をしっかりと抑えておきましょう。
2. まとめ
以上が等温変化における議論となります!計算は良いなものが多いですが、しっかりと定義を確認して符号ミスがないように注意してください!
最後に今回学んだことをまとめておくので、復習に役立ててください!
熱力学第一法則:\( W = Q \)
\( \displaystyle W = Q = nRT \log \frac{V_B}{V_A} \)














目から鱗
これ等温じゃなくて等温可逆では?
P=nRT/VはP(ex)に≒P(in)が条件では?