東大塾長の山田です。
このページでは、「高校物理の熱力学の公式」をすべてまとめてあります。
(該当記事がある場合)それぞれの公式を詳しく説明した記事へのリンクが貼ってあります。
それぞれの解説記事も併せて読むことで、さらなる理解につながるので、そちらもぜひ参考にしてください!
熱力学公式まとめ
比熱の公式
比熱:単位質量の物体の温度を1[K]上昇させるために必要な熱量のこと。
熱量保存則:異なった温度の物体を接触させた時、しばらく時間がたった時全体が中間期な温度になる(熱平衡)。このとき、他との熱のやり取りがないとすると、
「低温物質が得た熱量=高温物質が失った熱量」
が成立する。
理想気体の状態方程式
理想気体については以下の状態方程式が成り立つ。
\( \displaystyle PV=nRT \)
\( P \):圧力\( [\rm{Pa}]\),\( V \):体積\( [\rm{m^3}] \),\( n \):物質量\( [\rm{mol}] \),\( R \):気体定数,\( T \):温度\( [\rm{K}] \)
また、気体の状態方程式より以下の法則が成り立つことが分かる。
温度一定のとき:\( \displaystyle PV=\rm{const.} \)(ボイルの法則)
圧力一定のとき:\(\displaystyle \frac{V}{T}=\rm{const.} \)(シャルルの法則)
上二つ合わせて:\(\displaystyle \frac{PV}{T} = \rm{const.} \)(ボイル・シャルルの法則)
気体分子運動論の公式
記事を取得できませんでした。記事IDをご確認ください。
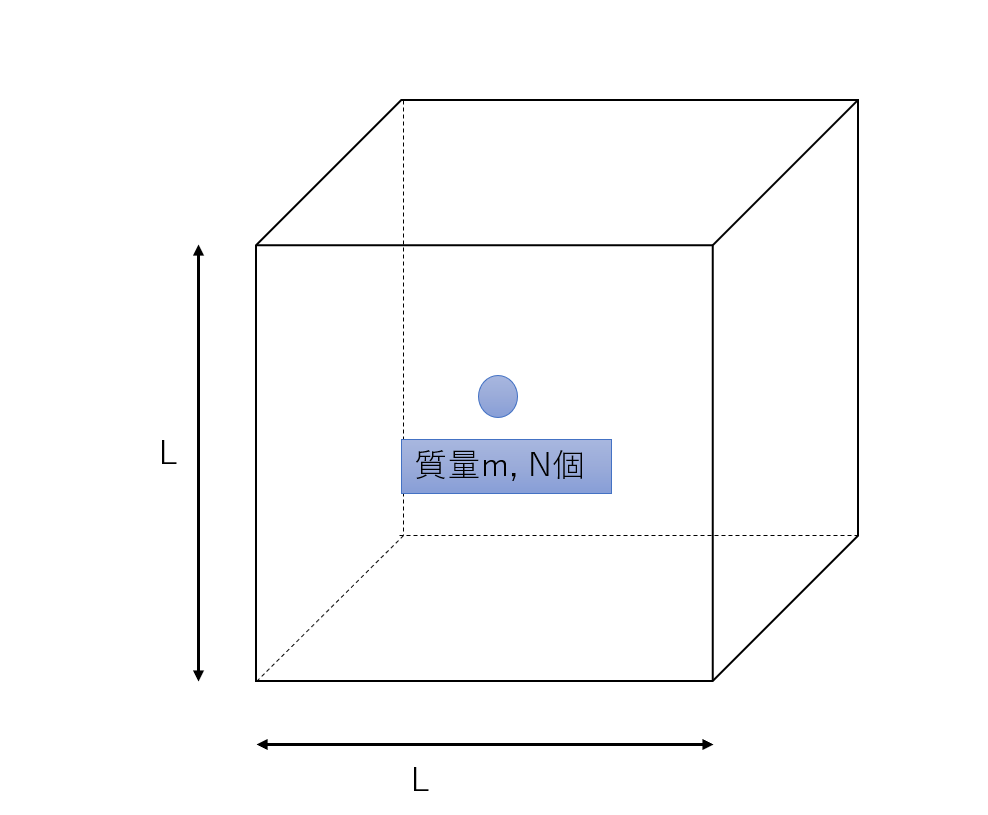
①一つの気体分子が単位時間あたりに壁に及ぼす力積を求める。
\( \displaystyle 2mv_x \)
②求めた力積から、一個の分子が単位時間あたりに気体分子が壁に及ぼす力 \( \displaystyle \bar{f} \) を求め、\( N \) 個の分子が及ぼす力 \( F \) を求める。
\( \displaystyle \bar{f} = \frac{mv_x^2 }{L} = \frac{m\bar{v}^2}{3L} \)
\( \displaystyle ∴ \ F = \frac{Nm\bar{v_x}^2}{L} = \frac{Nm\bar{v}^2}{3L} \)
③壁にかかる圧力 \( P \) を求める。
\( \displaystyle P = \frac{Nm\bar{v}^2}{3V} \)
④理想気体の状態方程式を用いて、「分子の平均運動エネルギー」「内部エネルギー」を求める。
\( \displaystyle \frac{1}{2} m \bar{v}^2 = \frac{3}{2}kT \)
\( \displaystyle U = \frac{3}{2}nRT \)
内部エネルギーの公式
単原子分子理想気体の内部エネルギー:\( \displaystyle U = \frac{3}{2}nRT \)
分子数と温度に比例することが分かる!
(cf.二原子分子の場合:\( \displaystyle U = \frac{5}{2}nRT \))
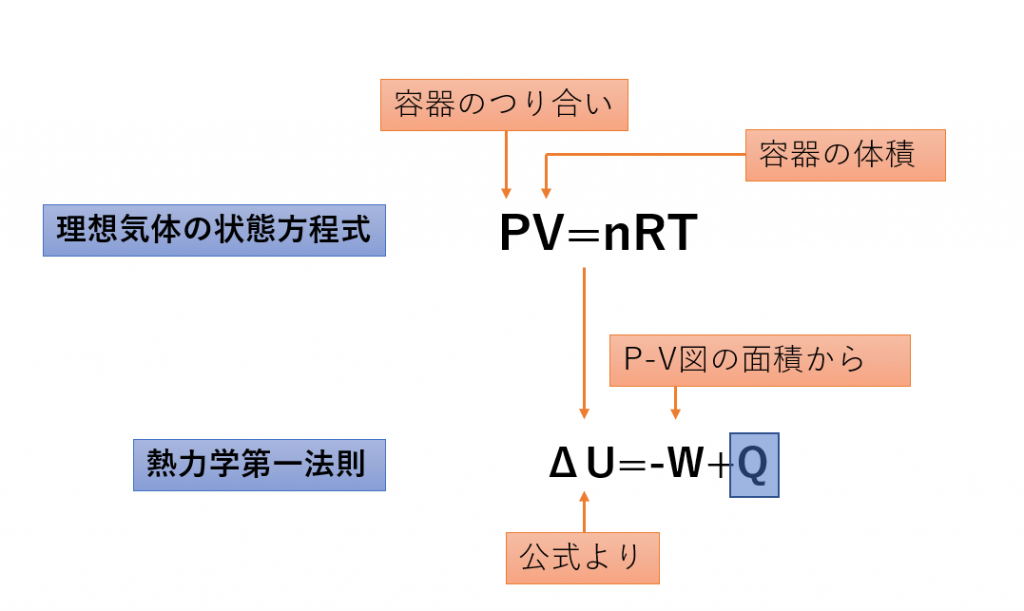
熱力学第一法則と熱力学の枠組みまとめ
熱力学第一法則:\( \Delta U=-W+Q \)
\( \begin{align}
& \Delta U : 内部エネルギーの変化 \\
& W:気体がする仕事 \\
& Q:吸熱量
\end{align} \)
熱力学の枠組み
定積モル比熱:\( \displaystyle C_V = \frac{3}{2}R \)
定圧モル比熱:\( \displaystyle C_P = \frac{5}{2}R \)
マイヤーの法則:\(C_P-C_V=R\)
比熱比:\( \displaystyle γ = \frac{C_P}{C_V} = \frac{5}{3} \)
ただしこれらは、すべて単原子理想気体における値。
定圧変化の公式
熱力学第一法則:\( \Delta U = – p \Delta V+Q \)
定圧モル比熱:\( \displaystyle C_P = \frac{5}{2} R \)
定積変化の公式
熱力学第一法則:\( \displaystyle \Delta U=Q \)
定積モル比熱:\( \displaystyle C_V = \frac{3}{2}R \)
等温変化の公式
熱力学第一法則:\( W=Q \)
\( \displaystyle W=Q=nRT \log \frac{V_B}{V_A} \)
断熱変化とポアソンの公式
熱力学第一法則:\( \displaystyle \Delta U=-W \)
ポアソンの公式:\( \displaystyle P V^{\gamma}=\rm{const.},\quad T V^{γ-1}=\rm{const.} \)
ただし \( \gamma \) は比熱比\( \displaystyle γ=\frac{C_P}{C_V} \)である。
断熱変化:ポアソンの公式と熱力学第一法則を用いる
非平衡過程:全体のエネルギー収支に着目する
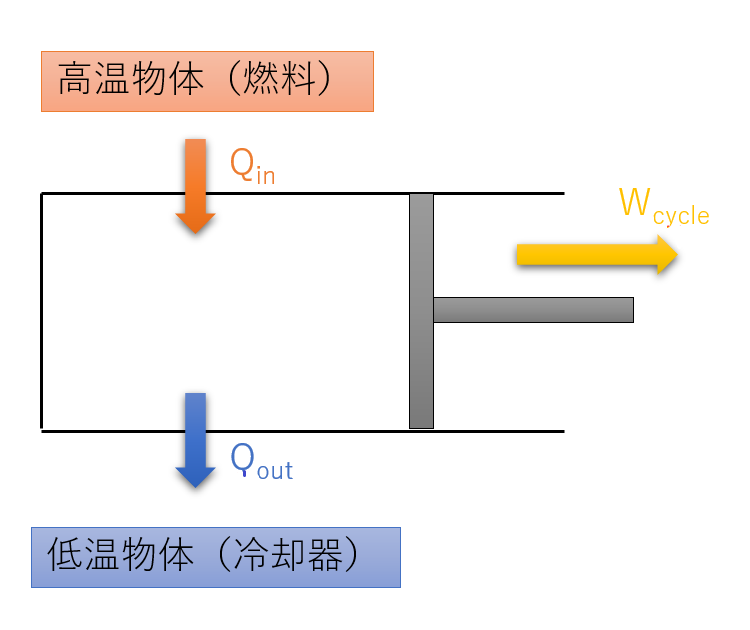
熱サイクルと熱効率の公式
熱サイクルにおける熱力学第一法則:\( \displaystyle W_{c y c l e}=Q_{i n}-Q_{o u t} \)
熱効率の定義:\( \displaystyle e = \frac{W_{c y c l e}}{Q_{i n}} = 1 – \frac{Q_{o u t}}{Q_{i n}} \)
以上です!
熱力学の公式は数は多くないものの、いざ使うにあたって形を間違えやすいものが多いです。
導出過程も含めて頭に入れておきましょう!














わからん
一本6000円のトマトジュース高いと思いますか
熱力学はバチクソ難しい
それは君の頭がパーチクリン
おれも
ピザ食べたい
うん美味しい
熱力学意味わかんなすぎて泣きそう
僕が分かると思うか?いや、分からないだろう。
それよりもおちんたまが痒い。