東大塾長の山田です。
このページでは結合エネルギーについて解説しています。
エネルギーにもいくつか種類がありますが、ここでは一つ一つ例を用いて紹介しています。是非参考にしてください。
1. エネルギー
1.1 結合エネルギー
共有結合している物質\(1 mol\)をバラバラにして、原子と原子に切り離す際に必要なエネルギーのことを結合エネルギーといいます。
【例】
\(H-H\)の結合エネルギーは\(432 kJ/mol\)である。
\[H_2(気)=2H(気)-432 kJ\]
1.2 解離エネルギー
分子\(1 mol\)に存在するすべての共有結合を切断するのに必要なエネルギーのことを解離エネルギーといいます。解離エネルギーの値は、分子中に存在するすべての結合の結合エネルギーの総和と等しくなります。
【例】
\(CH_4\)の解離エネルギーは\(1644 kJ/mol\)である。
\[CH_4(気)=C(気)+4H(気)-1644 kJ\]
\(1 mol\)の\(CH_4\)は分子中に、\(4 mol\)の\(C-H\)をもつ。\(CH_4\)の解離エネルギーが\(1644 kJ/mol\)であるということは、\(4 mol\)の\(C-H\)の結合エネルギーの総和が\(1644 kJ/mol\)であるということを意味する。これより、\(C-H\)の結合エネルギーは
\[C-Hの結合エネルギー=\frac{1644 kJ}{4 mol}=411 kJ/mol\]
となることがわかる。
1.3 格子エネルギー
結晶を気体の構成粒子まで完全にバラバラにするのに必要なエネルギーのことを格子エネルギーといいます。格子エネルギーの値が大きいことは、結晶を構成する粒子間の結びつきが強いことを意味します。
【例】
ナトリウム\(Na\)単体の結晶の格子エネルギーは\(91.7 kJ/mol\)である。
\[Na(固)=Na(気)-91.7 kJ\]
この熱化学方程式からわかるように、金属結晶や分子結晶(または、共有結晶)の格子エネルギーは、それらの昇華熱に相当する。
塩化ナトリウム\(NaCl\)の結晶の格子エネルギーは\(772 kJ/mol\)である。
\[NaCl(固)=Na^+(気)+Cl^-(気)-772 kJ\]
実際に、イオン結晶の構成粒子をバラバラにして、気体状態のイオンにすることは困難であるので、イオン結晶の格子エネルギーを直接測定することはできない。したがって、ヘスの法則を用いるなどして格子エネルギーを算出する。
1.4 イオン化エネルギー
原子から1個の電子を取り去って1価の陽イオンにするために必要なエネルギーのことをイオン化エネルギーといいます。
【例】
ナトリウム\(Na(気)\)のイオン化エネルギーは\(496 kJ/mol\)である。
\[Na(気)=Na^+(気)+e^–496kJ\]
1.5 電子親和力
原子が電子を1個受け取って1価の陰イオンになるときに放出される熱量のことを電子親和力といいます。これまで、この記事で紹介したエネルギーはすべて「エネルギー」でありますが、電子親和力だけは「熱」になります。
【例】
塩素\(Cl(気)\)の電子親和力は\(349 kJ/mol\)である。
\[Cl(気)+e^-=Cl^-(気)+349 kJ\]
2. 結合エネルギーに関する計算問題
ここでは、結合エネルギーに関する計算問題の例を紹介します。
\(H-H\)、\(Cl-Cl\)、\(H-Cl\)の結合エネルギーがそれぞれ、\(432 kJ/mol\)、\(239 kJ/mol\)、\(428 kJ/mol\)のとき、\(HCl\)の生成熱を求めよ。
まず、問題文で与えられた結合エネルギーに関する熱化学方程式を作ります。
①\(H-H\)の結合エネルギー
\[H_2(気)=2H(気)-432 kJ\]
②\(Cl-Cl\)の結合エネルギー
\[Cl_2(気)=2Cl(気)-239 kJ\]
③\(H-Cl\)の結合エネルギー
\[HCl(気)=H(気)+Cl(気)-428 kJ\]
次に、\(HCl\)の生成熱を\(Q kJ/mol\)としてこれに関する熱化学方程式を作ります。
\[\frac{1}{2}H_2(気)+\frac{1}{2}Cl_2(気)=HCl(気)+Q kJ\]
これをもとにエネルギー図を作ると次のようになります。
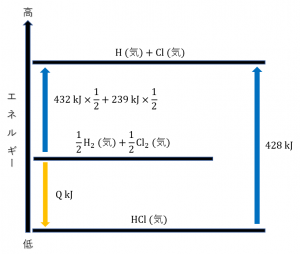
このエネルギー図より、
\[432 kJ\times \frac{1}{2}+239 kJ\times \frac{1}{2}+Q kJ=428 kJ\]
の式が成り立ちます。これより、\(Q=92.5 kJ\)が求まります。
答・・92.5 〔kJ〕
\(H-H\)、\(H-O\)の結合エネルギーがそれぞれ、\(436 kJ/mol\)、\(463 kJ/mol\)、\(H_2O(気)\)の生成熱が\(242 kJ/mol\)のとき、\(O-O\)の結合エネルギーを求めよ。
まず、問題文で与えられた結合エネルギー、生成熱に関する熱化学方程式を作ります。
①\(H-H\)の結合エネルギー
\[H_2(気)=2H(気)-436 kJ\]
②\(H-O\)の結合エネルギー
ここで、この問題に関連して\(H-O結合\)をもっているのは\(H_2O(気)\)であるから、\(H_2O(気)\)を分解して\(2H(気)\)、\(O(気)\)になるときの熱化学方程式を作ります。
\[H_2O(気)=2H(気)+O(気)-926 kJ\]
③\(H_2O(気)\)の生成熱
\[H_2(気)+\frac{1}{2}O_2(気)=H_2O(気)+242 kJ\]
次に、\(O-O\)の結合エネルギーを\(Q kJ/mol\)としてこれに関する熱化学方程式を作ります。
\[O_2(気)=2O(気)-Q kJ\]
これをもとにエネルギー図を作ると次のようになります。
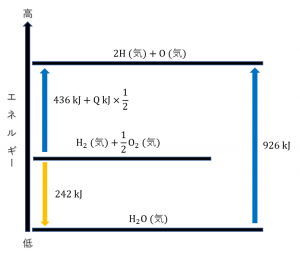
このエネルギー図より、
\[436 kJ+Q kJ\times \frac{1}{2}+242 kJ=926 kJ\]
の式が成り立ちます。これより、\(Q=496 kJ\)が求まります。
答・・496 〔kJ〕
\(NaCl(固)\)の格子エネルギーが\(772 kJ/mol\)、\(Na(気)\)のイオン化エネルギーが\(496 kJ/mol\)、\(Na(固)\)の昇華熱が\(92 kJ/mol\)、\(Cl_2(気)\)の結合エネルギーが\(244 kJ/mol\)、\(Cl(気)\)の電子親和力が\(349 kJ/mol\)となるとき、\(NaCl(固)\)の生成熱を求めよ。
まず、問題文で与えられた結合エネルギー、熱に関する熱化学方程式を作ります。
①\(NaCl(固)\)の格子エネルギー
\[NaCl(固)=Na^+(気)+Cl^-(気)-772 kJ\]
②\(Na(気)\)のイオン化エネルギー
\[Na(気)=Na^+(気)+e^–496 kJ\]
③\(Na(固)\)の昇華熱
\[Na(固)=Na(気)-92 kJ\]
④\(Cl_2(気)\)の結合エネルギー
\[Cl_2(気)=2Cl(気)-244 kJ\]
⑤\(Cl(気)\)の電子親和力
\[Cl(気)+e^-=Cl^-(気)+349 kJ\]
次に、\(NaCl(固)\)の生成熱を\(Q kJ/mol\)としてこれに関する熱化学方程式を作ります。
\[Na(固)+\frac{1}{2}Cl_2(気)=NaCl(固)+Q kJ\]
これをもとにエネルギー図を作ると次のようになります。
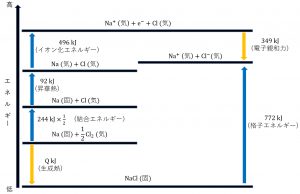
このエネルギー図より、
\[496 kJ+92 kJ+244 kJ\times \frac{1}{2}+Q kJ=349 kJ+772 kJ\]
の式が成り立ちます。これより、\(Q=411 kJ\)が求まります。
答・・411 〔kJ〕
3. まとめ
最後に結合エネルギーについてまとめておこうと思います。
- 共有結合している物質\(1 mol\)をバラバラにして、原子と原子に切り離す際に必要なエネルギーのことを結合エネルギーといいます。
- 分子\(1 mol\)に存在するすべての共有結合を切断するのに必要なエネルギーのことを解離エネルギーといいます。解離エネルギーの値は、分子中に存在するすべての結合の結合エネルギーの総和と等しくなります。
- 結晶を気体の構成粒子まで完全にバラバラにするのに必要なエネルギーのことを格子エネルギーといいます。
- 原子から1個の電子を取り去って1価の陽イオンにするために必要なエネルギーのことをイオン化エネルギーといいます。
- 原子が電子を1個受け取って1価の陰イオンになるときに放出される熱量のことを電子親和力といいます。
結合エネルギーも問題を解くうえで大事な知識です。
値は計算するときに与えられますが、熱化学方程式を作れるようにしっかり理解してください!















解答2のO-Oの結合エネルギーの式
(1/2)O2=2O-QはO2=2O-Qの間違いではありませんか?
今年からエンタルピーとして計算するようになりましたね
ΔH=QkJで反応熱は表す
エネルギー図ではなく、エンタルピー図