東大塾長の山田です。
このページでは電気分解について解説しています。
電気分解は理解することが多く間違えやすいですが、この記事では電気分解についてのすべてのパターンを解説し、それを応用したものや関連した知識についても詳しく説明しています。
是非参考にしてください。
1. 電気分解
1.1 電気分解とは?
電解質の溶液に電極を差し込み電流を流したとき、その電気エネルギーによって電極と溶液の間で酸化還元反応を起こし、電解質が分解される現象のことを電気分解といいます。
また、直流電源の負極に接続した電極のことを陰極といいます。「ボルタ電池とは(仕組み・分極の原理など)」の記事で解説したように、負極は導線に向かって電子が流れ出す電極です。したがって、陰極では電子が与えられます。そのため、陰極では還元反応が起こります。
一方で、直流電源の正極に接続した電極を陽極といいます。正極は導線から電子が流れ込む電極であることから、陽極では電子が奪われます。そのため、陽極は酸化反応が起こります。
1.2 電池と電気分解
電気分解は電池で起こる酸化還元反応と似ていますが、大きく異なる部分が1つあります。それは、不可逆反応であるということです。
電気分解では、安定な状態でいるような物質に強制的にエネルギーを与えて酸化還元反応を引き起こし化合物を分解します。一方で、電池は自発的に酸化還元反応が起こり電気を取り出しています。
また、電池の負極と電気分解の陰極、電池の正極と電気分解の正極、それぞれの違いをしっかり理解しておきましょう。
2. 陽極・陰極での反応
ここでは、電気分解の時に陽極、陰極それぞれで起こる反応について解説していきます。
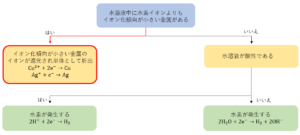
電気分解では、陽極、陰極で起こる反応が電極や水溶液中に含まれるイオンによって変わってきます。どのような反応が起こるかはこれから説明する手順に沿って考えていけば間違えることなく導き出すことができます。
(ここでは、イオン化傾向の知識を利用します。イオン化傾向については、「イオン化傾向とは(覚え方・電池・金属と腐食・大きさの表)」の記事で解説しているので曖昧な人は確認するようにしてください!)
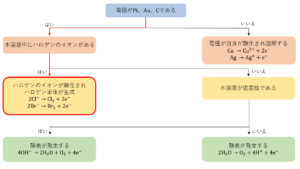
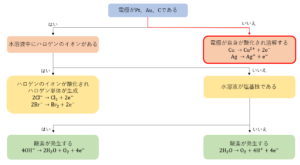
2.1 陽極での反応
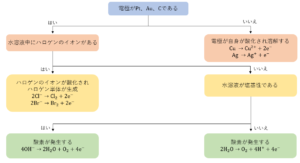
まずは、陽極で起こる反応について考えていきましょう。陽極では酸化反応が起こります。
陽極で起こる反応を決定するには次の①、②を考えます。
①電極が金\(Au\)や白金\(Pt\)、炭素\(C\)であるかどうか
②電解液中にハロゲンのイオンが含まれるかどうか
①電極が金\(Au\)や白金\(Pt\)、炭素\(C\)であるかどうか
まず、①で電極の種類が何かを考えます。陽極の電極が\(Au\)や\(Pt\)、\(C\)であった場合、\(Au\)や\(Pt\)のようなイオン化傾向が小さく安定である金属や\(C\)などの非金属は反応できないので、電極は反応しません。このため、次の②を考えます。
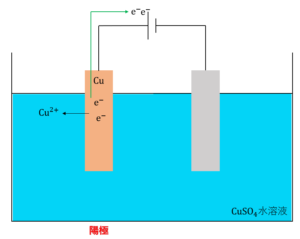
一方で、陽極の電極が\(Au\)や\(Pt\)、\(C\)ではなかった場合(つまり、銀\(Ag\)または、\(Ag\)よりもイオン化傾向が大きい金属であった場合)、電極自身が酸化されてイオンとなって溶け出します。これが陽極での反応となります。例を挙げると以下の通りです。
\(Cu →Cu^{2+} + 2e^-\)
\(Ag →Ag^+ + e^-\)
②電解液中にハロゲンのイオンが含まれるかどうか
①で電極について考えましたが、陽極の電極が\(Au\)や\(Pt\)、\(C\)であった場合は電解液中にハロゲンのイオンが含まれるかどうかを考えます。
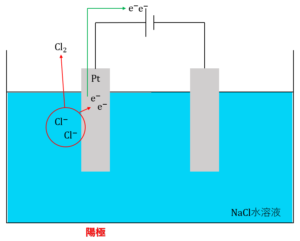
電解液中にハロゲンのイオンが含まれる場合、これらのイオンが酸化され、単体となって発生または析出します。これが陽極での反応となります。例を挙げると以下の通りです。
\(2Cl^- →Cl_2 + 2e^-\)
\(2Br^-→Br_2 + 2e^-\)
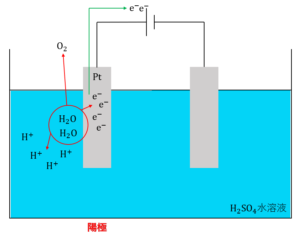
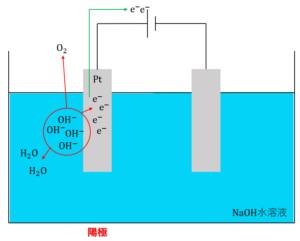
一方で、電解液中にハロゲンのイオンが含まれない場合、陰イオンには硫酸イオン\({SO_4}^{2-}\)や硝酸イオン\({NO_3}^-\)などの酸化されにくいイオンのみを含み、これらのイオンは酸化されず反応しません。したがって、水\(H_2O\)が酸化され、酸素\(O_2\)が発生します。これが陽極での反応となります。ただし、水溶液の液性が塩基性の場合は、水ではなく水酸化物イオン\(OH^-\)が酸化され、酸素\(O_2\)が発生します。
【水溶液の液性が中性、酸性の場合】
\(2H_2O →O_2 + 4H^+ + 4e^-\)
【水溶液の液性が塩基性の場合】
\(4OH^- →2H_2O + O_2 +4e^-\)
このように水溶液の電気分解において、陽極では「電極の溶解」、「ハロゲン単体の生成」、「酸素の発生」のいずれかの反応が起こります。どの反応が起こるかは①、②を順番に考えることで決定することができます。
下の図が陽極で起こる反応を決定するうえで、考える順番とその結果をまとめたものです。
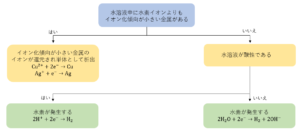
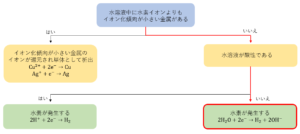
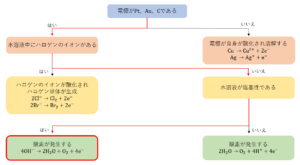
2.2 陰極での反応
次に、陰極での反応を考えましょう。陰極では還元反応が起こります。
陰極で起こる反応を決定するには次のことを考えます。
電解液中に水素イオンよりもイオン化傾向が小さい金属イオンが含まれるかどうか
陽極では電極の種類によって反応が変化しましたが、陰極では電極の種類によって反応が変わることはありません。したがって、陰極では電解液中に含まれるイオンについて考えます。
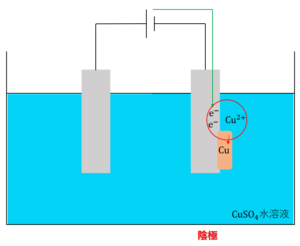
電解液中に水素イオンよりもイオン化傾向が小さい金属イオン(\(Cu\)、\(Ag\)など)が存在する場合、極めて低濃度でもこれらのイオンが還元され、単体となって析出します。これが陰極で起こる反応です。例を挙げると次のようになります。
\(Cu^{2+} + 2e^- →Cu\)
\(Ag^+ + e^- →Ag\)
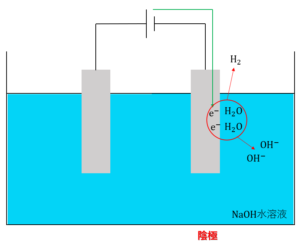
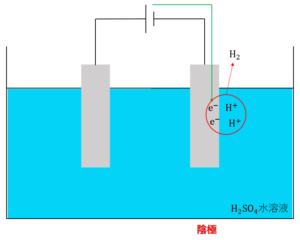
一方で、電解液中にイオン化傾向が大きい金属のイオンのみが存在する場合、どんなに高濃度でもこれらのイオンは還元されません。そのため、水\(H_2O\)が還元され、水素\(H_2\)となって発生します。これが陰極での反応となります。ただし、水溶液の液性が酸性の場合は、水ではなく水素イオン\(H^+\)が還元され、水素\(H_2\)が発生します。
【水溶液の液性が中性、塩基性の場合】
\(2H_2O + 2e^- →H_2 + 2OH^-\)
【水溶液の液性が酸性の場合】
\(2H^+ + 2e^- →H_2\)
このように水溶液の電気分解において、陰極では「重金属単体の析出」、「水素の発生」のどちらかの反応が起こります。
イオン化傾向が中くらいの\(Zn\)、\(Fe\)、\(Ni\)などは電圧や電極の種類、濃度などによって反応が変化します。大学受験においては問われることがないので、上で説明した反応をしっかり覚えるようにしてください!
下の図が陰極で起こる反応を決定するうえで、考える順番とその結果をまとめたものです。
3. 電気分解の例
2では陽極、陰極でそれぞれで起こる反応の決定の仕方を説明しました。ここでは、2で説明したことをもとに実際に具体例を用いて解説していきます。
3.1 塩化ナトリウム水溶液
陽極に炭素\(C\)、陰極に鉄\(Fe\)を用いて、塩化ナトリウム\(NaCl\)水溶液を電気分解するときの反応を考えましょう。
まず、陽極についてです。
電極は炭素\(C\)です。したがって、電極は反応しないのでハロゲンのイオンが電解液中に存在するかを考えます。この水溶液は、塩化ナトリウム\(NaCl\)水溶液で電解液中にハロゲンのイオン\(Cl^-\)が含まれています。よって、このハロゲンイオンが酸化され、塩素\(Cl_2\)に変化します。これがこの水溶液の電気分解において、陽極で起こる反応になります。
\(2Cl^- →Cl_2 + 2e-^-\)
次に、陰極について考えましょう。
陰極では電極の種類に依存せず反応は起こるので、電極は考える必要はありません。それでは、電解液中に水素イオンよりもイオン化傾向が小さい金属イオンが含まれるか見てみましょう。この水溶液に含まれている金属イオンは、ナトリウムイオン\(Na^+\)です。これは、イオン化傾向がかなり大きく還元され単体として生成することはありません。これより、陰極では水素が発生する反応が起こることがわかりますね。水溶液の液性は中性であるので、陰極での反応は次のようになります。
\(2H_2O + 2e^- →H_2 + 2OH^-\)
陽極、陰極の反応式から電子を消去し、水溶液中に存在するナトリウムイオン\(Na^+\)を付け加えると次の反応式が得られます。
\(2NaCl + 2H_2O →2NaOH + H_2 + Cl_2\)
これが塩化ナトリウム水溶液を電気分解したときの全体の反応を表した反応式です。
3.2 硝酸銀水溶液
両極に銀\(Ag\)を用いて、硝酸銀\(AgNO_3\)水溶液を電気分解するときの反応を考えましょう。
まず、陽極についてです。
電極は銀\(Ag\)です。電極は金\(Au\)や白金\(Pt\)、炭素\(C\)ではないので、電極自身が酸化され溶解します。このときの反応式は、
\(Ag →Ag^+ + e^-\)
となります。
次に、陰極について考えましょう。
陰極では電極の種類に依存せず反応は起こるので、電極は考える必要はありません。それでは、電解液中に水素イオンよりもイオン化傾向が小さい金属イオンが含まれるか見てみましょう。この水溶液に含まれている金属イオンは、銀イオン\(Na^+\)です。これは、イオン化傾向が水素イオンよりも小さくなるため、還元され単体として生成します。
\(Ag^+ + e^- →Ag\)
この電気分解の全体の反応を考えると、陽極で溶解した銀イオンが陰極で銀として生成すると考えることができます。
3.3 水酸化ナトリウム水溶液
両極に白金\(Pt\)を用いて、水酸化ナトリウム\(NaOH\)水溶液を電気分解するときの反応を考えましょう。
まず、陽極についてです。
電極は白金\(Pt\)です。したがって、電極は反応しないのでハロゲンのイオンが電解液中に存在するかを考えます。この水溶液は、水酸化ナトリウム\(NaOH\)水溶液で電解液中にハロゲンのイオンは含まれていません。よって、陽極では酸素が発生する反応が起こります。この水溶液は塩基性であるので、水酸化ナトリウム水溶液の電気分解において、陽極で起こる反応は次のようになります。
\(4OH^- →2H_2O + O_2 + 4e-^-\)
次に、陰極について考えましょう。
陰極では電極の種類に依存せず反応は起こるので、電極は考える必要はありません。それでは、電解液中に水素イオンよりもイオン化傾向が小さい金属イオンが含まれるか見てみましょう。この水溶液に含まれている金属イオンは、ナトリウムイオン\(Na^+\)です。これは、イオン化傾向がかなり大きく還元され単体として生成することはありません。これより、陰極では水素が発生する反応が起こることがわかりますね。水溶液の液性は塩基性であるので、陰極での反応は次のようになります。
\(2H_2O + 2e^- →H_2 + 2OH^-\)

陽極、陰極の反応式から電子を消去し、水溶液中に存在するナトリウムイオン\(Na^+\)を付け加えると次の反応式が得られます。
\(2H_2O →2H_2 + O_2\)
これが水酸化ナトリウム水溶液を電気分解したときの全体の反応を表した反応式です。この反応は水の電気分解によって\(H_2\)と\(O_2\)が発生します。
4. 電気分解の化学工業での応用例
これまで、電気分解の仕組みについて説明してきました。現在の化学工業ではこの電気分解を利用したものがたくさんあります。ここでは、その一部を詳しく説明していきます。
4.1 金属のメッキ
金属は酸素や酸と反応して腐食します。腐食する際に、金属にはさびが生じます。さびとは、金属が空気中で腐食されて生じた酸化物や水酸化物のことをいいます。
このようなさびを防ぐために有効な方法の1つとして、メッキといわれるものがあります。メッキとは物質の表面を薄い金属で覆うことをいいます。特に、電気分解を利用したメッキのことを電気メッキといいます。
例として、銅\(Cu\)板の表面を銀\(Ag\)で電気メッキすることを考えましょう。
この電気メッキでは、電解液に硝酸銀\(AgNO_3\)水溶液、陽極に\(Ag\)板、陰極に\(Cu\)板を使います。このとき、各極で起こる反応は次のようになります。
陽極:\(2H_2O→4H^+ +O_2+ 4e^-\)
陰極:\(Ag^+ + e^- →Ag\)
陽極では、銀板が酸化され銀イオンとなり電解液中に溶けだし、陰極では、電解液中の銀イオンが還元され銀となり銅板に析出します。(各極での反応は2で解説した考え方に基づいて求めることができます。)
全体としては見かけ上、銀が陽極から陰極版の表面に移動することになり、実際には銅板が銀でメッキされます。
他の電気メッキの例には、クロムメッキがあります。これは、鉄\(Fe\)の表面をクロム\(Cr\)で電気メッキするものです。クロムイオンを含んだ水溶液を電解液として、陰極に\(Fe\)を用いて電気分解を行うことでメッキすることができます。
4.2 イオン交換膜法
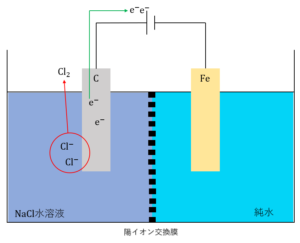
塩化ナトリウム\(NaCl\)水溶液の電気分解を用いて純度の高い水酸化ナトリウム\(NaOH\)を作る方法のことをイオン交換膜法といいます。これは、水酸化ナトリウムの工業的製法として知られています。
この電気分解では、陽極に炭素\(C\)電極、陰極に鉄\(Fe\)電極を使います。また、陽極側の電解液に塩化ナトリウム\(NaCl\)水溶液、陰極側の電解液に純水を用いて電気分解を行います。
このとき、陽極側の電解液と陰極側の電解液が混ざらないように、両者の間に陽イオン交換膜を使用します。陽イオン交換膜とは、合成樹脂でできた膜で陽イオンだけを通す性質を持っています。
では、各極で起こる反応を見ていきましょう。
まず、陽極側の塩化物イオン\(Cl^-\)が酸化され、塩素\(Cl_2\)が発生します。
\(2Cl^- →Cl_2 + 2e^-\)
このとき発生した電子\(e^-\)が陽極側に流れ込み、これと水が反応することで水が還元され水素\(H_2\)が生成します。
\(2H_2O + 2e^- →H_2 + 2OH^-\)
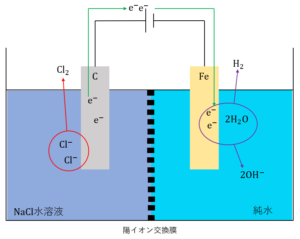
このように、陽極では塩化物イオンが減少し、陰極では水酸化物イオンが増加します。したがって、陽極ではナトリウムイオン\(Na^+\)が多く存在するため+に、陰極では水酸化物イオンが多く存在するため-に帯電します。これによって、陽極側の電解液と陰極側の電解液の間で電荷の偏りが生じます。
この偏りをなくすために陽イオン交換膜が働くのです。陽極側に過剰に存在するナトリウムイオンが陽イオン交換膜を通って陰極側に流れ込みます。陽イオン交換膜は陽イオンしか通さないので他のイオンは移動することができません。このようにして、両極の電解液の間での電荷が等しくなるように調整するのです。
また、陰極側に移動したナトリウムイオンと陰極での反応で生成した水酸化物イオンが反応して水酸化ナトリウム\(NaOH\)が生成するのです。陰極側には塩化物イオンは移動しないので純度の高い水酸化ナトリウムを得ることができます。
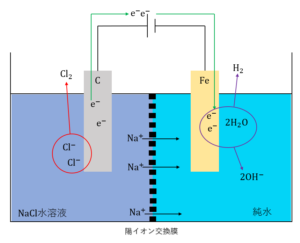
全体でのこの電気分解の反応式は次のようになります。
\(2NaCl + 2H_2O →2NaOH + H_2 + Cl_2\)
\(NaCl\)水溶液が電気分解され、陰極で\(H_2\)、陽極で\(Cl_2\)が発生し、陰極側の電解液中に\(NaOH\)が生成します。
4.3 銅の電解精錬
鉱石から製錬によって得られた金属から、不純物を取り除き金属の純度を高める操作のことを精錬といいます。製錬を電気分解を利用して行うことを電気精錬といいます。
ここでは、銅の電解精錬について説明していきます。これは、不純物を含む銅(粗銅)から純度の高い銅(純銅)を製造する方法のことで、陽極には粗銅(不純物を含む銅)板を、陰極には薄い純銅(純度の高い銅)を使い、電解液には硫酸銅(Ⅱ)\(CuSO_4\)水溶液を用いて電気分解を行います。この電気分解は、約\(0.3V\)の低電圧で長時間行います。
では、実際にどのような反応が起こっているのか詳しく見ていきましょう。
まず、陽極の粗銅\(Cu\)が酸化され、銅イオン\(Cu^{2+}\)となり電解液中に溶解します。
\(Cu →Cu^{2+} + 2e^-\)
今まで説明してきた電気分解では各電極で1つの反応しか起こりませんでしたね。しかし、銅の電解精錬における電気分解は他の電気分解とは少し違います。
陽極には粗銅板を使いましたが、粗銅とは不純物を含む銅のことでした。つまり、銅以外に他の金属が含まれているのです。したがって、電気分解を行うと銅以外の金属が反応してしまうのです。
どのように反応するかは金属のイオン化傾向によって以下のように2つに分けられます。
【\(Cu\)よりもイオン化傾向が大きい金属】
粗銅板中に含まれる\(Zn\)や\(Fe\)、\(Ni\)などの\(Cu\)よりもイオン化傾向が大きい金属は、電気分解を行うことで酸化されそれぞれ\(Zn^{2+}\)、\(Fe^+{2+}\)、\(Ni^{2+}\)に変化し電解液中に溶け出します。
\(Zn →Zn^{2+} + 2e^-\)
\(Fe →Fe^{2+} + 2e^-\)
\(Ni →Ni^{2+} + 2e^-\)
しかしこれらのイオンは\(Cu^{2+}\)とは異なり、陰極で還元され単体として析出することはありません。
【\(Cu\)よりもイオン化傾向が小さい金属】
粗銅板中に含まれる\(Au\)や\(Pt\)、\(Ag\)などの\(Cu\)よりもイオン化傾向が小さい金属は、これらを取り囲んでいる\(Cu\)が溶け出すと、そのまま単体として陽極の下に沈殿します。この沈殿のことを陽極泥といいます。
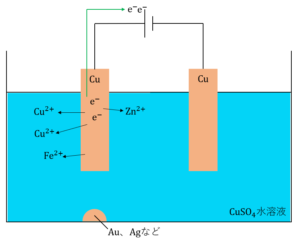
また、陰極では電解液中の\(Cu^{2+}\)(陽極から溶け出した\(Cu^{2+}\)と、もともと\(CuSO_4\)水溶液に含まれていた\(Cu^{2+}\))が還元され、\(Cu\)単体となり純銅板上に析出します。
\(Cu^{2+} + 2e^- →Cu\)
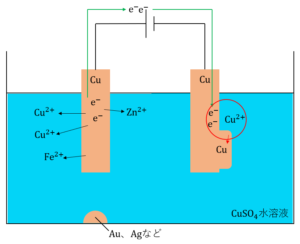
全体としては、見かけ上\(Cu\)が陽極から陰極に移動するということになります。
4.4 アルミニウムの融解塩電解
アルミニウムやナトリウムなどのイオン化傾向が非常に大きい金属は、その金属のイオンを含む水溶液を電気分解しても水溶液中の水が還元されてしまうため、目的の金属イオンが還元されず金属単体を得ることができません。
このようなイオン化傾向が非常に大きい金属の単体を得る方法として融解塩電解があります。融解塩電解とは、水溶液ではなく、金属の塩や酸化物、水酸化物などの融解液を電気分解することで金属の単体を生成する方法のことです。\(Al\)や\(Na\)などの金属の酸化物や水酸化物、塩化物を高温で融解して液体にし、水を含まない状態で電気分解を行うのです。
ここでは、アルミニウムの融解塩電解を例に説明します。
アルミニウムの融解塩電解では、酸化アルミニウム\(Al_2O_3\)の融解液を電解液とし、電極には炭素\(C\)を用いて電気分解をします。
まず、陰極で起こる反応を見ていきましょう。
陰極では、融解液中のアルミニウムイオン\(Al^{3+}\)が還元され、融解状態のアルミニウム\(Al\)となり陰極に析出します。
\(Al^{3+} + 3e^- →Al\)
また、陽極では電極の炭素\(C\)が酸化され、一酸化炭素\(CO\)、または二酸化炭素\(CO_2\)が発生し電極の炭素は消費されます。そのため、電極の炭素は補充する必要があります。
\(C + O^{2-} →CO + 2e^-\)
\(C + 2O^{2-} →CO_2 + 4e^-\)
5. ファラデー定数
5.1 ファラデーの電気分解の法則
電極で変化するイオンの物質量は流れた電気量に比例することをファラデーの電気分解の法則といいます。
例えば、次のような反応が起こったとしましょう。
\(2Cl^- →Cl_2 + 2e^-\)
このような反応では、\(2 mol\)の電子が流れたとき、塩素イオン\(2 mol\)が減少し塩素\(1 mol\)が発生するということを意味します。
5.2 ファラデー定数
\(1A(アンペア)\)の電流が\(1秒間\)流れたときの電気量を\(1C(クーロン)\)という単位で表します。
\(1〔A〕=1〔C/s〕\)
また、\(1 mol\)の電子\(e^-\)が持つ電気量のことをファラデー定数といいます。ファラデー定数の値は\(9.65 \times 10^4〔C/mol〕\)です。
これは、電子1個が持つ電気量\(1.602 \times 10^{-19}〔C〕\)、アボガドロ定数\(6.022 \times 10^{23}〔/mol〕\)をかけることで求めることができます。
\(1.602 \times 10^{-19}〔C〕 \times 6.022 \times 10^{23}〔/mol〕=9.65 \times 10^4〔C/mol〕\)
5.3 例題
5.2ではファラデー定数について説明しました。ここでは、ファラデー定数を使った例題を紹介します。
\(Cu^{2+} + 2e^- →Cu\)
銅の電解精錬において、陰極では上の式のような反応が起こった。このとき、次の(1)、(2)の問いに答えよ。銅の原子量は\(64 g/mol\)、ファラデー定数は\(9.65 \times 10^4 C/mol\)とする。答えは有効数字2桁で求めよ。
(1) \(2.5A\)である程度の時間電流を流したら、陰極の質量は\(2.56 g\)増加した。このとき、電流を何秒流したのか求めよ。
(2) \(5.0A\)で193秒間電流を流した。このとき、陰極の質量はどれだけ増加したか求めよ。
【解答】
(1)
電流を\(x\)秒間流したとします。単位アンペア\(A\)は\(A=C/s\)であるので、このときに流れた電気量は\(2.5〔C/s〕\times x〔s〕\)と表すことができます。
また、陰極では銅が析出し質量は\(2.56 g\)増加したので、増加した銅の物質量は\(\displaystyle \frac{2.56}{64}〔mol〕\)となります。陰極で起こった反応の反応式から流れた電子と析出した銅の物質量の比は\(2:1\)となります。この関係を使ってこの反応で流れた電気量を表すことができ、\(\displaystyle 2 \times \frac{2.56}{64} \times 9.65 \times 10^4〔C〕\)となります。
これより、
\(\begin{align}
\displaystyle 2.5〔C/s〕\times x〔s〕&=2 \times \frac{2.56}{64} \times 9.65 \times 10^4〔C〕\\
\\
x &=3.1 \times 10^3 〔s〕\\
\\
\end{align}\)
答‥3.1×103〔s〕
(2)
流れた電子の物質量は\(\displaystyle \frac{5.0〔C/s〕\times 193〔s〕}{9.65 \times 10^4〔C/mol〕}〔mol〕\)です。電子と析出した銅の物質量の比は\(2:1\)であるから陰極で増加した質量を\(y〔g〕\)とすると、
\(\begin{align}
\displaystyle y &=\frac{5.0 \times 193}{9.65 \times 10^4} \times \frac{1}{2} \times 64 \\
\\
&=0.32〔g〕\\
\\
\end{align}\)
答‥0.32〔g〕
6. まとめ
最後に電気分解についてまとめておこうと思います。
電気分解のときの陽極で起こる反応を決定する手順は以下の通りです。
電気分解のときの陰極で起こる反応を決定する手順は以下の通りです。

電気分解は様々なパターンがあるのでよく出題されます。
計算問題を出題されることが多いですが、どのような反応が起こるのかしっかり導き出せないと確実に解くことはできません。
曖昧な部分がなくなるまでこの記事を何度も読んでしっかりマスターしてください!














電気分解の陰極‥電子が与えられ、還元反応が起こる。
電池の負極‥電子を押し出し、酸化反応が起こる。
電気分解の陽極‥電子が奪われて、酸化反応が起こる。
電池の正極‥電子を引き込み、還元反応が起こる。