東大塾長の山田です。
このページでは、「定積変化」について詳しく説明しています。ぜひ勉強の参考にしてください!
また、この内容を扱うにおいて熱力学第一法則の知識が不可欠です。「熱力学第一法則と熱力学の枠組み」の解説記事の内容を理解してから読むと、より理解が深まるので,ぜひこちらも参考にしてください。
1. 定積変化について
それでは,定積変化について解説していきます。
1.1 定積変化とは
定積変化とは、文字通り気体が入った容器の体積を一定とした状態変化のことです。
実際にどのような変化が定積変化となりうるのか、以下の例を用いて確認してみましょう!
以下のように、質量 \( m \)、断面積 \( S \) のピストンが固定された状態で、容器内の気体を加熱したとします。このとき、ピストンは固定されているので、体積は一定です。(大気圧は無視)
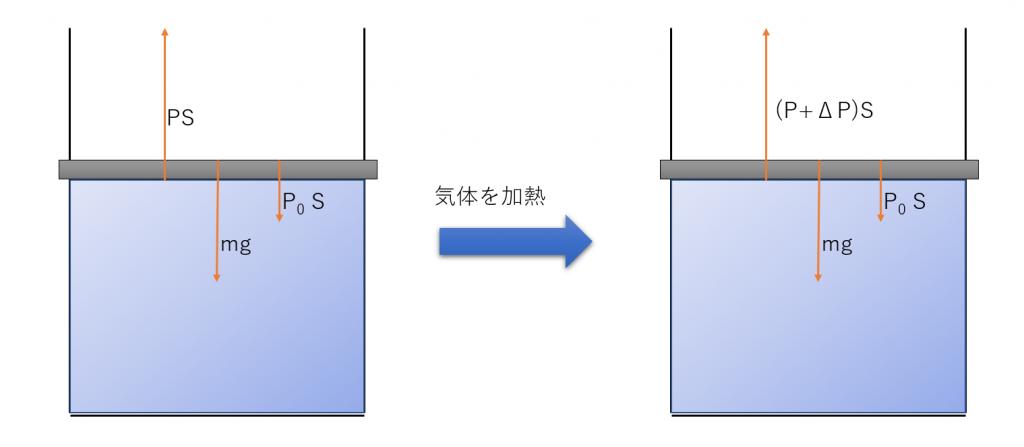
上図において、圧力も \( P \) から \( P + \Delta P \) に上昇します。
これはボイル・シャルルの法則からも説明できますし、分子運動の観点から考えても、温度が上昇すると、内部エネルギーと気体分子の速さが大きくなり、ピストンに分子が衝突する回数が増え、気体の圧力が大きくなる、という風に説明することができます。
このとき、容器の体積が変化していないため、気体のした仕事\(W\)はゼロです。
よって定積変化における熱力学第一法則は以下のようになります。
上の式より、定積変化においては気体が加えた熱は、すべて内部エネルギーの増加となる、ことが分かります!
1.2 P-Vグラフによる議論
定積変化が起こっている場合、どのようなことが起こっているのでしょうか?P-Vグラフを用いて議論していきましょう!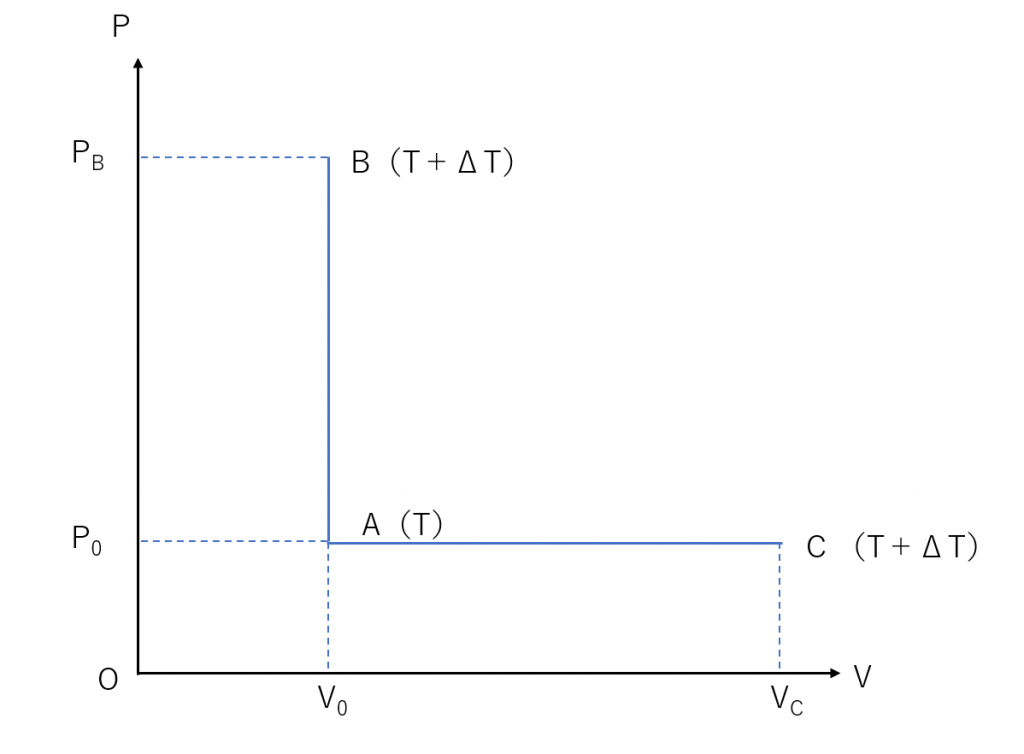
上のように、\( n \) [mol]の気体が状態A、B、Cを取る状況を考えてみましょう。ただしAにおける温度を \( T \) [K]、B・Cにおける温度を \( T + \Delta T \) とします。
このとき、定積変化である変化は、A⇒B と B⇒Aです。二つの変化について同時に考察していきます。
状態方程式
AとBにおける状態方程式は
\( \begin{cases}
\displaystyle P_0 V_0=nRT \\
\displaystyle P_B V_0=nR\left(T+\Delta T \right)
\end{cases} \)
内部エネルギー変化
内部エネルギー変化は温度変化のみに依存するから、それぞれの過程における内部エネルギー変化は、
\( \displaystyle \left\{\begin{array}{l}{\displaystyle \Delta U_{A B} = \frac{3}{2} n R\Delta T} \\ {\displaystyle \Delta U_{B A} = – \frac{3}{2} n R \Delta T }\end{array} \right. \)
仕事
ここで、気体が外部にした仕事は、P-V図の面積となります。
先ほどの説明した通り、定積変化においてはP-Vグラフの面積がゼロになってしまうので、それぞれ過程における気体がした仕事は、
\( \begin{cases}
\displaystyle W_{AB} = \int_{V_{0}}^{V_{0}} P_{0} d V=0 \\
\displaystyle W_{BA} = \int_{V_{0}}^{V_{0}} P_{0} d V=0
\end{cases} \)
となります。
あとはこれを定積変化における熱力学第一法則 \( Q = \Delta U \) に代入すると、
\( \begin{cases}
\displaystyle \Delta U_{AB} = \frac{3}{2}nR\Delta T \\
\displaystyle \Delta U_{BA} = – \frac{3}{2}nR \Delta T
\end{cases} \)
が得られます!
定積モル比熱
吸熱量が分かったところ、定積モル比熱を求めることができます。
モル比熱とは、1molの気体の温度を1K上げるために必要な熱量のことで、
\( \displaystyle (モル比熱) = \frac{(吸熱量)}{(モル数) \times (温度変化)} \)
で計算することができる。
それぞれ計算してみると、
A⇒B におけるモル比熱 \( C_V \) は、
\( \displaystyle C_V = \frac{Q_{AB}}{n\Delta T} = \frac{3}{2}R \)
B⇒A におけるモル比熱 \( C_V \) は、
\( \displaystyle C_V = \frac{Q_{BA}}{-n\Delta T} = \frac{3}{2}R \)
となります。
\( \displaystyle C_V = \frac{3}{2}R \)
2. まとめ
以上が定積変化における議論となります!
最後に今回学んだことをまとめておくので、復習に役立ててください!
熱力学第一法則:\( \displaystyle \Delta U = Q \)
定積モル比熱:\( \displaystyle C_V = \frac{3}{2}R \)














\( \displaystyle \Delta U = Q \)