東大塾長の山田です。
このページでは「実在気体の状態方程式」について解説しています。
ここでは、実在気体の状態方程式を自分で導き出せるように詳しく説明しています。是非参考にしてください。
(ファンデルワールス力については、「イオン結晶・共有結合の結晶・分子結晶」の記事で解説しているのでそちらを参照してください。)
1. 実在気体の状態方程式
理想気体の状態方程式については、「理想気体と実在気体・状態方程式」の記事で説明したように、 \( \displaystyle P_{理想} V_{理想} = nRT \) となります。
理想気体は分子自身の体積と分子間に働く引力を無視しています。
しかし、実際に存在する実在気体には分子自身の体積、分子間に働く引力があります。
ここでは、実在気体に適用できる実在気体の状態方程式について説明します。
1.1 分子自身の体積
理想気体では、分子自身の体積を0と仮定していると説明しました。
しかし、実在気体には分子自身の体積があります。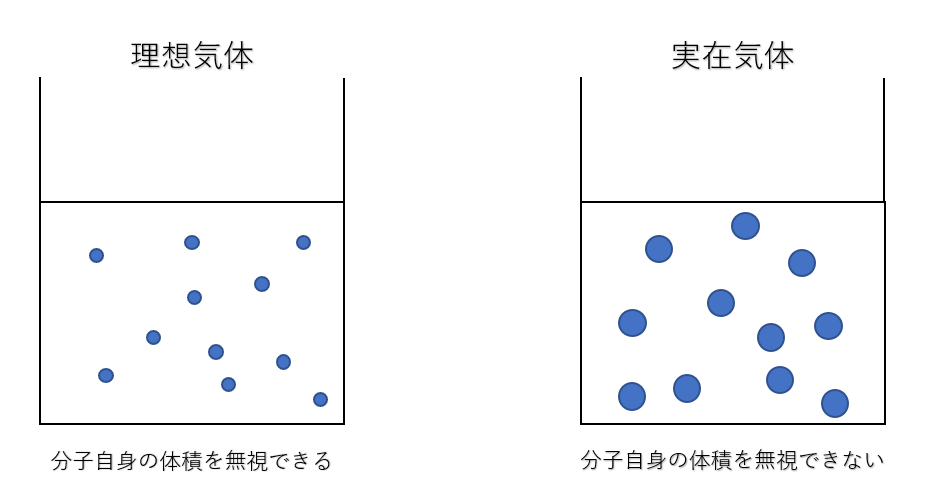
上図のように、実在気体では、その分子は分子自身の体積をもっているため、内容積分だけ動き回れるわけではありません。
上図の右の実在気体を下に集めて考えてみましょう。
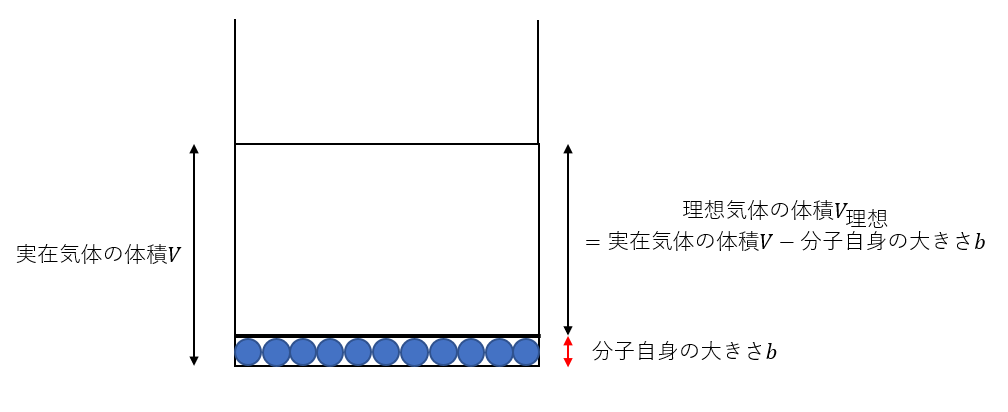
分子が動き回れるのは、内容積から分子自身の体積を引いた部分だけになるのです。
そのため、気体の体積は、実在気体よりも理想気体の方が小さくなります。
ここで、実在気体 \( 1mol \) あたりの分子自身の大きさを \( b \) とすると、実在気体の体積 \( V \) と理想気体の体積 \( V_{理想} \) との間には
\( \displaystyle \color{red}{ V=V_{理想}+nb } \)
すなわち,\( \displaystyle \color{red}{ V_{理想}=V-nb } \cdots ① \)
の関係式が成り立ちます。
ちなみに、ここで \( b \) は、分子自身の体積を反映した気体の種類によって異なる定数です。
1.2 分子間に働く引力
理想気体では、分子間に働く引力がないと説明しました。
しかし、実在気体には、分子間に働く引力があります。
理想気体では、その分子は分子間に引力が働かないため、その分子の内側にある他の分子に引きとめられることはなく内壁に衝突します。
その一方で、実在気体では、その分子は、分子間に引力が働くため、その分子の内側にあってそれに引力を及ぼす他の分子に引きとめられながら内壁に衝突します。
そのため、気体が示す圧力は、理想気体の方が実在気体よりも大きくなります。
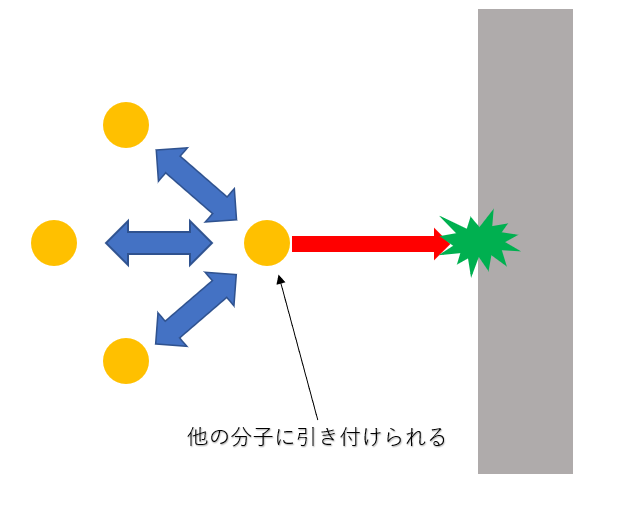
分子間力は、引きとめられる分子から見ると、まわりに存在する分子の数に比例します。
つまり、気体の分子数密度 \( \displaystyle \frac{n}{V} \) に比例します。
また、壁に衝突する数も分子数密度 \( \displaystyle \frac{n}{V} \) に比例します。
比例定数を \( a \) とすると、実在気体の圧力 \( P \) と理想気体の圧力 \( P_{理想} \) との間には
\( \displaystyle \color{red}{ P = P_{理想} – a \left( \frac{n}{V} \right)^2 } \)
すなわち,\( \displaystyle \color{red}{ P_{理想} = P + a \left( \frac{n}{V} \right)^2 } \cdots ② \)
の関係式が成り立ちます。
ちなみに、ここで \( a \) は、分子間に働く引力を反映した、気体の種類によって異なる定数です。
1.3 実在気体の状態方程式
1.1、1.2より理想気体の状態方程式 \( P_{理想} V_{理想} = nRT \) に、①式、②式を代入することで、実在気体の状態方程式が得られます。
この式は、ファンデルワールスの状態方程式と呼ばれます。
また、上式の定数 \( a \)、\( b \) はともにファンデルワールス定数と呼ばれます。
2. まとめ
さいごに,実在気体の状態方程式についてまとめます。
実在気体の状態方程式は,\( a \),\( b \) を定数とすると
\( \displaystyle \color{red}{ \left\{ P + a \left( \frac{n}{V} \right)^2 \right\} \left( V -nb \right) = nRT } \)
入試では、実在気体の状態方程式が出たことがあります。
覚えていなくても、ここで説明した考え方を覚えていれば自分で導出することができると思います。
自分で導き出せるようにしっかりマスターしてください!















\( \displaystyle \color{red}{ \left\{ P + a \left( \frac{n}{V} \right)^2 \right\} \left( V -nb \right) = nRT } \)